Протактиний (Pa)
АктиноидТвёрдое тело
Стандартный атомный вес
231.03588 uЭлектронная конфигурация
[Rn] 7s2 5f2 6d1Температура плавления
1571.85 °C (1845 K)Температура кипения
N/AПлотность
1.537000e+4 kg/m³Степени окисления
+2, +3, +4, +5Электроотрицательность (Полинг)
1.5Энергия ионизации (1-я)
Год открытия
1913Атомный радиус
180 pmДополнительно
Протактиний — плотный серебристый металл-актинид с атомным номером 91. Он находится между торием и ураном и химически примечателен стабильностью степени окисления +5, хотя соединения +4 также известны. Все изотопы радиоактивны. Природный протактиний встречается лишь в следовых количествах, главным образом как ²³¹Pa в ряду распада ²³⁵U и как краткоживущие продукты в других цепочках распада, поэтому он имеет мало технологического значения вне ядерных и геохимических исследований.
Металлический протактиний представляет собой плотный серебристо-серый материал с ярким металлическим блеском, который он сохраняет в течение некоторого времени на воздухе, однако легко реагирует с кислородом, водяным паром и неорганическими кислотами с образованием различных соединений. В твёрдых соединениях протактиний наиболее устойчив в степени окисления +5, но он также существует в степенях окисления +4, +3 и +2. В растворе состояние +5 быстро гидролизуется, соединяясь с гидроксид-ионами с образованием растворимых или нерастворимых гидроксооксидных твёрдых фаз, которые имеют тенденцию прилипать к поверхностям сосудов, в которых они содержатся. Известен ряд соединений протактиния, некоторые из которых окрашены. Элемент сверхпроводящ ниже 1.4K.
Название происходит от греческого protos (первый) и связано с тем, что элемент предшествует актинию, поскольку его наиболее распространённый изотоп (231Pa) распадается с образованием 227Ac при испускании α-частицы.
В 1913 году немецкие химики К. Фаянс и О. Г. Горинг идентифицировали первый изотоп протактиния, 234Pa, и предложили название brevium из-за короткого периода полураспада этого изотопа, составляющего 6,7 ч. 231Pa с более длительным периодом полураспада 3,25(1)×104 a был идентифицирован в 1918 году немецким химиком О. Ганом и австрийским физиком Л. Мейтнер; независимо от них, в Великобритании — Ф. Содди и Дж. А. Кранстоном.
Протактиний был впервые идентифицирован Касимиром Фаянсом и О. Х. Гёрингом в 1913 году при изучении цепи распада урана. Обнаруженный ими конкретный изотоп, протактиний-234m, имеет период полураспада около 1,17 минуты. Они назвали элемент brevium, что означает «краткий», а затем продолжили свои исследования. Существование протактиния было подтверждено в 1918 году, когда другой изотоп, протактиний-231, был независимо открыт и изучен двумя группами учёных: Отто Ганом и Лизе Мейтнер в Германии и Фредериком Содди и Джоном Кранстоном в Великобритании. Протактиний был впервые выделен Аристидом В. Гроссе в 1934 году. Протактиний — редкий, ядовитый и дорогой элемент, присутствующий в урановых рудах в очень малых количествах. В 1961 году Управление по атомной энергии Великобритании смогло получить 125 г протактиния чистотой 99,9 %, хотя для этого пришлось переработать около 55 000 кг руды и потратить около 500 000 долларов.
Наиболее стабильный изотоп протактиния, протактиний-231, имеет период полураспада около 32 760 лет. Он распадается с образованием актиния-227 посредством α-распада.
Название «протактиний» образовано добавлением греческого protos, означающего «первый», перед словом «актиний». В 1871 году Дмитрий Менделеев предсказал существование элемента между торием и ураном. В 1900 году Уильям Крукс выделил протактиний из урана. Это было сильно радиоактивное вещество, однако он не смог охарактеризовать его как новый химический элемент и поэтому назвал его uranium-X. В 1913 году первый изотоп элемента 91, 234Pa, был открыт К. Фаянсом и О. Х. Гёрингом. Это был очень короткоживущий член естественного ряда распада 238U, и поэтому они назвали его «brevium». В 1917/18 годах две группы учёных — Отто Ган и Лизе Мейтнер в Германии и Фредерик Содди и Джон Кранстон в Великобритании — независимо открыли другой изотоп протактиния, 231Pa, имеющий гораздо более длительный период полураспада, около 32 000 лет. Название было изменено на proto-actinium как более соответствующее более долгоживущим характеристикам наиболее распространённого изотопа. В 1927 году Гроссе приготовил 2 мг белого порошка, который был идентифицирован как Pa2O5. В 1934 году он выделил элемент из 0,1 г чистого Pa2O5 двумя методами, один из которых заключался в превращении оксида в иодид и его «раскалывании» в высоком вакууме электрически нагреваемой нитью по реакции: 2PaI5 > 2Pa + 5I2. В 1949 году IUPAC сократил название protoactinium, официально назвав его protactinium и признав Гана и Мейтнер сооткрыватели. Новое название означало «родитель актиния» и отражало тот факт, что актиний является продуктом распада радиоактивного протактиния.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
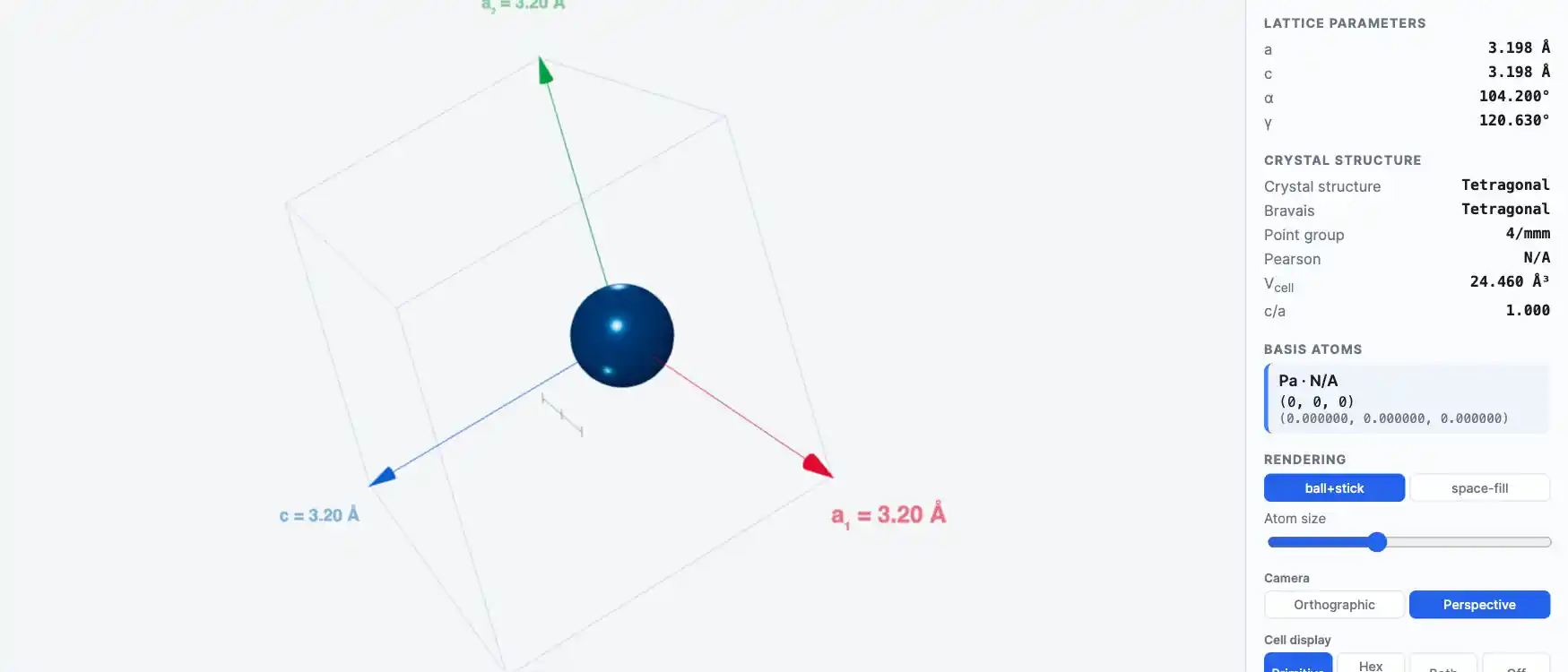
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Pa: 5f² 6d¹ 7s²[Rn] 5f² 6d¹ 7s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹⁰ 6s² 6p⁶ 5f² 6d¹ 7s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
Нет стабильных изотопов.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 224 Радиоактивный | 224,0256176 ± 0,0000082 | N/A | 844 мс |
| 218 Радиоактивный | 218,020059 ± 0,00002 | N/A | 108 us |
| 216 Радиоактивный | 216,019109 ± 0,000057 | N/A | 105 мс |
| 219 Радиоактивный | 219,019904 ± 0,000055 | N/A | 56 ns |
| 227 Радиоактивный | 227,0288054 ± 0,000008 | N/A | 38.3 минут |
Фазовое состояние
Причина: на 1546.8 °C ниже точки плавления (1571.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 91 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Pa I | 0 | 55 | 0 | 0 |
| Pa II | +1 | 33 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Pa I | 0 | 2 |
| Pa II | +1 | 2 |
| Pa III | +2 | 2 |
| Pa IV | +3 | 2 |
| Pa V | +4 | 2 |
| Pa VI | +5 | 2 |
| Pa VII | +6 | 2 |
| Pa VIII | +7 | 2 |
| Pa IX | +8 | 2 |
| Pa X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 104 пм |
| +3 | 9 | N/A | 119.9 пм |
| +4 | 6 | N/A | 90 пм |
| +4 | 8 | N/A | 101 пм |
| +5 | 6 | N/A | 78 пм |
| +5 | 8 | N/A | 91 пм |
| +5 | 9 | N/A | 95 пм |
Соединения
Изотопы (5)
Twenty-nine radioisotopes of protactinium have been discovered. Nearly all naturally occurring protactinium is 231Pa with a half-life of 32,700 years. It is an alpha emitter and is formed by the decay of uranium-235, whereas the beta radiating protactinium-234 with a half-life of 6.74 hours is produced as a result of uranium-238 decay. Nearly all uranium-238 (99.8%) decays first to the 234mPa isomer and then to 234Pa. Smaller trace amounts of the short-lived nuclear isomer protactinium-234m occur in the decay chain of uranium-238. Protactinium-233 results from the decay of thorium-233 as part of the chain of events used to produce uranium-233 by neutron irradiation of thorium-232.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 224 Радиоактивный | 224,0256176 ± 0,0000082 | N/A | 844 мс | α ≈100%β+ ? | |
| 218 Радиоактивный | 218,020059 ± 0,00002 | N/A | 108 us | α =100% | |
| 216 Радиоактивный | 216,019109 ± 0,000057 | N/A | 105 мс | α ≈100%β+ ? | |
| 219 Радиоактивный | 219,019904 ± 0,000055 | N/A | 56 ns | α =100%β+ ? | |
| 227 Радиоактивный | 227,0288054 ± 0,000008 | N/A | 38.3 минут | α =85±0.2%ε =15±0.2% |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Фазовые переходы и аллотропы
| Температура плавления | 1845.15 K |
Категории степеней окисления
Расширенные справочные данные
Детализация кристаллических радиусов (7)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 118 | estimated, | |
| 4 | VI | 104 | from r^3 vs V plots, | |
| 4 | VIII | 115 | ||
| 5 | VI | 92 | ||
| 5 | VIII | 105 | ||
| 5 | IX | 109 | ||
| 3 | IX | — | 133.9 |
Режимы распада изотопов (51)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 211 | A | 100% |
| 211 | B+ | — |
| 211 | p | — |
| 212 | A | 100% |
| 213 | A | 100% |
| 214 | A | 100% |
| 215 | A | 100% |
| 216 | A | 100% |
| 216 | B+ | — |
| 217 | A | 100% |
Факторы рассеяния X‑лучей (516)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.75788 |
| 10.1617 | — | 1.76101 |
| 10.3261 | — | 1.76414 |
| 10.4931 | — | 1.76728 |
| 10.6628 | — | 1.73466 |
| 10.8353 | — | 1.69295 |
| 11.0106 | — | 1.65224 |
| 11.1886 | — | 1.61457 |
| 11.3696 | — | 1.58512 |
| 11.5535 | — | 1.5562 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.4×10-6 milligrams per kilogram
Источники (1)
- [5] Protactinium https://education.jlab.org/itselemental/ele091.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
5×10-11 milligrams per liter
Источники (1)
- [5] Protactinium https://education.jlab.org/itselemental/ele091.html
Sources
Sources of this element.
Protactinium is one of the rarest and most expensive naturally occurring elements. The average concentrations of protactinium in the Earth's crust is typically on the order of a few parts per trillion, but may reach up to a few parts per million in some uraninite ore deposits. The element occurs in pitchblende to the extent of about 1 part 231Pa to 10 million parts of ore. Ores from Zaire have about 3 ppm. In 1959 and 1961, it was announced that the Great Britain Atomic Energy Authority extracted by a 12-stage process 125 g of 99.9% protactinium, the world's only stock of the metal for many years following. The extraction was made from 60 tons of waste material at a cost of about $500,000.
Источники (1)
- [6] Protactinium https://periodic.lanl.gov/91.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Protactinium.
The element property data was retrieved from publications.