Уран (U)
АктиноидТвёрдое тело
Стандартный атомный вес
238.02891 uЭлектронная конфигурация
[Rn] 7s2 5f3 6d1Температура плавления
1134.85 °C (1408 K)Температура кипения
4130.85 °C (4404 K)Плотность
1.895000e+4 kg/m³Степени окисления
−1, +1, +2, +3, +4, +5, +6Электроотрицательность (Полинг)
1.38Энергия ионизации (1-я)
Год открытия
1789Атомный радиус
175 pmДополнительно
Уран — это плотный металл-актиноид и самый тяжёлый элемент, встречающийся на Земле в существенном природном количестве. Природный уран в основном представлен ²³⁸U, при меньшем содержании делящегося ²³⁵U и следовых количествах ²³⁴U. Его химия сильно оксофильна и обычно включает уранильный ион UO₂²⁺. Уран имеет важное технологическое значение как ядерное топливо и исторически важен для открытия и развития радиоактивности и ядерного деления.
Чистый уран — серебристо-белый слаборадиоактивный металл, более твердый, чем большинство элементов. Он ковкий, пластичный, слабо парамагнитный, сильно электроотрицательный и является плохим проводником электричества. Металлический уран имеет очень высокую плотность, примерно на 70% большую, чем у свинца, но немного меньшую, чем у золота. Металлический уран существует в трех кристаллографических модификациях: alpha > (688°C) > beta > (776°C) > gamma. Уран пирофорен в мелкоизмельченном состоянии. Он немного мягче стали и в мелкодисперсном состоянии разлагается холодной водой. На воздухе металлический уран покрывается слоем оксида. Кислоты растворяют металл, образуя состояние окисления +3, которое быстро окисляется водой и воздухом с образованием более высоких степеней окисления. Металлический уран не подвержен действию щелочей. Металлический уран может быть получен восстановлением галогенидов урана щелочными или щелочноземельными металлами либо восстановлением оксидов урана кальцием, алюминием или углеродом при высоких температурах. Металл также может быть получен электролизом KUF5 или UF4, растворенных в расплавленной солевой смеси CaCl2 и NaCl. Высокочистый уран может быть получен термическим разложением галогенидов урана на раскаленной нити.
Металлический уран реагирует почти со всеми неметаллическими элементами и их соединениями, причем реакционная способность возрастает с температурой. Соляная и азотная кислоты растворяют уран, но неокисляющие кислоты, кроме соляной кислоты, очень медленно воздействуют на элемент. В мелкодисперсном состоянии он может реагировать с холодной водой. На воздухе металлический уран окисляется и покрывается темным слоем оксида урана. Уран образует разнообразные сплавы и соединения, при этом наиболее важными состояниями окисления являются уран(IV) и уран(VI), а соответствующие им два оксида — это соответственно диоксид урана, UO2, и триоксид урана, UO3. Помимо оксидов, другие важные соединения урана включают фториды, хлориды, бромиды, иодиды, карбонаты, гидриды, карбиды, нитриды, фосфаты и т. д. При комнатной температуре гексафторид урана UF6 имеет высокое давление пара, что делает его полезным в процессе газовой диффузии, используемом для разделения редкого изотопа U-235 от распространенного изотопа U-238. Гидриды, нитриды и карбиды урана представляют собой относительно инертные полуметаллические соединения, слабо растворимые в кислотах, и использовались в качестве стабильных топливных таблеток в технологии ядерных энергетических реакторов.
Уран существует в водных растворах в степенях окисления +3, +4, +5 и +6. Степень окисления +6 в виде иона UO22+ (желтого цвета) является наиболее стабильной в растворе. Уран в степени +5 в виде иона UO2+ бесцветен, весьма нестабилен и диспропорционирует (реагирует сам с собой) с образованием состояний +6 и +4. Состояние +4 (зеленое) в растворе достаточно стабильно, однако состояние +3 (темно-зеленое или темно-красное в зависимости от источника освещения — дневной свет или флуоресцентный свет) нестабильно и легко окисляется до +4. Состояние +4 в растворах с близким к нейтральному pH легко гидролизуется с образованием черных оксогидроксидных осадков.
Название происходит от планеты Уран, которая в римской мифологии была «Отцом Небом». Немецкий химик Мартин-Генрих Клапрот открыл элемент в 1789 году, после открытия планеты Уильямом Гершелем в 1781 году. Металлический уран был впервые выделен французским химиком Эженом-Мельхиором Пелиго в 1841 году.
Уран был открыт Мартином Генрихом Клапротом, немецким химиком, в минерале смолистая обманка (преимущественно смесь оксидов урана) в 1789 году. Хотя Клапрот, как и вся научная общественность, считал, что вещество, извлечённое им из смолистой обманки, является чистым ураном, на самом деле это был диоксид урана (UO2). После того как было замечено, что «чистый» уран странно реагирует с тетрахлоридом урана (UCl4), французский химик Эжен-Мельхуа́р Пелиго выделил чистый уран, нагревая диоксид урана с калием в платиновом тигле. Радиоактивность была впервые обнаружена в 1896 году, когда Антуан Анри Беккерель, французский физик, обнаружил её в образце урана. В настоящее время уран получают из урановых руд, таких как смолистая обманка, уранинит (UO2), карнотит (K2(UO2)2VO4·1-3H2O) и автунит (Ca(UO2)2(PO4)2·10H2O), а также из фосфоритной породы (Ca3(PO4)2), лигнита (бурого угля) и монацитового песка ((Ce, La, Th, Nd, Y)PO4). Поскольку спрос на металлический уран невелик, уран обычно продают в виде уранилдинатрия (Na2U2O7·6H2O), также известного как yellow cake, или триоксида урана (U3O8).
Использование урана в его природной оксидной форме восходит к 79 году н. э., когда он применялся как жёлтый красящий агент в керамических глазурях. Жёлтое стекло с 1 % оксида урана было обнаружено в древнеримской вилле близ Неаполя, Италия. В позднем Средневековье смолистую обманку добывали на серебряных рудниках и использовали как красящий агент в стекольной промышленности. Идентификация урана как элемента обычно приписывается Мартину Г. Клапроту. В ходе экспериментов со смолистой обманкой в 1789 году он пришёл к выводу, что она содержит новый элемент, который он назвал в честь недавно открытой планеты Уран (названной в честь греческого бога неба). На самом деле Клапрот идентифицировал не чистый элемент, а оксид урана. Чистый металл был впервые выделен в 1841 году Эженом-Мельхиором Пелиго, который восстановил безводный тетрахлорид урана металлическим калием.
В 1896 году Антуан А. Беккерель обнаружил, что уран испускает невидимый свет или лучи; это была радиоактивность. В 1934 году исследования Энрико Ферми и других в конечном итоге привели к использованию деления урана в первой ядерной бомбе, применённой в войне, а позднее — к мирному использованию урана как топлива в атомной энергетике. Последовавшая гонка вооружений в период холодной войны между Соединёнными Штатами и Советским Союзом привела к созданию десятков тысяч ядерных боеприпасов, использовавших металлический уран и плутоний-239, полученный из урана. Безопасность этих вооружений и их делящегося материала после распада Советского Союза в 1991 году остаётся актуальной проблемой.
В 1972 году французский физик Франсис Перрен обнаружил древние и уже неактивные доисторические природные ядерные реакторы деления в залежах урановой руды на руднике Окло в Габоне, Западная Африка, вместе известные как ископаемые реакторы Окло. Месторождению руды 1,7 миллиарда лет; в то время уран-235 составлял около 3 % от общего количества урана на Земле (0,72 % сегодня). Этого достаточно для возникновения устойчивой цепной реакции ядерного деления при наличии других необходимых геологических условий.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
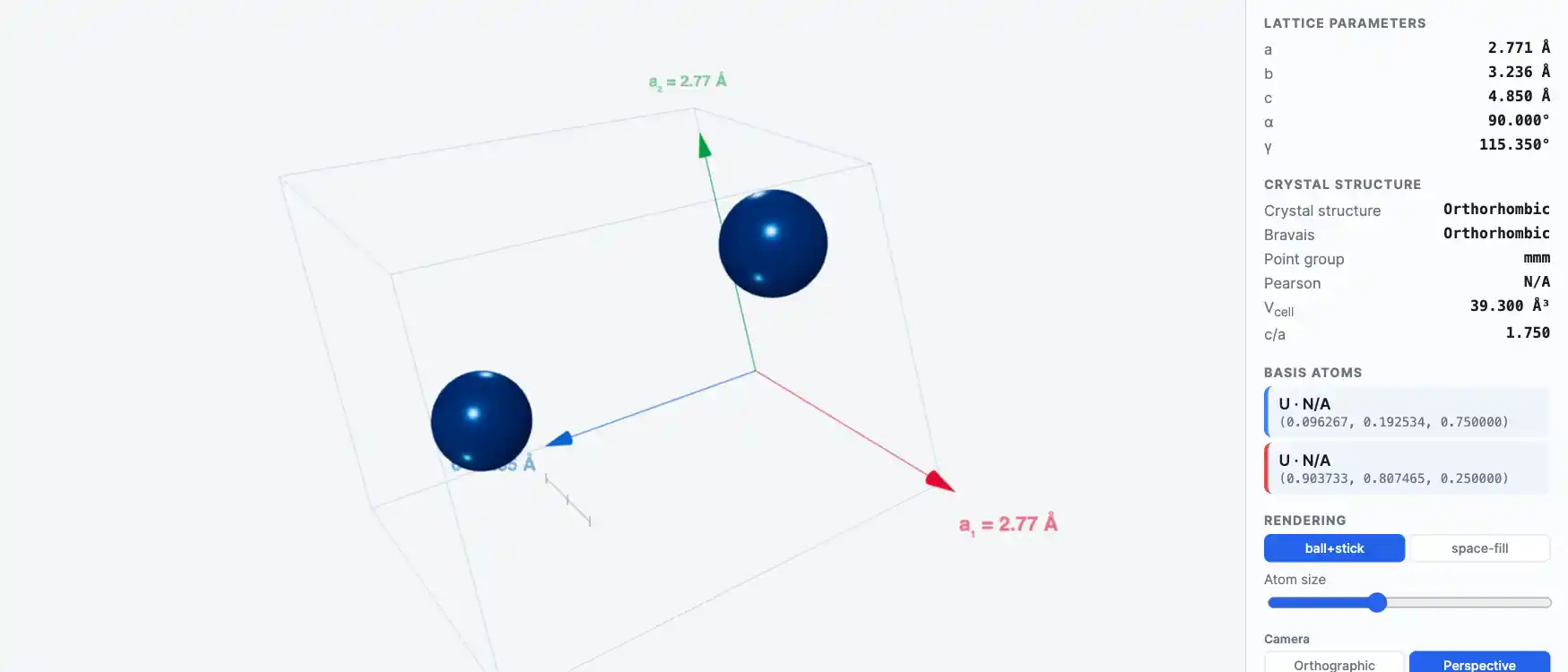
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
U: 5f³ 6d¹ 7s²[Rn] 5f³ 6d¹ 7s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹⁰ 6s² 6p⁶ 5f³ 6d¹ 7s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
Нет стабильных изотопов.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 217 Радиоактивный | 217,02466 ± 0,00011 | N/A | 850 us |
| 235 Радиоактивный | 235,0439301 ± 0,0000019 | 0.7204% | 704 My |
| 221 Радиоактивный | 221,02628 ± 0,00011 | N/A | 660 ns |
| 224 Радиоактивный | 224,027605 ± 0,000027 | N/A | 396 us |
| 218 Радиоактивный | 218,023523 ± 0,00002 | N/A | 354 us |
Фазовое состояние
Причина: на 1109.8 °C ниже точки плавления (1134.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 92 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| U I | 0 | 216 | 57 | 0 |
| U II | +1 | 258 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| U I | 0 | 2 |
| U II | +1 | 2 |
| U III | +2 | 2 |
| U IV | +3 | 2 |
| U V | +4 | 2 |
| U VI | +5 | 2 |
| U VII | +6 | 2 |
| U VIII | +7 | 2 |
| U IX | +8 | 2 |
| U X | +9 | 2 |
Ионные радиусы
Показано 10 из 14 Ионные радиусы.
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 102.49999999999999 пм |
| +3 | 9 | N/A | 118.9 пм |
| +4 | 6 | N/A | 89 пм |
| +4 | 7 | N/A | 95 пм |
| +4 | 8 | N/A | 100 пм |
| +4 | 9 | N/A | 105 пм |
| +4 | 12 | N/A | 117 пм |
| +5 | 6 | N/A | 76 пм |
| +5 | 7 | N/A | 84 пм |
| +6 | 2 | N/A | 45 пм |
Соединения
Изотопы (5)
Uranium is weakly radioactive because all naturally occurring (or primordial) isotopes of uranium (238U, 235U and 234U) are unstable, with half-lives varying between 159,200 years and 4.5 billion years. There are 27 known isotopes of uranium ranging in atomic weights 217–219, 222–240 and 242, with half-lives of from billions of years to a few nanoseconds. Naturally occurring uranium consists of three major isotopes: 238U (99.28% abundance), 235U (0.71%), and 234U (0.0054%). (The US DOE has adopted the value of 0.711 as being their official percentage of 235U in natural uranium.) All three isotopes are radioactive, with small probabilities of undergoing spontaneous fission but preferentially decaying by alpha emission. The half-life of uranium-238 is about 4.47 billion years and that of uranium-235 is 704 million years, making them useful in dating the age of the Earth. It also suggests that half of the uranium that existed from the formation of the Earth has decayed to other radioactive elements and eventually to stable elements. Much of the internal heat of the earth is thought to be attributable to the decay of uranium and thorium radio-isotopes.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 217 Радиоактивный | 217,02466 ± 0,00011 | N/A | 850 us | α ≈100%β- ? | |
| 235 Радиоактивный | 235,0439301 ± 0,0000019 | 0.7204% ± 0.0006% | 704 My | IS =0.7204±0.6%α =100%SF =7e-9±0.2% | |
| 221 Радиоактивный | 221,02628 ± 0,00011 | N/A | 660 ns | α ≈100%β+ ? | |
| 224 Радиоактивный | 224,027605 ± 0,000027 | N/A | 396 us | α =100%β+ ? | |
| 218 Радиоактивный | 218,023523 ± 0,00002 | N/A | 354 us | α =100% |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1408.15 K |
| Температура кипения | 4404.15 K |
Категории степеней окисления
Расширенные справочные данные
Детализация кристаллических радиусов (14)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 116.5 | from r^3 vs V plots, | |
| 4 | VI | 103 | ||
| 4 | VII | 109 | estimated, | |
| 4 | VIII | 114 | from r^3 vs V plots, | |
| 4 | IX | 119 | ||
| 4 | XII | 131 | estimated, | |
| 5 | VI | 90 | ||
| 5 | VII | 98 | estimated, | |
| 6 | II | 59 | ||
| 6 | IV | 66 |
Режимы распада изотопов (60)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 215 | A | — |
| 215 | B+ | — |
| 216 | A | 100% |
| 217 | A | 100% |
| 217 | B- | — |
| 218 | A | 100% |
| 219 | A | 100% |
| 219 | B+ | — |
| 220 | A | — |
| 220 | B+ | — |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.627 |
| 10.1617 | — | 1.61282 |
| 10.3261 | — | 1.59877 |
| 10.4931 | — | 1.58416 |
| 10.6628 | — | 1.56547 |
| 10.8353 | — | 1.547 |
| 11.0106 | — | 1.52874 |
| 11.1886 | — | 1.5107 |
| 11.3696 | — | 1.49287 |
| 11.5535 | — | 1.47526 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.7 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
3.2×10-3 milligrams per liter
Источники (1)
Sources
Sources of this element.
Uranium is the heaviest naturally-occurring element available in large quantities. The heavier “transuranic” elements are either man-made or they exist only as trace quantities in uranium ore deposits as activation products. Uranium occurs naturally in low concentrations of a few parts per million in soil, rock and water, and is commercially extracted from uranium-bearing minerals. Uranium, not as rare as once thought, is now considered to be more plentiful than mercury, antimony, silver, or cadmium, and is about as abundant as molybdenum or arsenic. It occurs in numerous natural minerals such as pitchblende, uraninite, carnotite, autunite, uranophane, and tobernite. It is also found in phosphate rocks, lignite, monazite sands, and is recovered commercially from these sources. The United States Department of Energy purchases uranium in the form of acceptable U3O8 concentrates. This incentive program has greatly increased the known uranium reserves.
Источники (1)
- [6] Uranium https://periodic.lanl.gov/92.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Uranium.
The element property data was retrieved from publications.