Торий (Th)
АктиноидТвёрдое тело
Стандартный атомный вес
232.0377 uЭлектронная конфигурация
[Rn] 7s2 6d2Температура плавления
1749.85 °C (2023 K)Температура кипения
4787.85 °C (5061 K)Плотность
1.172000e+4 kg/m³Степени окисления
−1, +1, +2, +3, +4Электроотрицательность (Полинг)
1.3Энергия ионизации (1-я)
Год открытия
1828Атомный радиус
180 pmДополнительно
Торий — это природно встречающийся металл-актиноид с атомным номером 90. Он слабо радиоактивен и встречается главным образом в виде ²³²Th, изотопа с очень большим периодом полураспада. Химически для него доминирует степень окисления +4, и он часто больше напоминает четырёхвалентные лантаноиды, чем уран или плутоний. Его основной технологический интерес связан с тем, что он является фертильным ядерным материалом, который в реакторах может быть превращён в делящийся ²³³U.
В чистом виде торий — серебристо-белый металл, устойчивый на воздухе и сохраняющий свой блеск в течение нескольких месяцев. При загрязнении оксидом торий на воздухе медленно тускнеет, становясь серым и в конце концов чёрным. Физические свойства тория в значительной степени зависят от степени загрязнения оксидом. В наиболее чистых образцах часто содержится несколько десятых процента оксида. Был получен высокочистый торий. Чистый торий мягкий, очень ковкий и может подвергаться холодной прокатке, обжатию и вытягиванию. Торий диморфен, при 1400°C переходя из кубической в объёмно-центрированную кубическую структуру. Оксид тория имеет температуру плавления 3300°C, что является наивысшим значением среди всех оксидов. Лишь немногие элементы, такие как вольфрам, и некоторые соединения, такие как карбид тантала, имеют более высокие температуры плавления. Торий медленно разрушается водой, но не растворяется легко в большинстве обычных кислот, за исключением соляной. Порошкообразный металлический торий часто пирофорен и должен обращаться с осторожностью. При нагревании на воздухе стружка тория воспламеняется и горит ярким белым пламенем.
Название происходит от Тора, скандинавского бога грома. Он был открыт в минерале торите (ThSiO4) шведским химиком Йёнсом Якобом Берцелиусом в 1828 году. Торий был впервые выделен химиками Д. Лели-младшим и Л. Гамбургером в 1914 году.
Торий был открыт Йёнсом Якобом Берцелиусом, шведским химиком, в 1828 году. Он обнаружил его в образце минерала, который был передан ему преподобным Хасом Мортеном Тране Эсмарком, подозревавшим, что он содержит неизвестное вещество. Минерал Эсмарка в настоящее время известен как торит (ThSiO4). Торий составляет около 0.0007% земной коры и в основном получают из торита, торианита (ThO2) и монацита ((Ce, La, Th, Nd, Y)PO4).
Мортен Эсмарк нашёл чёрный минерал на острове Лёвёя, Норвегия, и передал образец своему отцу Йенсу Эсмарку, известному минералогу. Старший Эсмарк не смог его идентифицировать и отправил образец шведскому химику Йёнсу Якобу Берцелиусу для исследования в 1828 году. В 1829 году Берцелиус установил, что он содержит новый элемент, который он назвал торием в честь Тора, скандинавского бога грома. Металл не имел практического применения до 1885 года, когда Карл Ауэр фон Вельсбах изобрёл газовую мантиию. Впервые радиоактивность тория была независимо обнаружена в 1898 году польско-французским физиком Марией Кюри и немецким химиком Герхардом Карлом Шмидтом. В период с 1900 по 1903 год Эрнест Резерфорд и Фредерик Содди показали, как торий с постоянной скоростью распадается во времени на ряд других элементов. Это наблюдение привело к установлению периода полураспада как одного из результатов экспериментов с альфа-частицами, которые привели к их теории распада радиоактивности. Процесс получения кристаллического прутка (или «йодидный процесс») был открыт Антоном Эдуардом ван Аркелем и Яном Хендриком де Бором в 1925 году для получения высокочистого металлического тория. Из-за опасений для здоровья торий в классических ламповых мантиях был заменён редкоземельными элементами, которые также дают интенсивный свет без радиоактивности.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
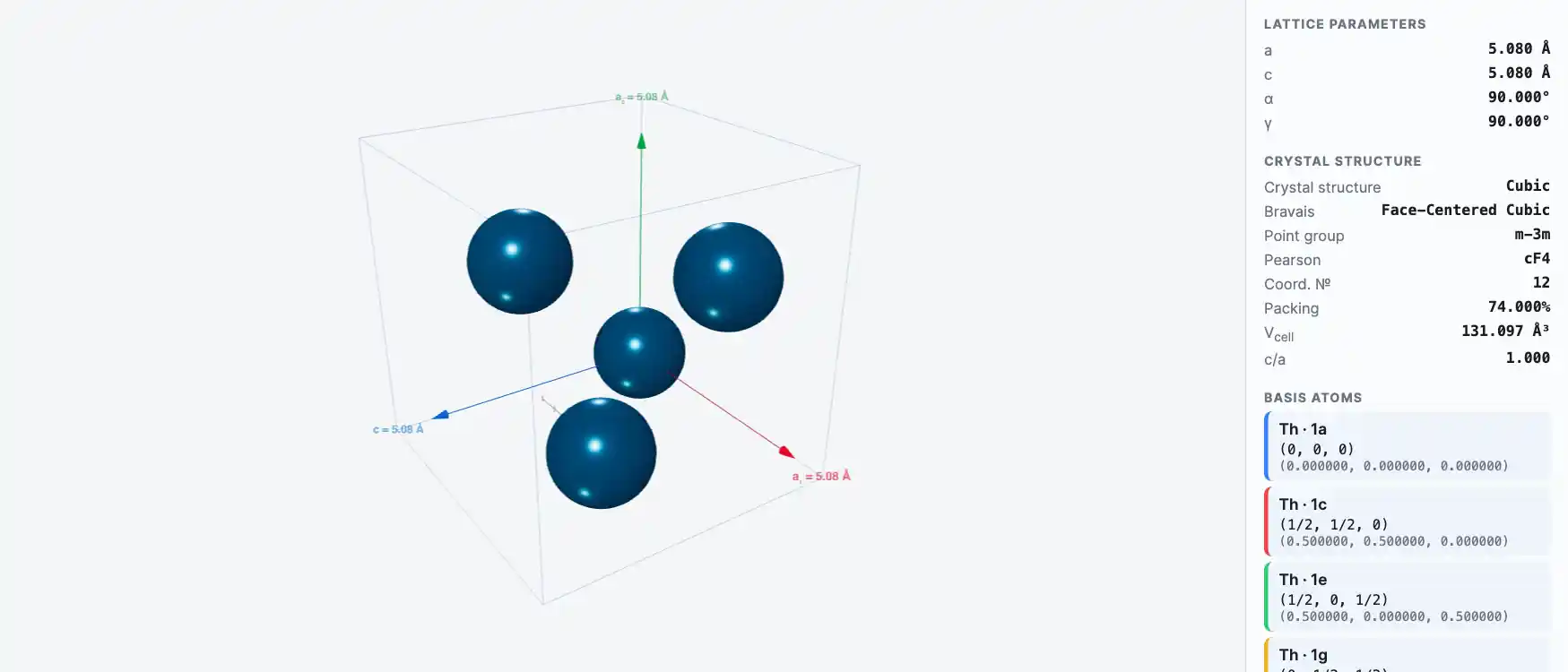
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Th: 6d² 7s²[Rn] 6d² 7s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹⁰ 6s² 6p⁶ 6d² 7s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
Нет стабильных изотопов.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 223 Радиоактивный | 223,0208119 ± 0,0000099 | N/A | 600 мс |
| 217 Радиоактивный | 217,013117 ± 0,000022 | N/A | 248 us |
| 213 Радиоактивный | 213,013009 ± 0,000076 | N/A | 144 мс |
| 218 Радиоактивный | 218,013276 ± 0,000011 | N/A | 122 ns |
| 214 Радиоактивный | 214,0115 ± 0,000017 | N/A | 87 мс |
Фазовое состояние
Причина: на 1724.8 °C ниже точки плавления (1749.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 90 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Th I | 0 | 13387 | 0 | 13387 |
| Th II | +1 | 6502 | 0 | 6502 |
| Th III | +2 | 227 | 0 | 227 |
| Th IV | +3 | 27 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Th I | 0 | 788 |
| Th II | +1 | 517 |
| Th III | +2 | 176 |
| Th IV | +3 | 2 |
| Th V | +4 | 2 |
| Th VI | +5 | 2 |
| Th VII | +6 | 2 |
| Th VIII | +7 | 2 |
| Th IX | +8 | 2 |
| Th X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 9 | N/A | 120.9 пм |
| +4 | 6 | N/A | 94 пм |
| +4 | 8 | N/A | 105 пм |
| +4 | 9 | N/A | 109.00000000000001 пм |
| +4 | 10 | N/A | 112.99999999999999 пм |
| +4 | 11 | N/A | 118 пм |
| +4 | 12 | N/A | 121 пм |
Соединения
Изотопы (5)
Twenty-seven thorium radioisotopes have been characterized, with a range in atomic weight from 210 to 236. All are unstable with the most stable being 232Th with a half-life of 14.05 billion years. Thorium-232 represents all but a trace of naturally occurring thorium. It is an alpha emitter and goes through six alpha and four beta decay steps before becoming the stable isotope 208Pb. 232Th is sufficiently radioactive to expose a photographic plate in a few hours. Other isotopes of thorium are short-lived intermediates in the decay chains of higher elements, and only found in trace amounts. The longer-lived of these trace isotopes include: 230Th with a half-life of 75,380 years which is a daughter product of 238U decay; 229Th with a half-life of 7340 years and 228Th with a half-life of 1.92 years. All of the remaining radioactive isotopes have half-lives that are less than thirty days and the majority of these have half-lives less than ten minutes. Much of the internal heat the earth produces has been attributed to thorium and uranium.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 223 Радиоактивный | 223,0208119 ± 0,0000099 | N/A | 600 мс | α =100% | |
| 217 Радиоактивный | 217,013117 ± 0,000022 | N/A | 248 us | α =100% | |
| 213 Радиоактивный | 213,013009 ± 0,000076 | N/A | 144 мс | α ≈100%β+ ? | |
| 218 Радиоактивный | 218,013276 ± 0,000011 | N/A | 122 ns | α =100% | |
| 214 Радиоактивный | 214,0115 ± 0,000017 | N/A | 87 мс | α ≈100%β+ ? |
Спектральные линии
Показано 50 из 9955 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 576.055056 нм | 53000 | Th I | emission | 6d2.7s2 3F → 5f.6d.7s2 3D* | Измерено | NIST | |
| 645.728238 нм | 44000 | Th I | emission | 5f.6d.7s2 3H* → 5f.6d.7s.7p 5I | Измерено | NIST | |
| 395.039509 нм | 42000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 618.262159 нм | 38000 | Th I | emission | 6d2.7s2 3F → 6d.7s2.7p 3P* | Измерено | NIST | |
| 658.390575 нм | 32000 | Th I | emission | 6d2.7s2 3F → 6d.7s2.7p 3F* | Измерено | NIST | |
| 572.018265 нм | 31000 | Th I | emission | 6d2.7s2 → 5f.6d.7s2 3D* | Измерено | NIST | |
| 698.965521 нм | 31000 | Th I | emission | 5f.6d.7s2 3H* → 5f.6d.7s.7p 5I | Измерено | NIST | |
| 716.889496 нм | 30000 | Th I | emission | 6d2.7s2 3F → 6d.7s2.7p 3F* | Измерено | NIST | |
| 449.3333668 нм | 28000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 658.853947 нм | 26000 | Th I | emission | 6d2.7s2 3P → 6d.7s2.7p 3P* | Измерено | NIST | |
| 691.12262 нм | 25000 | Th I | emission | 6d2.7s2 3F → 6d2.7s.7p 5G* | Измерено | NIST | |
| 380.307494 нм | 24000 | Th I | emission | 6d2.7s2 3F → 6d2.7s.7p 3D* | Измерено | NIST | |
| 403.6047645 нм | 24000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 659.148431 нм | 21000 | Th I | emission | 6d2.7s2 3F → 6d2.7s.7p 5G* | Измерено | NIST | |
| 401.912876 нм | 20000 | Th II | emission | 6d.7s2 2D → 6d.7s.(3D).7p * | Измерено | NIST | |
| 558.702644 нм | 20000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 411.2754309 нм | 18000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 470.398977 нм | 18000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 580.414105 нм | 18000 | Th I | emission | 6d2.7s2 3F → 6d2.7s.7p 5F* | Измерено | NIST | |
| 616.982198 нм | 18000 | Th I | emission | 6d2.7s2 3F → 5f.6d.7s2 3D* | Измерено | NIST | |
| 597.366467 нм | 17000 | Th I | emission | 6d2.7s2 → 6d.7s2.7p 3P* | Измерено | NIST | |
| 653.134169 нм | 17000 | Th I | emission | 6d3.(4F).7s 5F → 6d2.7s.7p 5P* | Измерено | NIST | |
| 383.969505 нм | 16000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 421.092303 нм | 16000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 515.86042 нм | 16000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 620.349239 нм | 16000 | Th I | emission | 6d2.7s2 3F → 6d2.7s.7p 5F* | Измерено | NIST | |
| 666.22685 нм | 16000 | Th I | emission | 6d3.(4F).7s 5F → 6d2.7s.7p 5P* | Измерено | NIST | |
| 394.8030341 нм | 15000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 403.0842224 нм | 15000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 410.0341193 нм | 15000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 467.366094 нм | 15000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 506.797381 нм | 15000 | Th I | emission | 5f.6d.7s2 3H* | Измерено | NIST | |
| 523.115956 нм | 15000 | Th I | emission | 6d2.7s2 3P → 6d2.7s.7p 5P* | Измерено | NIST | |
| 634.285945 нм | 15000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 382.838452 нм | 14000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 472.3438197 нм | 14000 | Th I | emission | 6d2.7s2 3F → 5f.6d.7s2 3D* | Измерено | NIST | |
| 553.926178 нм | 14000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 694.361046 нм | 14000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 720.80062 нм | 14000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 425.0314489 нм | 13000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 489.495493 нм | 13000 | Th I | emission | 6d2.7s2 3F → 6d.7s2.7p 3P* | Измерено | NIST | |
| 387.382217 нм | 12000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 423.5463454 нм | 12000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 480.81337 нм | 12000 | Th I | emission | 6d2.7s2 3F → * | Измерено | NIST | |
| 541.748576 нм | 12000 | Th I | emission | 6d2.7s2 → * | Измерено | NIST | |
| 599.412865 нм | 12000 | Th I | emission | 6d2.7s2 3P → 6d.7s2.7p 3P* | Измерено | NIST | |
| 659.393903 нм | 12000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 708.416896 нм | 12000 | Th I | emission | 6d3.(4F).7s 5F → * | Измерено | NIST | |
| 738.550045 нм | 12000 | Th I | emission | 6d2.7s2 → 6d2.7s.7p 5F* | Измерено | NIST | |
| 392.440084 нм | 11000 | Th I | emission | 6d2.7s2 → * | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 2023.15 K |
| Температура кипения | 5058.15 K |
Категории степеней окисления
Расширенные справочные данные
Детализация кристаллических радиусов (7)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 4 | VI | 108 | calculated, | |
| 4 | VIII | 119 | from r^3 vs V plots, calculated, | |
| 4 | IX | 123 | ||
| 4 | X | 127 | estimated, | |
| 4 | XI | 132 | calculated, | |
| 4 | XII | 135 | calculated, | |
| 3 | IX | — | 134.9 |
Режимы распада изотопов (52)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 208 | A | 100% |
| 209 | A | — |
| 209 | B+ | — |
| 210 | A | 100% |
| 210 | B+ | — |
| 211 | A | 100% |
| 211 | B+ | — |
| 212 | A | 100% |
| 212 | B+ | — |
| 213 | A | 100% |
Факторы рассеяния X‑лучей (516)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 3.14769 |
| 10.1617 | — | 3.1007 |
| 10.3261 | — | 3.05442 |
| 10.4931 | — | 3.00883 |
| 10.6628 | — | 2.96392 |
| 10.8353 | — | 2.91968 |
| 11.0106 | — | 2.87611 |
| 11.1886 | — | 2.83318 |
| 11.3696 | — | 2.79089 |
| 11.5535 | — | 2.74024 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
9.6 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1×10-6 milligrams per liter
Источники (1)
Sources
Sources of this element.
Thorium-232 is a primordial nuclide, having existed in its current form for over 4.5 billion years, a half-life is comparable to the age of the Universe and thus predating the formation of the Earth. Thorium was forged in the cores of dying stars through the r-process and scattered across the galaxy by supernovas. Thorium is found in small amounts in most rocks and soils. Soil commonly contains an average of around 6 parts per million (ppm) of thorium. Thorium occurs in several minerals including thorite (ThSiO4), thorianite (ThO2 + UO2) and monazite. Thorianite is a rare mineral and may contain up to about 12% thorium oxide. Monazite contains 2.5% thorium, allanite has 0.1 to 2% thorium and zircon can have up to 0.4% thorium.[66] Thorium-containing minerals occur on all continents. Thorium is now thought to be about three times as abundant as uranium and about as abundant as lead or molybdenum. Thorium is recovered commercially from the mineral monazite, which contains from 3 to 9% ThO2 along with rare-earth minerals.
Источники (1)
- [6] Thorium https://periodic.lanl.gov/90.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
Production
Several methods are available for producing thorium metal; it can be obtained by reducing thorium oxide with calcium, by electrolysis of anhydrous thorium chloride in a fused mixture of sodium and potassium chlorides, by calcium reduction of thorium tetrachloride mixed with anhydrous zinc chloride, and by reduction of thorium tetrachloride with an alkali metal.
Источники (1)
- [6] Thorium https://periodic.lanl.gov/90.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Thorium.
The element property data was retrieved from publications.