Тантал (Ta)
Переходный металлТвёрдое тело
Стандартный атомный вес
180.94788 uЭлектронная конфигурация
[Xe] 6s2 4f14 5d3Температура плавления
3016.85 °C (3290 K)Температура кипения
5457.85 °C (5731 K)Плотность
1.640000e+4 kg/m³Степени окисления
−3, −1, 0, +1, +2, +3, +4, +5Электроотрицательность (Полинг)
1.5Энергия ионизации (1-я)
Год открытия
1802Атомный радиус
145 pmДополнительно
Тантал — это плотный, тугоплавкий переходный металл группы 5, тесно связанный геологически и химически с ниобием. Он известен исключительной стойкостью к коррозии, очень высокой температурой плавления и устойчивой оксидной плёнкой с высокой диэлектрической проницаемостью, образующейся на его поверхности. Большая часть природного тантала представлена ¹⁸¹Ta, с небольшим вкладом долгоживущего ядерного изомера ¹⁸⁰ᵐTa. Его химия определяется степенью окисления +5.
Тантал — серый, тяжёлый и очень твёрдый металл. В чистом виде он ковкий и может быть вытянут в тонкую проволоку, которая используется в качестве нити для испарения металлов, таких как алюминий. Тантал почти полностью устойчив к химическому воздействию при температурах ниже 150°C и разрушается только плавиковой кислотой, кислые растворы, содержащие ион фторида, и свободный триоксид серы. Щёлочи действуют на него лишь медленно. При высоких температурах тантал становится значительно более реакционноспособным. Температура плавления этого элемента превышается только вольфрамом и рением. Тантал используют для получения различных сплавов с желательными свойствами, такими как высокая температура плавления, высокая прочность, хорошая пластичность и т. д. Тантал обладает хорошей способностью к «геттерированию» при высоких температурах, а плёнки оксида тантала стабильны и обладают хорошими выпрямляющими и диэлектрическими свойствами.
Название происходит от греческого мифологического персонажа Тантала, который был низвергнут в Аид, область потерянных душ, где он стоял в воде по подбородок, но вода отступала, когда бы он ни пытался напиться, и под ветвями с плодами, которые отодвигались, когда бы он ни пытался сорвать их плоды. Это название было выбрано из-за нерастворимости тантала в кислотах; таким образом, помещенный среди кислот, он не способен вступать в какое-либо взаимодействие с ними. Тантал был открыт шведским химиком и минералогом Андерсом-Густавом Экебергом в 1802 году.
Тантал был открыт Андерсом Густавом Экенбергом, шведским химиком, в 1802 году в минералах, полученных из Иттербю, Швеция. Многие ученые считали, что он открыл лишь аллотроп ниобия, элемента, химически сходного с танталом. Вопрос окончательно был решен в 1866 году, когда швейцарский химик Жан Шарль Галиссар де Мариньяк доказал, что тантал и ниобий являются двумя различными элементами. Первые относительно чистые образцы тантала были получены в 1907 году. Сегодня тантал в основном получают из минералов колумбита ((Fe, Mn, Mg)(Nb, Ta)2O6), танталита ((Fe, Mn)(Ta, Nb)2O6) и эвксенита ((Y, Ca, Er, La, Ce, U, Th)(Nb, Ta, Ti)2O6).
Назван в честь Тантала, греческого мифологического персонажа, отца Ниобы. Открыт в 1802 году Экебергом, но многие химики считали ниобий и тантал идентичными элементами до тех пор, пока Роу в 1844 году и Мариньяк в 1866 году не показали, что ниобиевая и танталовая кислоты — это две разные кислоты. Ранние исследователи выделяли только нечистый металл. Первый относительно чистый пластичный тантал был получен фон Болтоном в 1903 году. Тантал главным образом встречается в минерале колумбит-танталит.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
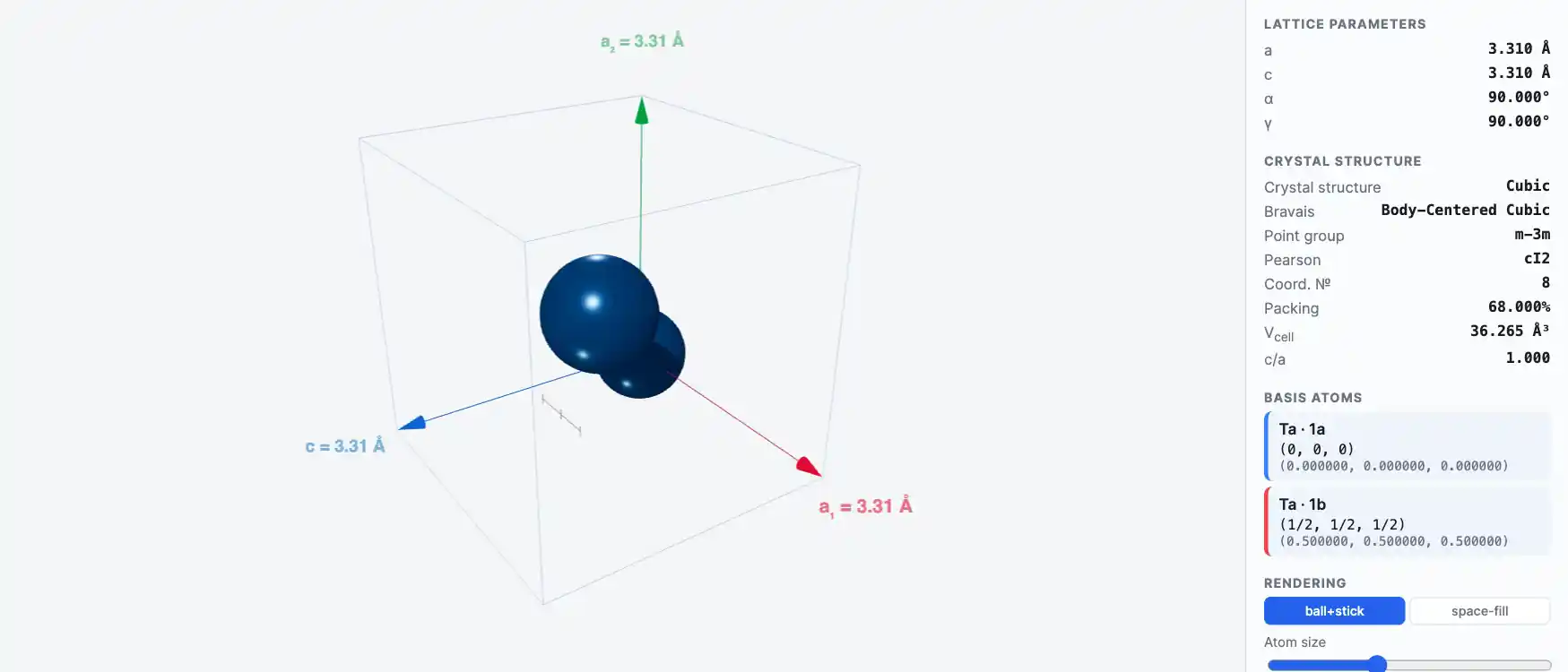
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Ta: 4f¹⁴ 5d³ 6s²[Xe] 4f¹⁴ 5d³ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d³ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 181 Стабильный | 180,9479958 ± 0,000002 | 99.9880% | Стабильный |
Фазовое состояние
Причина: на 2991.8 °C ниже точки плавления (3016.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 73 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Ta I | 0 | 526 | 200 | 510 |
| Ta II | +1 | 141 | 0 | 13 |
| Ta IV | +3 | 83 | 0 | 0 |
| Ta V | +4 | 12 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Ta I | 0 | 301 |
| Ta II | +1 | 134 |
| Ta III | +2 | 2 |
| Ta IV | +3 | 2 |
| Ta V | +4 | 2 |
| Ta VI | +5 | 2 |
| Ta VII | +6 | 2 |
| Ta VIII | +7 | 2 |
| Ta IX | +8 | 2 |
| Ta X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 72 пм |
| +4 | 6 | N/A | 68 пм |
| +5 | 6 | N/A | 64 пм |
| +5 | 7 | N/A | 69 пм |
| +5 | 8 | N/A | 74 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 181 Стабильный | 180,9479958 ± 0,000002 | 99.9880% ± 0.0003% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 3290.15 K |
| Температура кипения | 5728.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (14)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.4163 |
| 2 | p | 4.4136 |
| 2 | s | 19.0702 |
| 3 | d | 13.5589 |
| 3 | p | 21.1996 |
| 3 | s | 21.9085 |
| 4 | d | 36.676 |
| 4 | f | 39.5296 |
| 4 | p | 34.2652 |
| 4 | s | 33.2412 |
Детализация кристаллических радиусов (5)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 86 | estimated, | |
| 4 | VI | 82 | estimated, | |
| 5 | VI | 78 | ||
| 5 | VII | 83 | ||
| 5 | VIII | 88 |
Режимы распада изотопов (52)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 155 | p | 100% |
| 156 | p | 71% |
| 156 | B+ | 29% |
| 157 | A | 96.6% |
| 157 | p | 3.4% |
| 157 | B+ | — |
| 158 | A | 100% |
| 158 | B+ | — |
| 159 | B+ | 66% |
| 159 | A | 34% |
Факторы рассеяния X‑лучей (716)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 3.16064 |
| 10.1152 | — | 3.23709 |
| 10.2317 | — | 3.31539 |
| 10.3496 | — | 3.39558 |
| 10.4688 | — | 3.47772 |
| 10.5894 | — | 3.56683 |
| 10.7114 | — | 3.65875 |
| 10.8348 | — | 3.75304 |
| 10.9596 | — | 3.84976 |
| 11.0859 | — | 3.94897 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.0 milligrams per kilogram
Источники (1)
- [5] Tantalum https://education.jlab.org/itselemental/ele073.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
2×10-6 milligrams per liter
Источники (1)
- [5] Tantalum https://education.jlab.org/itselemental/ele073.html
Sources
Sources of this element.
Tantalum ores are found in Australia, Brazil, Mozambique, Thailand, Portugal, Nigeria, Zaire, and Canada.
Источники (1)
- [6] Tantalum https://periodic.lanl.gov/73.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
Separation of tantalum from niobium requires several complicated steps. Several methods are used to commercially produce the element, including electrolysis of molten potassium fluorotantalate, reduction of potassium fluorotantalate with sodium, or reacting tantalum carbide with tantalum oxide. Twenty five isotopes of tantalum are known to exist. Natural tantalum contains two isotopes.
Источники (1)
- [6] Tantalum https://periodic.lanl.gov/73.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Tantalum.
The element property data was retrieved from publications.