Диспрозий (Dy)
ЛантаноидТвёрдое тело
Стандартный атомный вес
162.5 uЭлектронная конфигурация
[Xe] 6s2 4f10Температура плавления
1411.85 °C (1685 K)Температура кипения
2566.85 °C (2840 K)Плотность
8550 kg/m³Степени окисления
0, +1, +2, +3, +4Электроотрицательность (Полинг)
1.22Энергия ионизации (1-я)
Год открытия
1878Атомный радиус
175 pmДополнительно
Диспрозий — тяжелый металл-лантаноид с атомным номером 66. В соединениях он почти исключительно трехвалентен, образуя бледные соли, химия которых напоминает химию соседних редкоземельных элементов. Его технологическое значение связано с необычно большим магнитным моментом и сильной магнитной анизотропией, особенно при включении в высокоэффективные постоянные магниты. Природный диспрозий представляет собой смесь стабильных изотопов и получают его вместе с другими редкоземельными элементами, а не как самородный металл.
Элемент имеет металлический, ярко-серебристый блеск. Он относительно стабилен на воздухе при комнатной температуре и легко разрушается и растворяется в разбавленных и концентрированных минеральных кислотах с выделением водорода. Металл достаточно мягок, чтобы его можно было резать ножом, и может подвергаться механической обработке без искрообразования, если избегать перегрева. Небольшие количества примесей могут сильно влиять на его физические свойства.
Название происходит от греческого dysprositos — «трудно добываемый», что связано с трудностью отделения этого редкоземельного элемента от минерала гольмия, в котором он был обнаружен. Он был открыт швейцарским химиком Марком Делафонтеном в минерале самарскит в 1878 году и назван philippia. Позднее считалось, что philippia представляет собой смесь тербия и иттрия. Впоследствии его заново обнаружил в образце гольмия французский химик Поль-Эмиль Лекок де Буабодран в 1886 году, которому тогда и приписали открытие. Диспрозий был впервые выделен французским химиком Жоржем Урбеном в 1906 году.
Диспрозий был открыт Полем-Эмилем Лекоком де Буабодраном, французским химиком, в 1886 году как примесь в эрбии, оксиде эрбия. Металл был выделен Жоржем Урбеном, другим французским химиком, в 1906 году. Чистые образцы диспрозия впервые были получены в 1950-х годах. В настоящее время диспрозий преимущественно получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами.
От греческого слова dysprositos, означающего трудно добываемый. Диспрозий был открыт в 1886 году Лекоком де Буабодраном, но не был выделен. Ни оксид, ни металл не были доступны в относительно чистой форме до 1950 года, когда были разработаны методы ионообменного разделения и металлографического восстановления, созданные Спеддингом и сотрудниками. Диспрозий встречается вместе с другими так называемыми редкоземельными или лантанидными элементами в ряде минералов, таких как ксенотим, фергюсонит, гадолинит, эвксенит, поликраз и бломстрандит. Однако наиболее важными источниками являются монацит и бастнезит. Диспрозий можно получить восстановлением трифторида кальцием.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
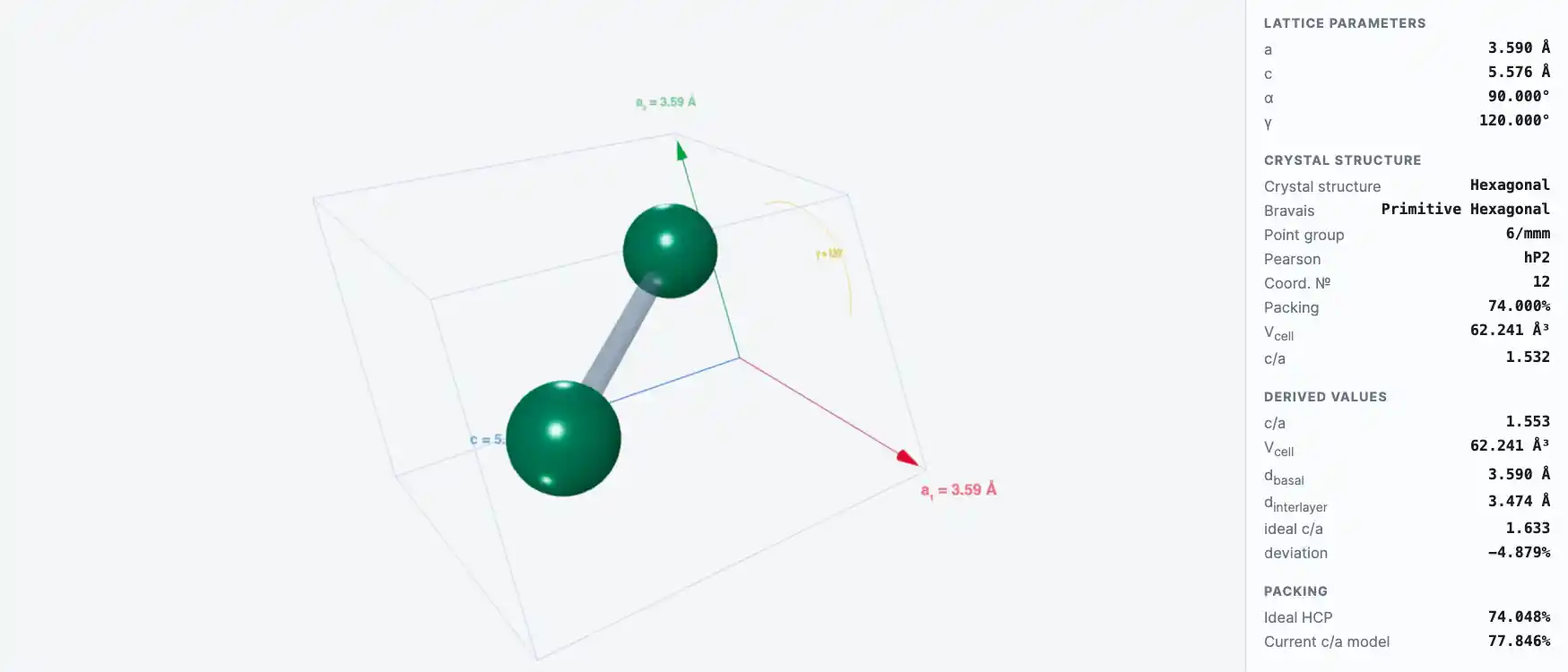
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Dy: 4f¹⁰ 6s²[Xe] 4f¹⁰ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁰ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 158 Стабильный | 157,9244159 ± 0,0000031 | 0.0950% | Стабильный |
| 160 Стабильный | 159,9252046 ± 0,000002 | 2.3290% | Стабильный |
| 161 Стабильный | 160,9269405 ± 0,000002 | 18.8890% | Стабильный |
| 162 Стабильный | 161,9268056 ± 0,000002 | 25.4750% | Стабильный |
| 163 Стабильный | 162,9287383 ± 0,000002 | 24.8960% | Стабильный |
| 164 Стабильный | 163,9291819 ± 0,000002 | 28.2600% | Стабильный |
Фазовое состояние
Причина: на 1386.8 °C ниже точки плавления (1411.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 66 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Dy I | 0 | 230 | 73 | 73 |
| Dy II | +1 | 421 | 17 | 17 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Dy I | 0 | 740 |
| Dy II | +1 | 576 |
| Dy III | +2 | 2 |
| Dy IV | +3 | 13 |
| Dy V | +4 | 2 |
| Dy VI | +5 | 2 |
| Dy VII | +6 | 2 |
| Dy VIII | +7 | 2 |
| Dy IX | +8 | 2 |
| Dy X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +2 | 6 | N/A | 107 пм |
| +2 | 7 | N/A | 112.99999999999999 пм |
| +2 | 8 | N/A | 119 пм |
| +3 | 6 | N/A | 91.2 пм |
| +3 | 7 | N/A | 97 пм |
| +3 | 8 | N/A | 102.69999999999999 пм |
| +3 | 9 | N/A | 108.3 пм |
Соединения
Изотопы (6)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 158 Стабильный | 157,9244159 ± 0,0000031 | 0.0950% ± 0.0030% | Стабильный | stable | |
| 160 Стабильный | 159,9252046 ± 0,000002 | 2.3290% ± 0.0180% | Стабильный | stable | |
| 161 Стабильный | 160,9269405 ± 0,000002 | 18.8890% ± 0.0420% | Стабильный | stable | |
| 162 Стабильный | 161,9268056 ± 0,000002 | 25.4750% ± 0.0360% | Стабильный | stable | |
| 163 Стабильный | 162,9287383 ± 0,000002 | 24.8960% ± 0.0420% | Стабильный | stable | |
| 164 Стабильный | 163,9291819 ± 0,000002 | 28.2600% ± 0.0540% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1685.15 K |
| Температура кипения | 2840.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.2914 |
| 2 | p | 4.3204 |
| 2 | s | 17.2906 |
| 3 | d | 13.6701 |
| 3 | p | 20.1195 |
| 3 | s | 20.6067 |
| 4 | d | 34.982 |
| 4 | f | 39.464 |
| 4 | p | 32.174 |
| 4 | s | 31.408 |
Детализация кристаллических радиусов (7)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 2 | VI | 121 | ||
| 2 | VII | 127 | ||
| 2 | VIII | 133 | ||
| 3 | VI | 105.2 | from r^3 vs V plots, | |
| 3 | VII | 111 | ||
| 3 | VIII | 116.7 | from r^3 vs V plots, | |
| 3 | IX | 122.3 | from r^3 vs V plots, |
Режимы распада изотопов (56)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 138 | B+ | — |
| 138 | B+p | — |
| 139 | B+ | 100% |
| 139 | B+p | 11% |
| 140 | B+ | — |
| 140 | B+p | — |
| 141 | B+ | 100% |
| 141 | B+p | — |
| 142 | B+ | 100% |
| 142 | e+ | 90% |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.15635 |
| 10.1617 | — | 0.1621 |
| 10.3261 | — | 0.16806 |
| 10.4931 | — | 0.17425 |
| 10.6628 | — | 0.18066 |
| 10.8353 | — | 0.18731 |
| 11.0106 | — | 0.19421 |
| 11.1886 | — | 0.20135 |
| 11.3696 | — | 0.20876 |
| 11.5535 | — | 0.21654 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
5.2 milligrams per kilogram
Источники (1)
- [5] Dysprosium https://education.jlab.org/itselemental/ele066.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
9.1×10-7 milligrams per liter
Источники (1)
- [5] Dysprosium https://education.jlab.org/itselemental/ele066.html
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Dysprosium.
The element property data was retrieved from publications.