Тербий (Tb)
ЛантаноидТвёрдое тело
Стандартный атомный вес
158.92535 uЭлектронная конфигурация
[Xe] 6s2 4f9Температура плавления
1355.85 °C (1629 K)Температура кипения
3229.85 °C (3503 K)Плотность
8230 kg/m³Степени окисления
0, +1, +2, +3, +4Электроотрицательность (Полинг)
N/AЭнергия ионизации (1-я)
Год открытия
1843Атомный радиус
175 pmДополнительно
Тербий — это редкоземельный металл-лантаноид с атомным номером 65. Он химически сходен с соседними гадолинием и диспрозием и встречается в минералах вместе с другими редкоземельными элементами, а не как самородный элемент. Его наиболее характерная технологическая роль связана с люминесценцией Tb³⁺, обеспечивающей интенсивное зелёное излучение в подходящих матричных материалах, а также с большим магнитострикционным откликом сплавов, содержащих тербий.
Тербий достаточно стабилен на воздухе. Это серебристо-серый металл, ковкий, пластичный и достаточно мягкий, чтобы его можно было резать ножом. Существуют две кристаллические модификации, с температурой превращения 1289°C. Признаны двадцать один изотоп с атомными массами от 145 до 165. Оксид имеет шоколадный или тёмно-бордовый цвет.
Название происходит от деревни Иттербю в Швеции, где впервые был найден минерал иттербит (источник тербия). Тербий был открыт шведским хирургом и химиком Карлом-Густавом Мосандером в 1843 году в соли иттрия, которую он разделил на три элемента. Один он назвал иттрием, розовую соль он назвал тербием, а тёмно-жёлтый пероксид он назвал эрбием. В 1862 году швейцарский химик Марк Делафонтен повторно исследовал иттрий и обнаружил жёлтый пероксид. Поскольку название «эрбий» к тому времени было присвоено розовому оксиду, он вновь ввёл название «тербий» для жёлтого пероксида. Таким образом, первоначальные названия образцов эрбия и тербия теперь поменялись местами.
Минерал гадолинит ((Ce, La, Nd, Y)2FeBe2Si2O10), обнаруженный в карьере близ города Иттербю, Швеция, был источником большого числа редкоземельных элементов. В 1843 году Карл Густав Мосандер, шведский химик, смог разделить гадолинит на три вещества, которые он назвал иттрией, эрбией и тербией. Как и следовало ожидать, учитывая сходство их названий и свойств, учёные вскоре перепутали эрбию и тербию и к 1877 году поменяли их названия местами. То, что Мосандер называл эрбией, теперь называется тербией и наоборот. Из этих двух веществ Мосандер открыл два новых элемента — тербий и эрбий. Сегодня тербий можно получать из минералов ксенотим (YPO4) и эвксенит ((Y, Ca, Er, La, Ce, U, Th)(Nb, Ta, Ti)2O6), однако в основном его получают посредством ионообменного процесса из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами, который обычно содержит до 0,03% тербия.
Открыт Мосандером в 1843 году. Тербий является членом группы лантаноидов, или «редкоземельных» элементов. Он встречается в церите, гадолините и других минералах вместе с другими редкоземельными элементами. Его промышленно извлекают из монацита, в котором его содержится 0,03%, из ксенотима и из эвксенита — сложного оксида, содержащего 1% или более тербии.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
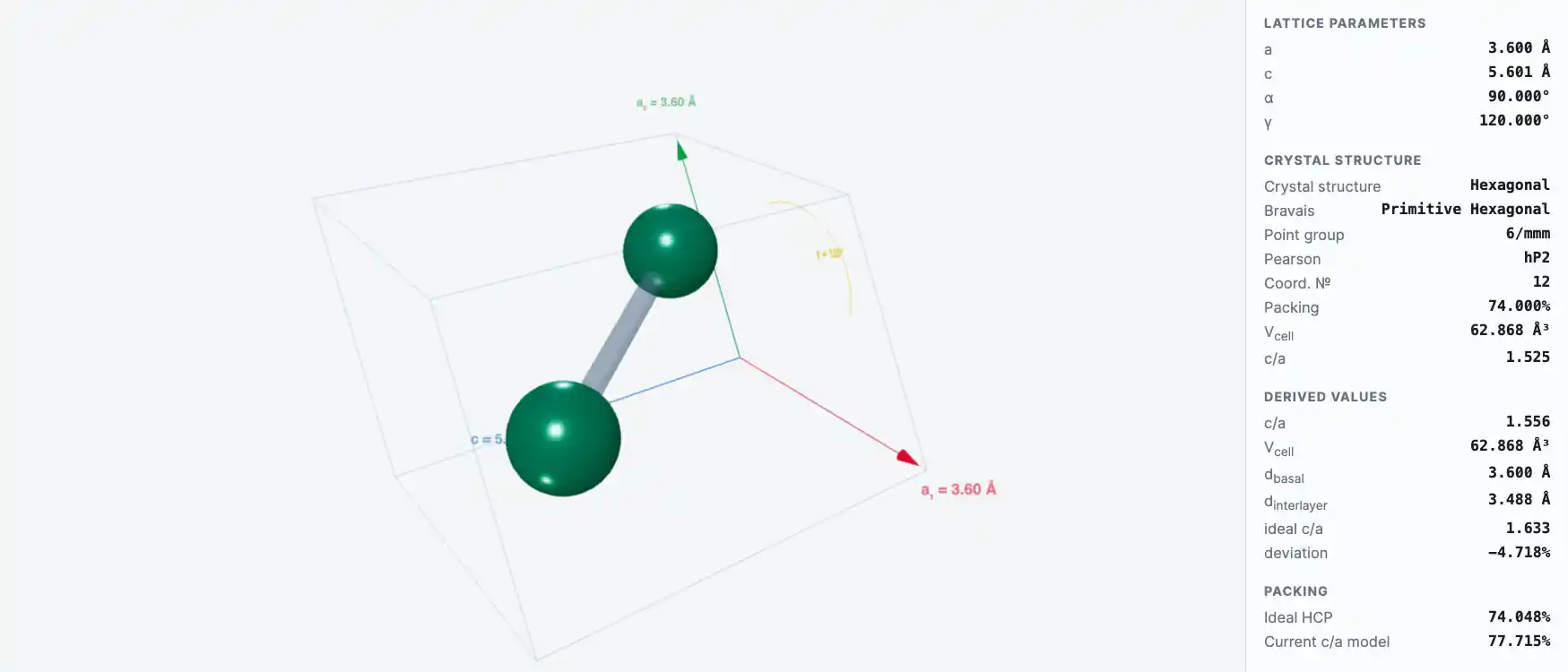
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Tb: 4f⁹ 6s²[Xe] 4f⁹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f⁹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 159 Стабильный | 158,9253547 ± 0,0000019 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 1330.8 °C ниже точки плавления (1355.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 65 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Tb I | 0 | 248 | 0 | 10 |
| Tb II | +1 | 424 | 8 | 18 |
| Tb IV | +3 | 48 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Tb I | 0 | 600 |
| Tb II | +1 | 154 |
| Tb III | +2 | 125 |
| Tb IV | +3 | 26 |
| Tb V | +4 | 2 |
| Tb VI | +5 | 2 |
| Tb VII | +6 | 2 |
| Tb VIII | +7 | 2 |
| Tb IX | +8 | 2 |
| Tb X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 92.30000000000001 пм |
| +3 | 7 | N/A | 98 пм |
| +3 | 8 | N/A | 104 пм |
| +3 | 9 | N/A | 109.5 пм |
| +4 | 6 | N/A | 76 пм |
| +4 | 8 | N/A | 88 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 159 Стабильный | 158,9253547 ± 0,0000019 | 100.0000% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1632.15 K |
| Температура кипения | 3503.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.2739 |
| 2 | p | 4.3076 |
| 2 | s | 17.0278 |
| 3 | d | 13.7015 |
| 3 | p | 19.9853 |
| 3 | s | 20.4485 |
| 4 | d | 34.69 |
| 4 | f | 39.1352 |
| 4 | p | 31.6012 |
| 4 | s | 30.98 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 106.3 | from r^3 vs V plots, | |
| 3 | VII | 112 | estimated, | |
| 3 | VIII | 118 | from r^3 vs V plots, | |
| 3 | IX | 123.5 | from r^3 vs V plots, | |
| 4 | VI | 90 | from r^3 vs V plots, | |
| 4 | VIII | 102 |
Режимы распада изотопов (63)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 135 | p | 100% |
| 135 | B+ | — |
| 136 | B+ | — |
| 136 | B+p | — |
| 137 | p | — |
| 137 | B+ | — |
| 138 | B+ | — |
| 138 | B+p | — |
| 138 | p | 0% |
| 139 | B+ | 100% |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.15974 |
| 10.1617 | — | 0.16625 |
| 10.3261 | — | 0.17301 |
| 10.4931 | — | 0.18005 |
| 10.6628 | — | 0.18738 |
| 10.8353 | — | 0.19501 |
| 11.0106 | — | 0.20295 |
| 11.1886 | — | 0.21121 |
| 11.3696 | — | 0.21981 |
| 11.5535 | — | 0.22823 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.2 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.4×10-7 milligrams per liter
Источники (1)
Production
Production of this element (from raw materials or other compounds containing the element).
Terbium has been isolated only in recent years with the development of ion-exchange techniques for separating the rare-earth elements. As with other rare earth metals, it can be produced by reducing the anhydrous chloride or fluoride with calcium metal in a tantalum crucible. Calcium and tantalum impurities can be removed by vacuum remelting. Other methods of isolation are possible.
Источники (1)
- [6] Terbium https://periodic.lanl.gov/65.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Terbium.
The element property data was retrieved from publications.