Гольмий (Ho)
ЛантаноидТвёрдое тело
Стандартный атомный вес
164.93033 uЭлектронная конфигурация
[Xe] 6s2 4f11Температура плавления
1473.85 °C (1747 K)Температура кипения
2699.85 °C (2973 K)Плотность
8800 kg/m³Степени окисления
0, +1, +2, +3Электроотрицательность (Полинг)
1.23Энергия ионизации (1-я)
Год открытия
1878Атомный радиус
175 pmДополнительно
Гольмий — металл лантаноид и один из тяжелых редкоземельных элементов. В соединениях он почти всегда трехвалентен, образуя соли Ho³⁺ с розовой, желтой или бледной окраской, типичной для f-электронных переходов. Природный гольмий моноизотопен и по существу состоит из стабильного ¹⁶⁵Ho. Его большой магнитный момент придает элементу и некоторым его соединениям необычное магнитное поведение при низкой температуре.
Чистый гольмий имеет металлический блеск до ярко-серебристого. Он относительно мягкий и пластичный, устойчив в сухом воздухе при комнатной температуре, но быстро окисляется во влажном воздухе и при повышенных температурах. Металл обладает необычными магнитными свойствами. Пока для этого элемента найдено мало применений. Как и другие редкоземельные элементы, он, по-видимому, обладает низкой острой токсичностью.
Название происходит от латинского holmia, означающего Стокгольм. Он был обнаружен в эрбии швейцарским химиком Ж. Л. Соре в 1878 году, который называл его элементом X. Позднее он был независимо открыт шведским химиком Пером Теодором Клеве в 1879 году. Впервые он был выделен в 1911 году Хомбергом, который предложил название «гольмий» либо в знак признания первооткрывателя Пера Клеве, который был родом из Стокгольма, либо, возможно, чтобы увековечить собственное имя в истории.
Гольмий был открыт Пером Теодором Клеве, шведским химиком, в 1879 году. Клеве использовал тот же метод, который Карл Густав Мосандер применил для открытия лантана, эрбия и тербия: он искал примеси в оксидах других редкоземельных элементов. Он начал с эрбии, оксида эрбия (Er2O3), и удалил все известные примеси. После дальнейшей обработки он получил два новых вещества, одно коричневое и одно зеленое. Клеве назвал коричневое вещество хольмией, а зеленое — тулией. Хольмия является оксидом элемента гольмия, а тулия — оксидом элемента тулия. Спектр поглощения гольмия был наблюден ранее в том же году швейцарскими химиками Ж. Л. Соре и М. Делафонтеном. Сегодня гольмий в основном получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами, который может содержать до 0,05% гольмия. У гольмия нет коммерческих применений, хотя он обладает необычными магнитными свойствами, которые могут быть использованы в будущем.
Гольмий не образует соединений, имеющих коммерческое значение. Среди соединений гольмия: оксид гольмия (Ho2O3), фторид гольмия (HoF3) и йодид гольмия (HoI3).
От латинского слова Holmia, означающего Стокгольм. Особые полосы поглощения гольмия были замечены в 1878 году швейцарскими химиками Делафонтеном и Соре, которые объявили о существовании «элемента X». Клеве из Швеции позднее независимо открыл элемент, работая с эрбиевой землей. Элемент назван в честь родного города Клеве. Хольмия, желтый оксид, была приготовлена Хомбергом в 1911 году. Гольмий встречается в гадолините, монаците и других редкоземельных минералах. В промышленности его получают из монацита, где он содержится примерно в количестве 0,05%. Он был выделен восстановлением безводного хлорида или фторида кальцием.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
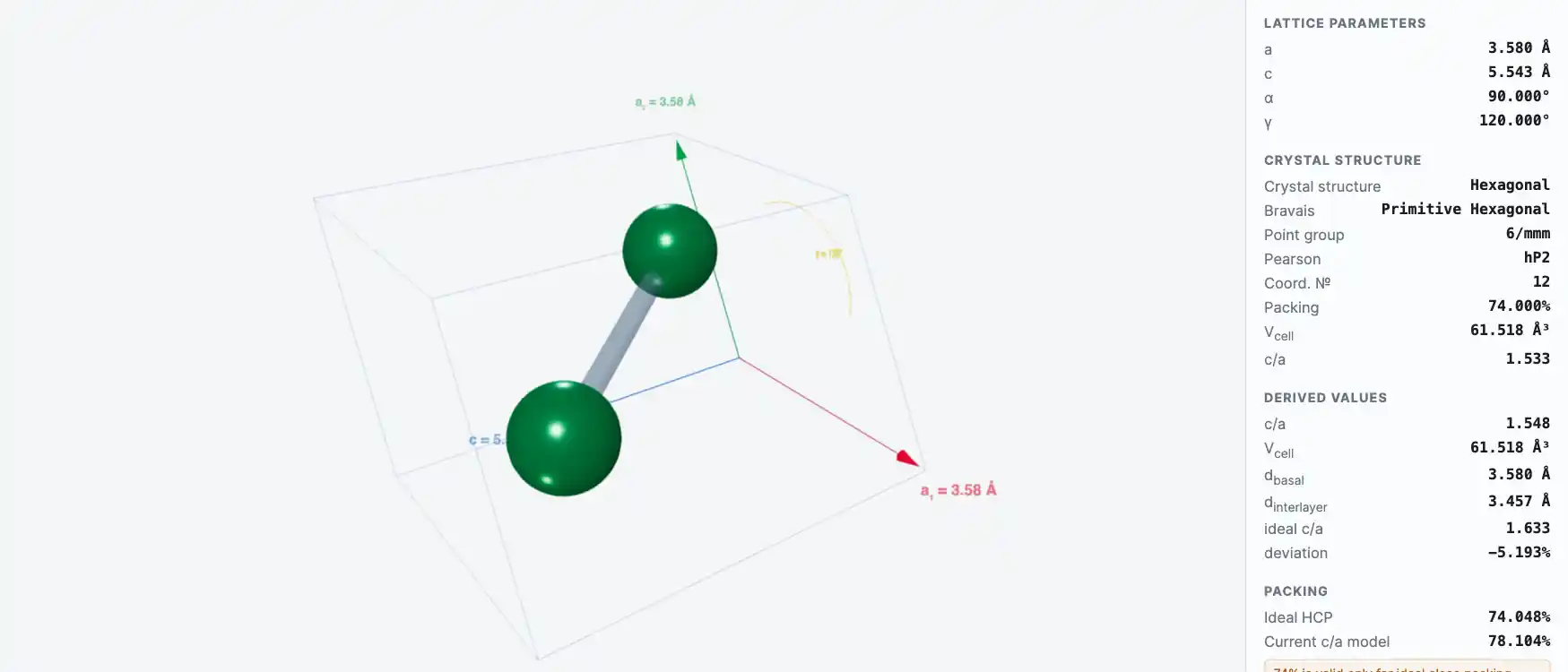
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Ho: 4f¹¹ 6s²[Xe] 4f¹¹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹¹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 165 Стабильный | 164,9303288 ± 0,0000021 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 1448.8 °C ниже точки плавления (1473.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 67 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Ho I | 0 | 282 | 13 | 13 |
| Ho II | +1 | 284 | 4 | 12 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Ho I | 0 | 234 |
| Ho II | +1 | 55 |
| Ho III | +2 | 126 |
| Ho IV | +3 | 21 |
| Ho V | +4 | 2 |
| Ho VI | +5 | 2 |
| Ho VII | +6 | 2 |
| Ho VIII | +7 | 2 |
| Ho IX | +8 | 2 |
| Ho X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 90.10000000000001 пм |
| +3 | 8 | N/A | 101.49999999999999 пм |
| +3 | 9 | N/A | 107.2 пм |
| +3 | 10 | N/A | 112.00000000000001 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 165 Стабильный | 164,9303288 ± 0,0000021 | 100.0000% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1745.15 K |
| Температура кипения | 2973.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.3088 |
| 2 | p | 4.3332 |
| 2 | s | 17.5444 |
| 3 | d | 13.6531 |
| 3 | p | 20.2546 |
| 3 | s | 20.7649 |
| 4 | d | 35.3284 |
| 4 | f | 39.5304 |
| 4 | p | 32.4372 |
| 4 | s | 31.688 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 104.1 | from r^3 vs V plots, | |
| 3 | VIII | 115.5 | from r^3 vs V plots, | |
| 3 | IX | 121.2 | from r^3 vs V plots, | |
| 3 | X | 126 |
Режимы распада изотопов (57)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 140 | p | — |
| 140 | B+ | — |
| 140 | B+p | — |
| 141 | p | 100% |
| 141 | B+ | — |
| 141 | B+p | — |
| 142 | B+ | 100% |
| 142 | B+p | — |
| 142 | p | 0% |
| 143 | B+ | — |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.16762 |
| 10.1617 | — | 0.17164 |
| 10.3261 | — | 0.17576 |
| 10.4931 | — | 0.17997 |
| 10.6628 | — | 0.18429 |
| 10.8353 | — | 0.1887 |
| 11.0106 | — | 0.19366 |
| 11.1886 | — | 0.20086 |
| 11.3696 | — | 0.20833 |
| 11.5535 | — | 0.21608 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.3 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
2.2×10-7 milligrams per liter
Источники (1)
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Holmium.
The element property data was retrieved from publications.