Гадолиний (Gd)
ЛантаноидТвёрдое тело
Стандартный атомный вес
157.25 uЭлектронная конфигурация
[Xe] 6s2 4f7 5d1Температура плавления
1312.85 °C (1586 K)Температура кипения
3272.85 °C (3546 K)Плотность
7900 kg/m³Степени окисления
0, +1, +2, +3Электроотрицательность (Полинг)
1.2Энергия ионизации (1-я)
Год открытия
1886Атомный радиус
180 pmДополнительно
Гадолиний — серебристый металл-лантаноид и один из средних редкоземельных элементов. Его химия определяется степенью окисления +3, но семь неспаренных 4f-электронов придают ему необычно сильные магнитные свойства для редкоземельного элемента. Природный гадолиний представляет собой смесь стабильных изотопов, причем ¹⁵²Gd очень долгоживущий и слабо радиоактивный. Элемент технологически важен в магнитных материалах, поглощении нейтронов, люминофорах и медицинских контрастных веществах.
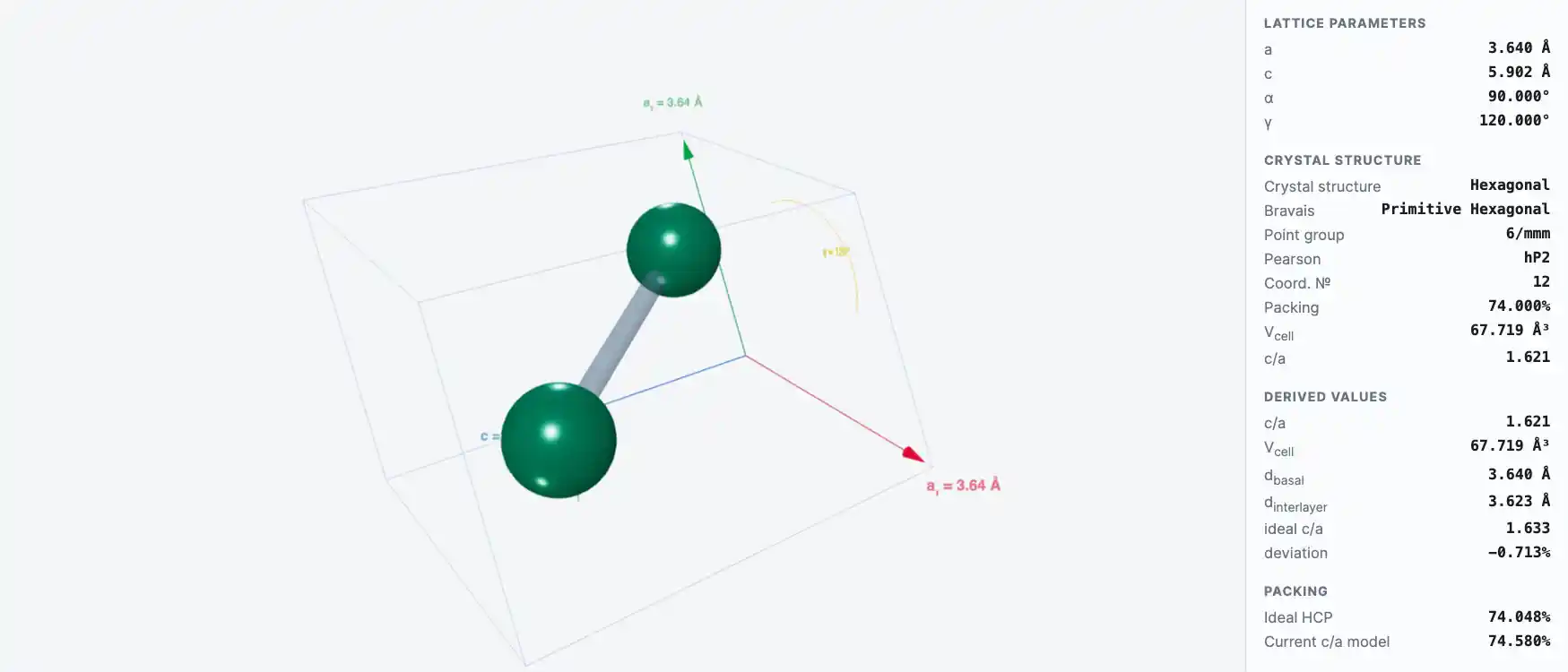
Как и другие родственные редкоземельные металлы, гадолиний серебристо-белый, обладает металлическим блеском, ковок и пластичен. При комнатной температуре гадолиний кристаллизуется в гексагональной плотноупакованной α-форме. При нагревании до 1235°C α-гадолиний переходит в β-форму, имеющую объёмно-центрированную кубическую структуру.
Металл относительно стабилен в сухом воздухе, но тускнеет во влажном воздухе и образует слабо прилипшую оксидную плёнку, которая отслаивается и открывает для окисления новые участки поверхности. Металл медленно реагирует с водой и растворим в разбавленной кислоте.
Гадолиний имеет наибольшее сечение захвата тепловых нейтронов среди всех известных элементов (49,000 barns).
Название происходит от минерала гадолинита, в котором он был найден, названного в честь финского химика-редкоземельщика Йохана Гадолина. Гадолиний был открыт швейцарским химиком Жаном-Шарлем Галисаром де Мариньяком в 1886 году, который получил белый оксид в минерале самарскита. В 1886 году французский химик Поль-Эмиль Лекок де Буабодран дал этому элементу название гадолиний.
Спектроскопические доказательства существования гадолиния впервые были обнаружены швейцарским химиком Жаном Шарлем Галисаром де Мариньяком в минералах дидимии и гадолините ((Ce, La, Nd, Y)2FeBe2Si2O10) в 1880 году. Сегодня гадолиний в основном получают из минералов монацита ((Ce, La, Th, Nd, Y)PO4) и бастнезита ((Ce,La,Y)CO3F).
От гадолинита, минерала, названного в честь Гадолина, финского химика. Редкоземельный металл получают из минерала гадолинита. Гадолиния, оксид гадолиния, был выделен Мариньяком в 1880 году, а Лекок де Буабодран независимо изолировал его из иттрий Mosандера в 1886 году.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Gd: 4f⁷ 5d¹ 6s²[Xe] 4f⁷ 5d¹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f⁷ 5d¹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 154 Стабильный | 153,9208741 ± 0,0000017 | 2.1800% | Стабильный |
| 155 Стабильный | 154,9226305 ± 0,0000017 | 14.8000% | Стабильный |
| 156 Стабильный | 155,9221312 ± 0,0000017 | 20.4700% | Стабильный |
| 157 Стабильный | 156,9239686 ± 0,0000017 | 15.6500% | Стабильный |
| 158 Стабильный | 157,9241123 ± 0,0000017 | 24.8400% | Стабильный |
Фазовое состояние
Причина: на 1287.8 °C ниже точки плавления (1312.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 64 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Gd I | 0 | 371 | 16 | 19 |
| Gd II | +1 | 465 | 0 | 17 |
| Gd III | +2 | 158 | 0 | 0 |
| Gd IV | +3 | 50 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Gd I | 0 | 634 |
| Gd II | +1 | 321 |
| Gd III | +2 | 28 |
| Gd IV | +3 | 5 |
| Gd V | +4 | 2 |
| Gd VI | +5 | 2 |
| Gd VII | +6 | 2 |
| Gd VIII | +7 | 2 |
| Gd IX | +8 | 2 |
| Gd X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 93.8 пм |
| +3 | 7 | N/A | 100 пм |
| +3 | 8 | N/A | 105.3 пм |
| +3 | 9 | N/A | 110.7 пм |
Соединения
Изотопы (5)
Natural gadolinium is a mixture of seven isotopes, but 17 isotopes of gadolinium are now recognized. Although two of these, 155Gd and 157Gd, have excellent capture characteristics, they are only present naturally in low concentrations. As a result, gadolinium has a very fast burnout rate and has limited use as a nuclear control rod material.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 154 Стабильный | 153,9208741 ± 0,0000017 | 2.1800% ± 0.0300% | Стабильный | stable | |
| 155 Стабильный | 154,9226305 ± 0,0000017 | 14.8000% ± 0.1200% | Стабильный | stable | |
| 156 Стабильный | 155,9221312 ± 0,0000017 | 20.4700% ± 0.0900% | Стабильный | stable | |
| 157 Стабильный | 156,9239686 ± 0,0000017 | 15.6500% ± 0.0200% | Стабильный | stable | |
| 158 Стабильный | 157,9241123 ± 0,0000017 | 24.8400% ± 0.0700% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1586.15 K |
| Температура кипения | 3546.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.2565 |
| 2 | p | 4.2946 |
| 2 | s | 16.783 |
| 3 | d | 13.723 |
| 3 | p | 19.8508 |
| 3 | s | 20.2903 |
| 4 | d | 34.3664 |
| 4 | f | 38.9864 |
| 4 | p | 31.3532 |
| 4 | s | 30.556 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 107.8 | from r^3 vs V plots, | |
| 3 | VII | 114 | ||
| 3 | VIII | 119.3 | from r^3 vs V plots, | |
| 3 | IX | 124.7 | from r^3 vs V plots, calculated, |
Режимы распада изотопов (57)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 133 | B+ | — |
| 133 | B+p | — |
| 134 | B+ | — |
| 134 | B+p | — |
| 135 | B+ | 100% |
| 135 | B+p | 2% |
| 136 | B+ | — |
| 136 | B+p | — |
| 137 | B+ | 100% |
| 137 | B+p | — |
Факторы рассеяния X‑лучей (719)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 2.59886 |
| 10.1152 | — | 2.63957 |
| 10.2317 | — | 2.68119 |
| 10.3496 | — | 2.72415 |
| 10.4688 | — | 2.7678 |
| 10.5894 | — | 2.81214 |
| 10.7114 | — | 2.8572 |
| 10.8348 | — | 2.90298 |
| 10.9596 | — | 2.94949 |
| 11.0859 | — | 2.99675 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
6.2 milligrams per kilogram
Источники (1)
- [5] Gadolinium https://education.jlab.org/itselemental/ele064.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
7×10-7 milligrams per liter
Источники (1)
- [5] Gadolinium https://education.jlab.org/itselemental/ele064.html
Sources
Sources of this element.
Gadolinium is found in several other minerals, including monazite and bastnasite, both of which are commercially important. With the development of ion-exchange and solvent extraction techniques, the availability and prices of gadolinium and the other rare-earth metals have greatly improved. The metal can be prepared by the reduction of the anhydrous fluoride with metallic calcium.
Источники (1)
- [6] Gadolinium https://periodic.lanl.gov/64.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Gadolinium.
The element property data was retrieved from publications.