Европий (Eu)
ЛантаноидТвёрдое тело
Стандартный атомный вес
151.964 uЭлектронная конфигурация
[Xe] 6s2 4f7Температура плавления
821.85 °C (1095 K)Температура кипения
1528.85 °C (1802 K)Плотность
5240 kg/m³Степени окисления
0, +2, +3Электроотрицательность (Полинг)
N/AЭнергия ионизации (1-я)
Год открытия
1896Атомный радиус
185 pmДополнительно
Европий — это редкоземельный металл-лантаноид с атомным номером 63. Он химически примечателен относительной устойчивостью как Eu³⁺, так и Eu²⁺, что контрастирует с большинством лантаноидов, для которых доминирует состояние +3. Эта редокс-изменчивость определяет большую часть его минералогического поведения и оптических применений. Европий лучше всего известен интенсивной узкой люминесценцией ионов Eu³⁺ и Eu²⁺ в твёрдых матрицах, особенно в люминофорах и защитных материалах.
Как и другие редкоземельные металлы, за исключением лантана, европий воспламеняется на воздухе примерно при 150–180°C. Европий примерно такой же твёрдый, как свинец, и довольно пластичен. Это наиболее реакционноспособный из редкоземельных металлов, быстро окисляющийся на воздухе. По реакции с водой он напоминает кальций. Бастнезит и монацит являются основными рудами, содержащими европий.
Название происходит от континента Европа. Он был выделен из минерала самарии в виде магний-самариевой селитры французским химиком Эженом-Антуаном Демарсе в 1896 году. Впервые он также был изолирован Демарсе в 1901 году.
Европий был открыт французским химиком Эженом-Антуаном Демарсе в 1896 году. Демарсе подозревал, что образцы недавно открытого элемента самария загрязнены неизвестным элементом. Ему удалось получить достаточно чистый европий в 1901 году. Сегодня европий преимущественно получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами.
Назван в честь Европы. В 1890 году Буабодран получил основные фракции из концентратов самарий- гадолиния, которые давали в искровом спектре линии, не объясняемые самарием или гадолинием. Позднее было показано, что эти линии принадлежат европию. Открытие европия обычно приписывают Демарсе, который в 1901 году выделил редкоземельный элемент в достаточно чистом виде. Чистый металл был выделен лишь в последние годы.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
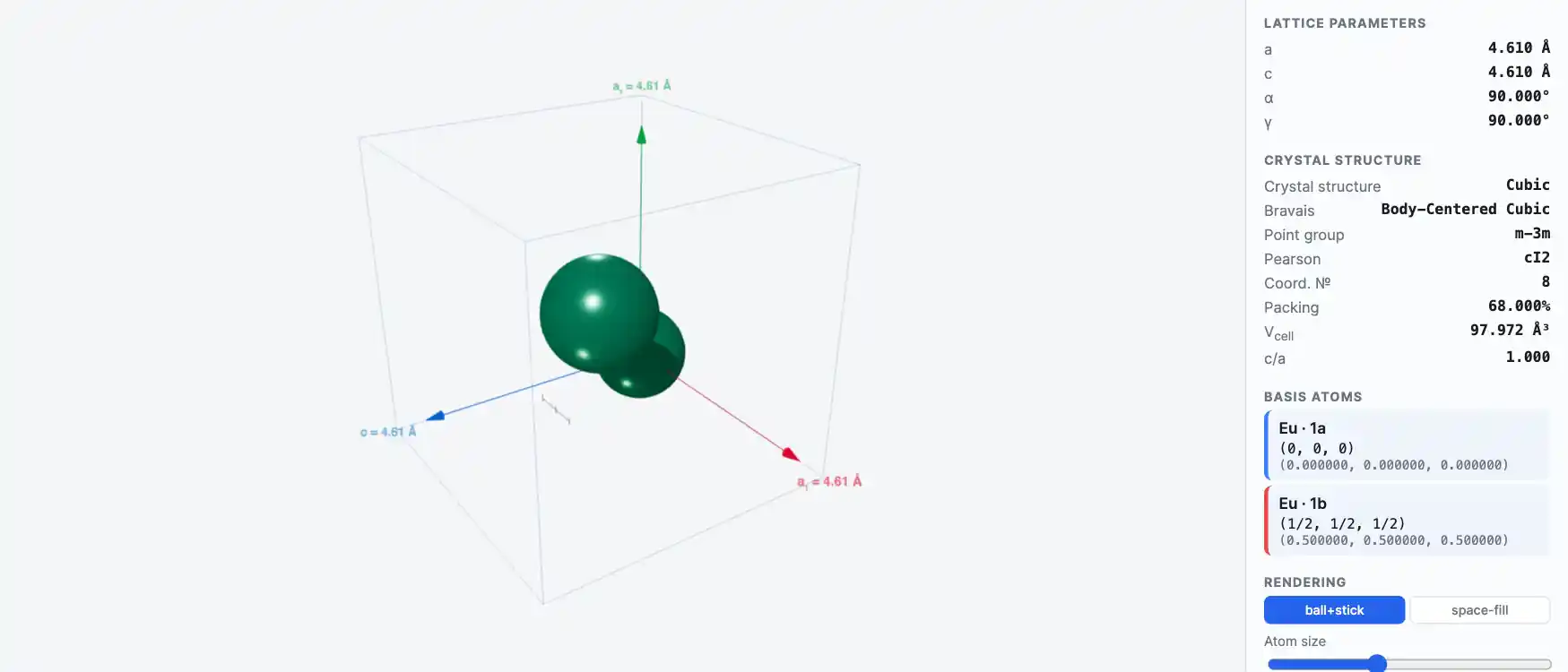
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Eu: 4f⁷ 6s²[Xe] 4f⁷ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f⁷ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
Нет стабильных изотопов.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 153 Радиоактивный | 152,921238 ± 0,0000018 | 52.1900% | 550 Py |
| 134 Радиоактивный | 133,9464 ± 0,00032 | N/A | 500 мс |
| 169 Радиоактивный | 168,961717 ± 0,000537 | N/A | 420 мс |
| 133 Радиоактивный | 132,94929 ± 0,00032 | N/A | 200 мс |
| 168 Радиоактивный | 167,957863 ± 0,000429 | N/A | 200 мс |
Фазовое состояние
Причина: на 796.9 °C ниже точки плавления (821.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 63 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Eu I | 0 | 350 | 152 | 343 |
| Eu II | +1 | 218 | 13 | 13 |
| Eu III | +2 | 229 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Eu I | 0 | 592 |
| Eu II | +1 | 163 |
| Eu III | +2 | 118 |
| Eu IV | +3 | 13 |
| Eu V | +4 | 2 |
| Eu VI | +5 | 2 |
| Eu VII | +6 | 2 |
| Eu VIII | +7 | 2 |
| Eu IX | +8 | 2 |
| Eu X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +2 | 6 | N/A | 117 пм |
| +2 | 7 | N/A | 120 пм |
| +2 | 8 | N/A | 125 пм |
| +2 | 9 | N/A | 130 пм |
| +2 | 10 | N/A | 135 пм |
| +3 | 6 | N/A | 94.69999999999999 пм |
| +3 | 7 | N/A | 101 пм |
| +3 | 8 | N/A | 106.60000000000001 пм |
| +3 | 9 | N/A | 112.00000000000001 пм |
Соединения
Изотопы (5)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 153 Радиоактивный | 152,921238 ± 0,0000018 | 52.1900% ± 0.0600% | 550 Py | IS =52.19±0.6% | |
| 134 Радиоактивный | 133,9464 ± 0,00032 | N/A | 500 мс | β+ =100%β+p =? | |
| 169 Радиоактивный | 168,961717 ± 0,000537 | N/A | 420 мс | β- ? | |
| 133 Радиоактивный | 132,94929 ± 0,00032 | N/A | 200 мс | β+ ?β+p ? | |
| 168 Радиоактивный | 167,957863 ± 0,000429 | N/A | 200 мс | β- =100%β-n ? |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1095.15 K |
| Температура кипения | 1802.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.2391 |
| 2 | p | 4.282 |
| 2 | s | 16.5292 |
| 3 | d | 13.7472 |
| 3 | p | 19.716 |
| 3 | s | 20.1318 |
| 4 | d | 34.0592 |
| 4 | f | 38.68 |
| 4 | p | 31.1252 |
| 4 | s | 30.132 |
Детализация кристаллических радиусов (9)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 2 | VI | 131 | ||
| 2 | VII | 134 | ||
| 2 | VIII | 139 | ||
| 2 | IX | 144 | ||
| 2 | X | 149 | ||
| 3 | VI | 108.7 | from r^3 vs V plots, | |
| 3 | VII | 115 | ||
| 3 | VIII | 120.6 | from r^3 vs V plots, | |
| 3 | IX | 126 | from r^3 vs V plots, |
Режимы распада изотопов (63)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 130 | p | 100% |
| 130 | B+ | — |
| 130 | B+p | — |
| 131 | p | 89% |
| 131 | B+ | — |
| 131 | B+p | — |
| 132 | B+ | — |
| 132 | B+p | — |
| 132 | p | 0% |
| 133 | B+ | — |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.18583 |
| 10.1617 | — | 0.19489 |
| 10.3261 | — | 0.20439 |
| 10.4931 | — | 0.21435 |
| 10.6628 | — | 0.22479 |
| 10.8353 | — | 0.23529 |
| 11.0106 | — | 0.24598 |
| 11.1886 | — | 0.25716 |
| 11.3696 | — | 0.26817 |
| 11.5535 | — | 0.27854 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.0 milligrams per kilogram
Источники (1)
- [5] Europium https://education.jlab.org/itselemental/ele063.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.3×10-7 milligrams per liter
Источники (1)
- [5] Europium https://education.jlab.org/itselemental/ele063.html
Sources
Sources of this element.
Europium has been identified spectroscopically in the sun and certain stars. Seventeen isotopes are now recognized. Europium isotopes are good neutron absorbers and are being studied for use in nuclear control applications.
Источники (1)
- [6] Europium https://periodic.lanl.gov/63.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
Europium is now prepared by mixing Eu2O3 with a 10%-excess of lanthanum metal and heating the mixture in a tantalum crucible under high vacuum. The element is collected as a silvery-white metallic deposit on the walls of the crucible.
Источники (1)
- [6] Europium https://periodic.lanl.gov/63.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Europium.
The element property data was retrieved from publications.