Лантан (La)
ЛантаноидТвёрдое тело
Стандартный атомный вес
138.90547 uЭлектронная конфигурация
[Xe] 6s2 5d1Температура плавления
917.85 °C (1191 K)Температура кипения
3463.85 °C (3737 K)Плотность
6150 kg/m³Степени окисления
0, +1, +2, +3Электроотрицательность (Полинг)
1.1Энергия ионизации (1-я)
Год открытия
1839Атомный радиус
195 pmДополнительно
Лантан — первый элемент ряда лантаноидов по общепринятой классификации, хотя его 4f-оболочка в нейтральном атоме пуста. Это мягкий, реакционноспособный редкоземельный металл, встречающийся вместе с другими легкими редкоземельными элементами в минералах, таких как монацит и бастнезит. Его химия определяется крупным ионом La³⁺, который образует в основном бесцветные, сильно ионные соединения. Лантан имеет важное значение в оптическом стекле, катализаторах, аккумуляторных сплавах и высокотемпературных керамических материалах.
Лантан серебристо-белый, ковкий, пластичный и достаточно мягкий, чтобы его можно было резать ножом. Это один из наиболее реакционноспособных редкоземельных металлов. Он быстро окисляется при воздействии воздуха. Холодная вода медленно действует на лантан, тогда как горячая — значительно быстрее.
Металл непосредственно реагирует с элементарными углеродом, азотом, бором, селеном, кремнием, фосфором, серой и с галогенами.
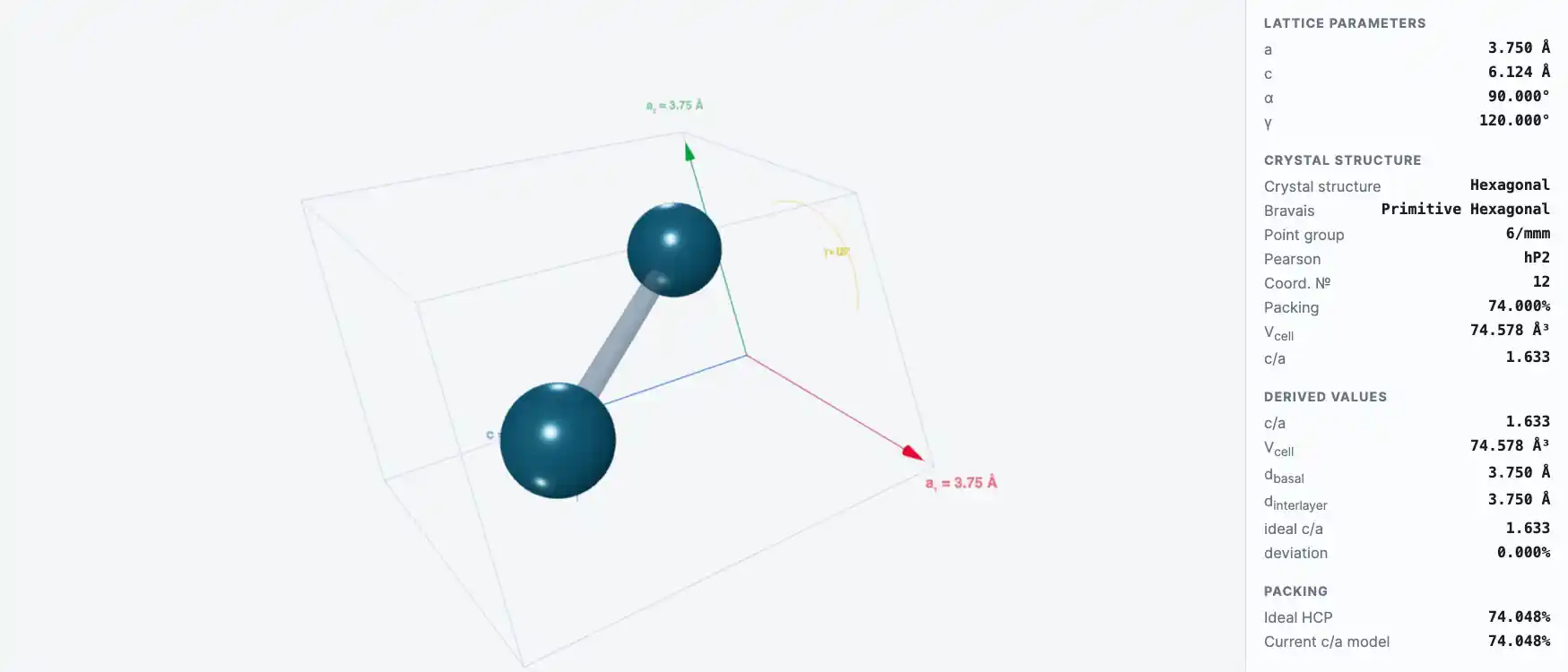
При 310°C лантан переходит из гексагональной в гранецентрированную кубическую структуру, а при 865°C вновь переходит в объёмно-центрированную кубическую структуру.
Название происходит от греческого lanthanein, означающего «быть скрытым» или «ускользать от внимания», поскольку он скрывался в цериевой руде и его было трудно отделить от этого редкоземельного минерала. Лантан был открыт шведским хирургом и химиком Карлом-Густавом Мосандером в 1839 году. В 1842 году Мосандер разделил свой образец лантания на два оксида; для одного из них он сохранил название лантан, а для другого дал название дидимий (или близнец).
Лантан был открыт Карлом Густавом Мосандером, шведским химиком, в 1839 году. Мосандер искал примеси, которые, по его мнению, существовали в образцах церия. Он обработал нитрат церия (Ce(NO3)3) разбавленной азотной кислотой (HNO3) и обнаружил новое вещество, которое назвал лантаной (La2O3). Примерно 0,0018% земной коры состоит из лантана. Сегодня лантан в основном получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами, который может содержать до 25% лантана.
От греческого слова lanthanein, ускользать от внимания. Мосандер в 1839 году выделил лантану из нечистого нитрата церия и распознал новый элемент.
Лантан был выделен в относительно чистой форме в 1923 году. Методы ионообменного и экстракционного разделения значительно облегчили выделение так называемых «редкоземельных» элементов.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
La: 5d¹ 6s²[Xe] 5d¹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 5d¹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 139 Стабильный | 138,9063563 ± 0,0000024 | 99.9112% | Стабильный |
Фазовое состояние
Причина: на 892.9 °C ниже точки плавления (917.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 57 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| La I | 0 | 393 | 315 | 393 |
| La II | +1 | 273 | 84 | 273 |
| La III | +2 | 122 | 0 | 0 |
| La IV | +3 | 87 | 0 | 0 |
| La V | +4 | 42 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| La I | 0 | 343 |
| La II | +1 | 119 |
| La III | +2 | 42 |
| La IV | +3 | 52 |
| La V | +4 | 37 |
| La VI | +5 | 2 |
| La VII | +6 | 2 |
| La VIII | +7 | 2 |
| La IX | +8 | 2 |
| La X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 103.2 пм |
| +3 | 7 | N/A | 110.00000000000001 пм |
| +3 | 8 | N/A | 115.99999999999999 пм |
| +3 | 9 | N/A | 121.6 пм |
| +3 | 10 | N/A | 127 пм |
| +3 | 12 | N/A | 136 пм |
Соединения
Изотопы (1)
Natural lanthanum is a mixture of two stable isotopes, 138La and 139La. Twenty three other radioactive isotopes are recognized.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 139 Стабильный | 138,9063563 ± 0,0000024 | 99.9112% ± 0.0007% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1193.15 K |
| Температура кипения | 3737.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.1317 |
| 2 | p | 4.2044 |
| 2 | s | 15.0466 |
| 3 | d | 13.9398 |
| 3 | p | 18.8604 |
| 3 | s | 19.0569 |
| 4 | d | 32.2748 |
| 4 | f | 55.64 |
| 4 | p | 29.2936 |
| 4 | s | 28.2036 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 117.2 | from r^3 vs V plots, | |
| 3 | VII | 124 | ||
| 3 | VIII | 130 | from r^3 vs V plots, | |
| 3 | IX | 135.6 | from r^3 vs V plots, | |
| 3 | X | 141 | ||
| 3 | XII | 150 | calculated, |
Режимы распада изотопов (64)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 116 | B+ | — |
| 116 | B+p | — |
| 116 | p | — |
| 117 | p | 100% |
| 117 | B+ | — |
| 117 | B+p | — |
| 118 | B+ | — |
| 118 | B+p | — |
| 119 | B+ | — |
| 120 | B+ | 100% |
Факторы рассеяния X‑лучей (711)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 3.31251 |
| 10.1152 | — | 3.28769 |
| 10.2317 | — | 3.26306 |
| 10.3496 | — | 3.23861 |
| 10.4688 | — | 3.20975 |
| 10.5894 | — | 3.15961 |
| 10.7114 | — | 3.11024 |
| 10.8348 | — | 3.06165 |
| 10.9596 | — | 3.01382 |
| 11.0859 | — | 2.96673 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
3.9×101 milligrams per kilogram
Источники (1)
- [5] Lanthanum https://education.jlab.org/itselemental/ele057.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
3.4×10-6 milligrams per liter
Источники (1)
- [5] Lanthanum https://education.jlab.org/itselemental/ele057.html
Sources
Sources of this element.
Lanthanum is found in rare-earth minerals such as cerite, monazite, allanite, and bastnasite. Monazite and bastnasite are principal ores in which lanthanum occurs in percentages up to 25 percent and 38 percent respectively. Misch metal, used in making lighter flints, contains about 25 percent lanthanum.
The availability of lanthanum and other rare earths has improved greatly in recent years. The metal can be produced by reducing the anhydrous fluoride with calcium.
Источники (1)
- [6] Lanthanum https://periodic.lanl.gov/57.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Lanthanum.
The element property data was retrieved from publications.