Церий (Ce)
ЛантаноидТвёрдое тело
Стандартный атомный вес
140.116 uЭлектронная конфигурация
[Xe] 6s2 4f1 5d1Температура плавления
797.85 °C (1071 K)Температура кипения
3423.85 °C (3697 K)Плотность
6770 kg/m³Степени окисления
+1, +2, +3, +4Электроотрицательность (Полинг)
1.12Энергия ионизации (1-я)
Год открытия
1801Атомный радиус
185 pmДополнительно
Церий — это первый лантаноид по атомному номеру и один из наиболее распространённых редкоземельных элементов в земной коре. Это реакционноспособный, электроотрицательный металл, чья химия необычна среди лантаноидов, поскольку в обычных соединениях доступны как Ce³⁺, так и Ce⁴⁺. Эта редокс-пара Ce³⁺/Ce⁴⁺, особенно в оксидах, делает церий важным в катализаторах, полировальных материалах, обработке стекла и системах накопления кислорода.
Церий особенно интересен из-за своей изменчивой электронной структуры. Энергия внутреннего уровня 4f почти такая же, как у внешних (валентных) электронов, и для изменения относительного заполнения этих электронных уровней требуется лишь небольшое количество энергии. Это приводит к двум состояниям валентности.
Например, при воздействии на церий высокого давления или низких температур происходит изменение объёма примерно на 10 процентов. Валентность цезия, по-видимому, изменяется примерно с 3 до 4 при охлаждении или сжатии. Поведение церия при низких температурах сложно.
Церий — блестящий металл железо-серого цвета. Он ковок и очень легко окисляется при комнатной температуре, особенно во влажном воздухе. За исключением европия, церий — наиболее реакционноспособный из редкоземельных металлов. Он медленно разлагается в холодной воде и быстро — в горячей воде.
Щёлочные растворы, а также разбавленные и концентрированные кислоты быстро разрушают металл. Чистый металл, если поцарапать его ножом, может легко воспламениться.
Соли церия имеют оранжево-красную или желтоватую окраску; соли церия(III) обычно белые.
Название происходит от планетоиды Церера, которая была открыта итальянским астрономом Джузеппе Пьяцци в 1801 году и названа в честь Цереры, римской богини земледелия и урожая. Два года спустя элемент церий был открыт немецким химиком Мартином-Хайнрихом Клапротом, который назвал его охроитовой землей из-за желтого цвета.
Церий был независимо открыт в то же время шведским химиком Йёнсом Якобом Берцелиусом и шведским минералогом Вильгельмом фон Гизингером, которые назвали его церией. Впервые он был выделен в 1875 году американским минералогом и химиком Уильямом Фрэнсисом Хиллебрандом и американским химиком Томасом Х. Нортоном.
Церий был открыт Йёнсом Якобом Берцелиусом и Вильгельмом фон Гизингером, шведскими химиками, а независимо от них — Мартином Генрихом Клапротом, немецким химиком, в 1803 году. Церий является самым распространенным из редкоземельных элементов и составляет около 0,0046% земной коры. Сегодня церий в основном получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами.
Церий был назван в честь астероида Церера, открытого в 1801 году. Элемент был открыт два года спустя, в 1803 году, Клапротом и Берцелиусом с Гизингером. В 1875 году Хиллебранд и Нортон получили металл.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
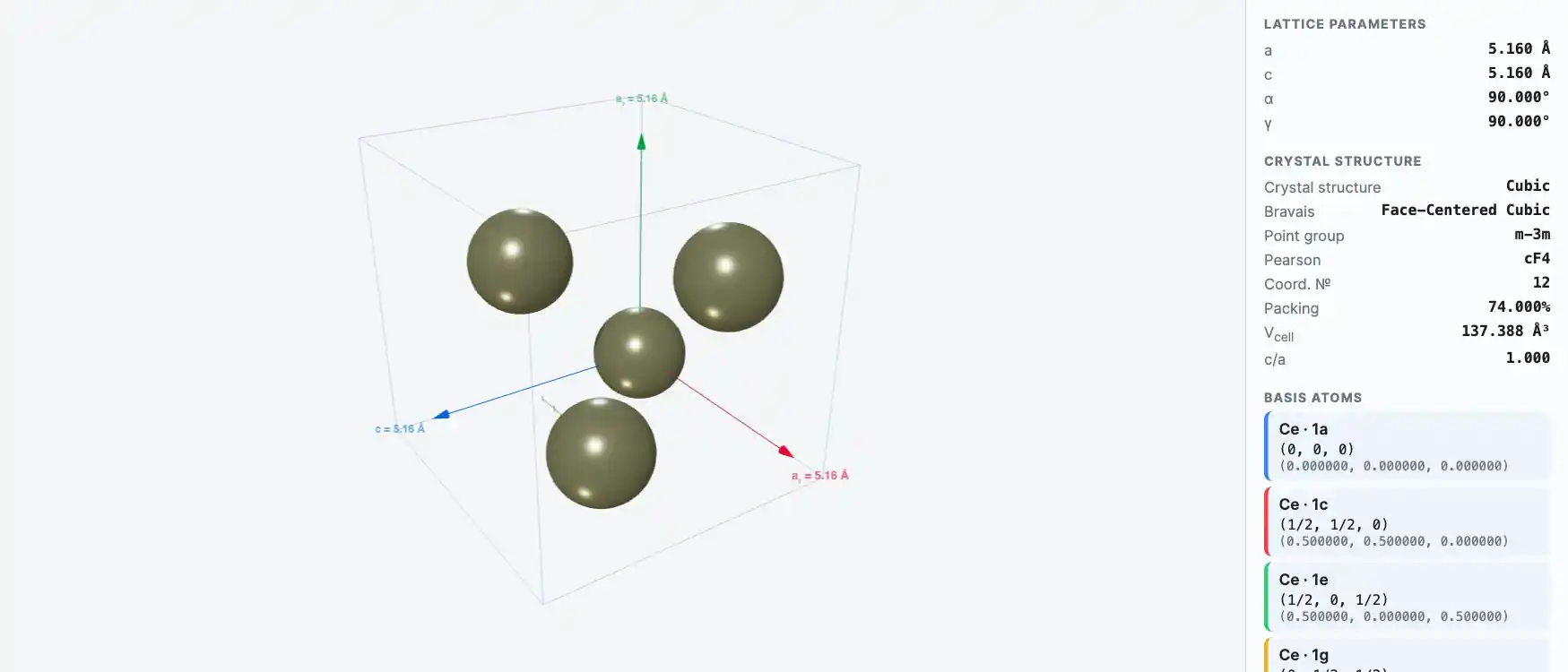
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Ce: 4f¹ 5d¹ 6s²[Xe] 4f¹ 5d¹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹ 5d¹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 140 Стабильный | 139,9054431 ± 0,0000023 | 88.4500% | Стабильный |
Фазовое состояние
Причина: на 772.9 °C ниже точки плавления (797.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 58 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Ce I | 0 | 209 | 67 | 209 |
| Ce II | +1 | 560 | 283 | 560 |
| Ce III | +2 | 262 | 0 | 0 |
| Ce IV | +3 | 27 | 0 | 0 |
| Ce V | +4 | 5 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Ce I | 0 | 953 |
| Ce II | +1 | 491 |
| Ce III | +2 | 227 |
| Ce IV | +3 | 17 |
| Ce V | +4 | 12 |
| Ce VI | +5 | 4 |
| Ce VII | +6 | 2 |
| Ce VIII | +7 | 2 |
| Ce IX | +8 | 2 |
| Ce X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 101 пм |
| +3 | 7 | N/A | 107 пм |
| +3 | 8 | N/A | 114.3 пм |
| +3 | 9 | N/A | 119.6 пм |
| +3 | 10 | N/A | 125 пм |
| +3 | 12 | N/A | 134 пм |
| +4 | 6 | N/A | 87 пм |
| +4 | 8 | N/A | 97 пм |
| +4 | 10 | N/A | 97 пм |
| +4 | 12 | N/A | 113.99999999999999 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 140 Стабильный | 139,9054431 ± 0,0000023 | 88.4500% ± 0.0510% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1072.15 K |
| Температура кипения | 3716.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (13)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.1519 |
| 2 | p | 4.2176 |
| 2 | s | 15.26 |
| 3 | d | 13.9147 |
| 3 | p | 19.0405 |
| 3 | s | 19.3408 |
| 4 | d | 32.3392 |
| 4 | f | 56.324 |
| 4 | p | 29.3936 |
| 4 | s | 28.32 |
Детализация кристаллических радиусов (10)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 115 | from r^3 vs V plots, | |
| 3 | VII | 121 | estimated, | |
| 3 | VIII | 128.3 | from r^3 vs V plots, | |
| 3 | IX | 133.6 | from r^3 vs V plots, | |
| 3 | X | 139 | ||
| 3 | XII | 148 | calculated, | |
| 4 | VI | 101 | from r^3 vs V plots, | |
| 4 | VIII | 111 | from r^3 vs V plots, | |
| 4 | X | 121 | from r^3 vs V plots, | |
| 4 | XII | 128 |
Режимы распада изотопов (54)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 119 | B+ | — |
| 119 | B+p | — |
| 120 | B+ | — |
| 120 | B+p | — |
| 121 | B+ | 100% |
| 121 | B+p | 1% |
| 122 | B+ | — |
| 122 | B+p | — |
| 123 | B+ | 100% |
| 123 | B+p | — |
Факторы рассеяния X‑лучей (508)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.28369 |
| 10.1617 | — | 1.26389 |
| 10.3261 | — | 1.24441 |
| 10.4931 | — | 1.22522 |
| 10.6628 | — | 1.20632 |
| 10.8353 | — | 1.18772 |
| 11.0106 | — | 1.16941 |
| 11.1886 | — | 1.15138 |
| 11.3696 | — | 1.13362 |
| 11.5535 | — | 1.11614 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
6.65×101 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.2×10-6 milligrams per liter
Источники (1)
Sources
Sources of this element.
Cerium is the most abundant so-called rare-earth metals. It is found in a number of minerals including allanite (also known as orthite), monazite, bastnasite, cerite, and samarskite. Monazite and bastnasite are presently the more important sources of cerium.
Large deposits of monazite (found on the beaches of Travancore, India and in river sands in Brazil), allanite (in the western United States), and bastnasite (in Southern California) will supply cerium, thorium, and the other rare-earth metals for many years to come.
Metallic cerium is prepared by metallothermic reduction techniques, such as reducing cerous fluoride with calcium, or using electrolysis of molten cerous chloride or others processes. The metallothermic technique produces high-purity cerium.
Источники (1)
- [6] Cerium https://periodic.lanl.gov/58.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Cerium.
The element property data was retrieved from publications.