Ксенон (Xe)
Благородный газГаз
Стандартный атомный вес
131.293 uЭлектронная конфигурация
[Kr] 5s2 4d10 5p6Температура плавления
-111.79 °C (161.36 K)Температура кипения
-108.1 °C (165.05 K)Плотность
5.887 kg/m³Степени окисления
0, +2, +4, +6, +8Электроотрицательность (Полинг)
2.6Энергия ионизации (1-я)
Год открытия
1898Атомный радиус
N/AДополнительно
Ксенон — тяжелый благородный газ с электронной конфигурацией замкнутой оболочки и очень низкой химической реакционной способностью в обычных условиях. В атмосфере он присутствует лишь в следовых количествах и извлекается из процессов разделения воздуха. Его большая атомная масса, легкость ионизации и сильное ультрафиолетовое излучение делают его технологически полезным, а способность образовывать устойчивые соединения с высокоэлектроотрицательными элементами отличает его от более легких благородных газов.
Ксенон используется в сверхярких лампах, применяемых для наблюдений в глубоком море.
Название происходит от греческого xenos — «чужой». Он был открыт шотландским химиком Уильямом Рамзаем и английским химиком Моррисом Уильямом Траверсом в 1898 году в образце жидкого воздуха.
Ксенон был открыт сэром Уильямом Рамзаем, шотландским химиком, и Моррисом М. Траверсом, английским химиком, 12 июля 1898 года, вскоре после их открытия элементов криптона и неона. Как и криптон и неон, ксенон был открыт при изучении жидкого воздуха. Атмосфера Земли содержит около 0,0000087% ксенона.
От греческого слова xenon, чужой. Открыт в 1898 году Рамзаем и Траверсом в остатке, оставшемся после испарения жидкого воздуха. Ксенон относится к так называемым благородным или «инертным» газам. В атмосфере он присутствует в количестве около одной части на двадцать миллионов. В атмосфере Марса ксенон присутствует в количестве 0,08 ppm. Элемент обнаружен в газах, выделяющихся из некоторых минеральных источников, и промышленно получается путем извлечения из жидкого воздуха.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
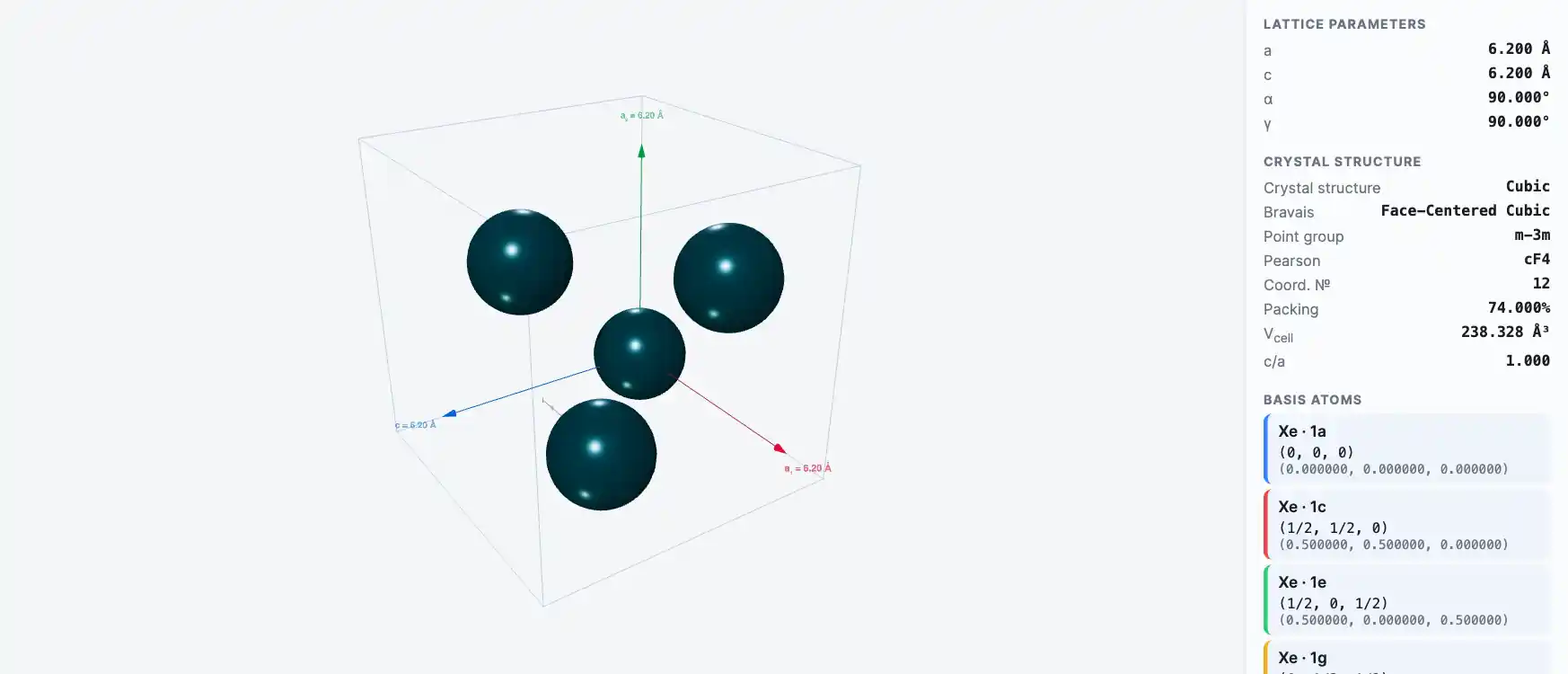
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Xe: 4d¹⁰ 5s² 5p⁶[Kr] 4d¹⁰ 5s² 5p⁶1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 126 Стабильный | 125,9042983 ± 0,0000038 | 0.0890% | Стабильный |
| 128 Стабильный | 127,903531 ± 0,0000011 | 1.9102% | Стабильный |
| 129 Стабильный | 128,9047808611 ± 0,000000006 | 26.4006% | Стабильный |
| 130 Стабильный | 129,903509349 ± 0,00000001 | 4.0710% | Стабильный |
| 131 Стабильный | 130,90508406 ± 0,00000024 | 21.2324% | Стабильный |
| 132 Стабильный | 131,9041550856 ± 0,0000000056 | 26.9086% | Стабильный |
Фазовое состояние
Причина: на 133.1 °C выше точки кипения (-108.1 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Расчёт по уравнению идеального газа при текущей T
Дополнительно
Атомные спектры
Показано 10 из 54 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Xe I | 0 | 1143 | 187 | 1143 |
| Xe II | +1 | 1115 | 22 | 1115 |
| Xe III | +2 | 1512 | 0 | 1512 |
| Xe IV | +3 | 769 | 0 | 769 |
| Xe V | +4 | 273 | 0 | 273 |
| Xe VI | +5 | 126 | 0 | 126 |
| Xe VII | +6 | 131 | 0 | 131 |
| Xe VIII | +7 | 135 | 0 | 135 |
| Xe IX | +8 | 144 | 0 | 144 |
| Xe X | +9 | 83 | 0 | 83 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Xe I | 0 | 445 |
| Xe II | +1 | 164 |
| Xe III | +2 | 158 |
| Xe IV | +3 | 95 |
| Xe V | +4 | 55 |
| Xe VI | +5 | 73 |
| Xe VII | +6 | 73 |
| Xe VIII | +7 | 83 |
| Xe IX | +8 | 61 |
| Xe X | +9 | 63 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +8 | 4 | N/A | 40 пм |
| +8 | 6 | N/A | 48 пм |
Соединения
Изотопы (6)
Natural xenon is composed of nine stable isotopes. In addition to these, 20 unstable isotopes have been characterized. Before 1962, it had generally been assumed that xenon and other noble gases were unable to form compounds. Evidence has been mounting in the past few years that xenon, as well as other members of zero valance elements, do form compounds. Among the "compounds" of xenon now reported are sodium perxenate, xenon deuterate, xenon hydrate, difluoride, tetrafluoride, and hexafluoride. Xenon trioxide, which is highly explosive, has been prepared. More than 80 xenon compounds have been made with xenon chemically bonded to fluorine and oxygen. Some xenon compounds are colored. Metallic xenon has been produced, using several hundred kilobars of pressure. Xenon in a vacuum tube produces a beautiful blue glow when excited by an electrical discharge.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 126 Стабильный | 125,9042983 ± 0,0000038 | 0.0890% ± 0.0002% | Стабильный | stable | |
| 128 Стабильный | 127,903531 ± 0,0000011 | 1.9102% ± 0.0008% | Стабильный | stable | |
| 129 Стабильный | 128,9047808611 ± 0,000000006 | 26.4006% ± 0.0082% | Стабильный | stable | |
| 130 Стабильный | 129,903509349 ± 0,00000001 | 4.0710% ± 0.0013% | Стабильный | stable | |
| 131 Стабильный | 130,90508406 ± 0,00000024 | 21.2324% ± 0.0030% | Стабильный | stable | |
| 132 Стабильный | 131,9041550856 ± 0,0000000056 | 26.9086% ± 0.0033% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Свойства инертного газа
| O₂ | forms oxides indirectly (XeO3, XeO4) |
| HALOGENS | XeF2, XeF4, XeF6 |
| OXIDES_TYPE | acidic |
Фазовые переходы и аллотропы
| Температура плавления | 161.4 K |
| Температура кипения | 165.05 K |
| Критическая точка (температура) | 289.73 K |
| Критическая точка (давление) | 5.84 MPa |
| Тройная точка (температура) | 161.4 K |
| Тройная точка (давление) | 81.77 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (11)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.0785 |
| 2 | p | 4.1654 |
| 2 | s | 14.197 |
| 3 | d | 14.0532 |
| 3 | p | 18.3324 |
| 3 | s | 18.4236 |
| 4 | d | 32.1068 |
| 4 | p | 29.0428 |
| 4 | s | 27.8272 |
| 5 | p | 41.5755 |
Детализация кристаллических радиусов (2)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 8 | IV | 54 | ||
| 8 | VI | 62 |
Режимы распада изотопов (68)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 108 | A | 100% |
| 109 | A | 100% |
| 109 | B+ | — |
| 109 | B+p | — |
| 110 | A | 64% |
| 110 | B+ | 36% |
| 110 | B+p | — |
| 111 | B+ | 89.6% |
| 111 | A | 10.4% |
| 111 | B+p | — |
Факторы рассеяния X‑лучей (509)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0 |
| 10.1617 | — | 0 |
| 10.3261 | — | 0 |
| 10.4931 | — | 0 |
| 10.6628 | — | 0 |
| 10.8353 | — | 0 |
| 11.0106 | — | 0 |
| 11.1886 | — | 0 |
| 11.3696 | — | 0 |
| 11.5535 | — | 0 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
3×10-5 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
5×10-5 milligrams per liter
Источники (1)
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
Radiogenic xenon isotopes are produced by nuclear reactions in atomic bombs and nuclear reactors. For example, 131Xe, 133Xe, and 135Xe are some of the fission products of 235U and 239Pu, and finding these isotopes would be evidence of a nuclear bomb reaction. Measurements of xenon isotopes (e.g. in the atmosphere or the subsurface) have been used to identify contamination from these sources, for example, to detect faults in nuclear reactors or to monitor compliance with nuclear test bans (Fig. IUPAC.54.1) [396] [396] P. R. J. Saey, C. Schlosser, P. Achim, M. Auer, A. Axelsson, A. Becker, X. Blanchard, G. Brachet, L. Cella, L.-E. De Geer, M. B. Kalinowski, G. Le Petit, J. Peterson, V. Popov, Y. Popov, A. Ringbom, H. Sartorius, T. Taffary, M. Zähringer. Pure Appl. Geophy.167, 499 (2010).[396] P. R. J. Saey, C. Schlosser, P. Achim, M. Auer, A. Axelsson, A. Becker, X. Blanchard, G. Brachet, L. Cella, L.-E. De Geer, M. B. Kalinowski, G. Le Petit, J. Peterson, V. Popov, Y. Popov, A. Ringbom, H. Sartorius, T. Taffary, M. Zähringer. Pure Appl. Geophy.167, 499 (2010)..
Источники (2)
- [396] P. R. J. Saey, C. Schlosser, P. Achim, M. Auer, A. Axelsson, A. Becker, X. Blanchard, G. Brachet, L. Cella, L.-E. De Geer, M. B. Kalinowski, G. Le Petit, J. Peterson, V. Popov, Y. Popov, A. Ringbom, H. Sartorius, T. Taffary, M. Zähringer. Pure Appl. Geophy.167, 499 (2010).
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Xenon.
The element property data was retrieved from publications.