Йод (I)
ГалогенТвёрдое тело
Стандартный атомный вес
126.90447 uЭлектронная конфигурация
[Kr] 5s2 4d10 5p5Температура плавления
113.7 °C (386.85 K)Температура кипения
184.4 °C (457.55 K)Плотность
4930 kg/m³Степени окисления
−1, +1, +2, +3, +4, +5, +6, +7Электроотрицательность (Полинг)
2.66Энергия ионизации (1-я)
Год открытия
1811Атомный радиус
140 pmДополнительно
Йод — это тяжёлый галоген и наименее распространённый стабильный галоген в земной коре. В природе элемент встречается в виде иодида и иодата, а не в виде свободного I₂. Он химически менее электроотрицателен и менее сильно окисляет, чем бром или хлор, и образует широкий спектр ковалентных, ионных и полииодидных соединений. Йод является жизненно важным микроэлементом для позвоночных, поскольку гормоны щитовидной железы содержат атомы йода.
Йод — голубовато-чёрное, блестящее твёрдое вещество, улетучивающееся при обычных температурах в синий-violet газ с раздражающим запахом; он образует соединения со многими элементами, но менее активен, чем другие галогены, которые вытесняют его из йодидов. Йод проявляет некоторые свойства, сходные с металлическими. Он легко растворяется в хлороформе, четырёххлористом углероде или сероуглероде с образованием красивых пурпурных растворов. Он лишь слабо растворим в воде.
Название происходит от греческого iodes, «фиолетовый», из-за его фиолетовых паров. Йод был открыт во водорослях французским химиком Бернаром Куртуа в 1811 году и назван французским химиком Луи-Жозефом Гей-Люссаком, когда тот доказал, что это элемент, в 1814 году.
Йод был открыт французским химиком Бернаром Куртуа в 1811 году. Куртуа извлекал соединения натрия и калия из золы морских водорослей. После удаления этих соединений он добавил серную кислоту (H2SO4) для дальнейшей обработки золы. Он случайно добавил слишком много кислоты, и из массы вырвалось фиолетово окрашенное облако. Газ сконденсировался на металлических предметах в комнате, образовав твёрдый йод. Сегодня йод главным образом получают из залежей йодата натрия (NaIO3) и периодата натрия (NaIO4) в Чили и Боливии. Следовые количества йода необходимы человеческому организму. Йод входит в состав тироксина, гормона, вырабатываемого щитовидной железой и контролирующего скорость физического и умственного развития организма. Недостаток йода также может вызывать зоб, увеличение щитовидной железы. Йод добавляют в соль (йодированная соль) для предотвращения этих заболеваний.
От греческого слова iodes, фиолетовый. Открыт Куртуа в 1811 году, йод, галоген, в небольших количествах встречается в виде йодидов в морской воде, из которой он усваивается водорослями, в чилийской селитре, нитратсодержащих землях (известных как каличе), рассолах из старых морских отложений и в солоноватых водах нефтяных и соляных скважин.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
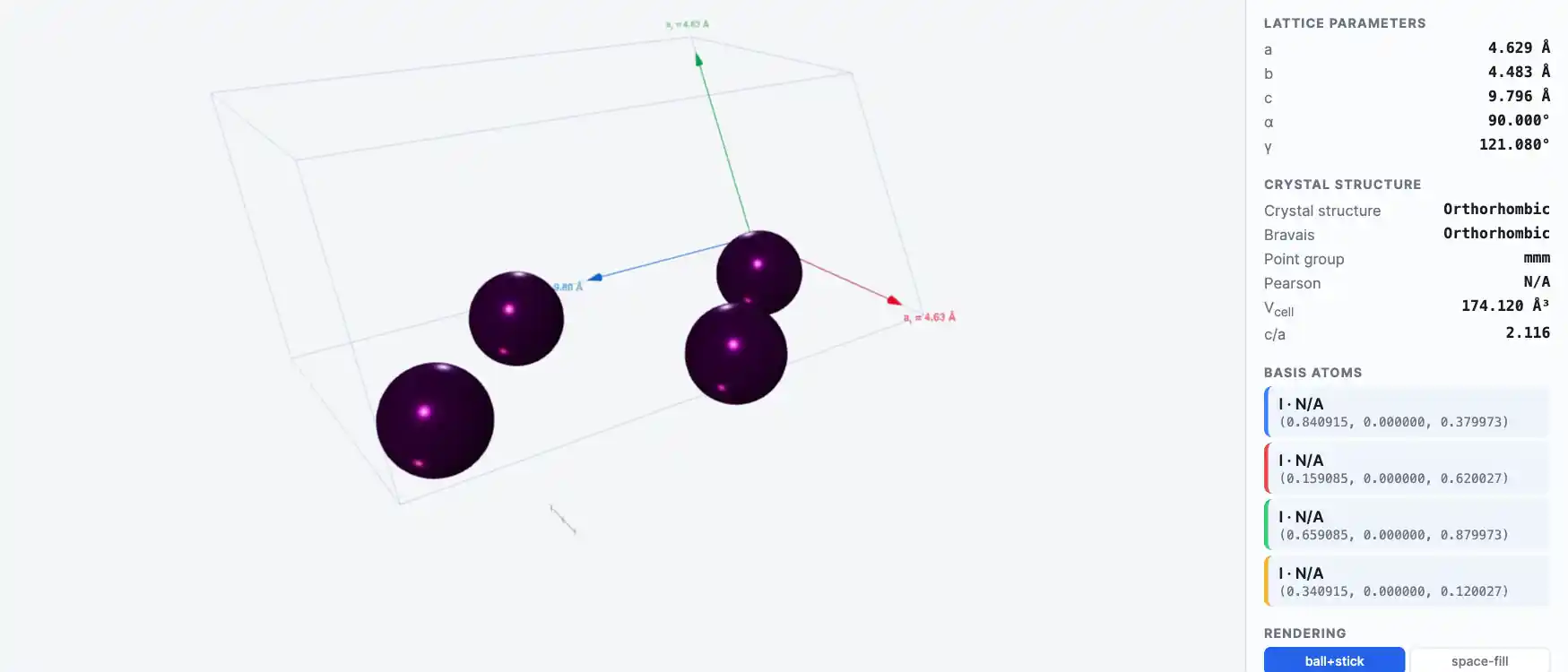
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
I: 4d¹⁰ 5s² 5p⁵[Kr] 4d¹⁰ 5s² 5p⁵1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁵Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 127 Стабильный | 126,9044719 ± 0,0000039 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 88.7 °C ниже точки плавления (113.7 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 53 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| I I | 0 | 1432 | 417 | 1432 |
| I II | +1 | 126 | 0 | 122 |
| I III | +2 | 76 | 0 | 0 |
| I IV | +3 | 47 | 0 | 0 |
| I V | +4 | 4 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| I I | 0 | 229 |
| I II | +1 | 315 |
| I III | +2 | 116 |
| I IV | +3 | 61 |
| I V | +4 | 54 |
| I VI | +5 | 40 |
| I VII | +6 | 25 |
| I VIII | +7 | 36 |
| I IX | +8 | 2 |
| I X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| -1 | 6 | N/A | 220.00000000000003 пм |
| +5 | 3 | N/A | 44 пм |
| +5 | 6 | N/A | 95 пм |
| +7 | 4 | N/A | 42 пм |
| +7 | 6 | N/A | 53 пм |
Соединения
Изотопы (1)
Thirty isotopes are recognized. Only one stable isotope, 127I is found in nature. The artificial radioisotope 131I, with a half-life of 8 days, has been used in treating the thyroid gland. The most common compounds are the iodides of sodium and potassium (KI) and the iodates (KIO3). Lack of iodine is the cause of goiter.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 127 Стабильный | 126,9044719 ± 0,0000039 | 100.0000% | Стабильный | stable |
Спектральные линии
Показано 50 из 474 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 511.92792 нм | 120000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<2>).7p 2[1]* | Измерено | NIST | |
| 740.20433 нм | 98000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).7d 2[4] | Измерено | NIST | |
| 661.96418 нм | 88000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).8d 2[4] | Измерено | NIST | |
| 746.89862 нм | 87000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).7d 2[4] | Измерено | NIST | |
| 723.78303 нм | 68000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).5f 2[4]* | Измерено | NIST | |
| 714.20318 нм | 53000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).7d 2[3] | Измерено | NIST | |
| 658.3733 нм | 48000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).6f 2[4]* | Измерено | NIST | |
| 633.78649 нм | 44000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[3] | Измерено | NIST | |
| 619.1891 нм | 36000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).9d 2[4] | Измерено | NIST | |
| 712.20331 нм | 33000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).7d 2[3] | Измерено | NIST | |
| 514.55362 нм | 26000 | I I | emission | 5s2.5p4.(3P<1>).6s 2[1] → 5s2.5p4.(3P<1>).7p 2[1]* | Измерено | NIST | |
| 741.0472 нм | 25000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[4] → 5s2.5p4.(3P<2>).6f 2[5]* | Измерено | NIST | |
| 656.64687 нм | 23000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).8d 2[4] | Измерено | NIST | |
| 633.94468 нм | 22000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[3] | Измерено | NIST | |
| 722.72727 нм | 22000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).5f 2[3]* | Измерено | NIST | |
| 716.47586 нм | 21000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).7d 2[3] | Измерено | NIST | |
| 698.6488 нм | 20000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[4] → 5s2.5p4.(3P<2>).7f 2[5]* | Измерено | NIST | |
| 621.3101 нм | 19000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).9d 2[4] | Измерено | NIST | |
| 608.24072 нм | 18000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<1>).6p 2[2]* | Измерено | NIST | |
| 624.4475 нм | 17000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).7f 2[4]* | Измерено | NIST | |
| 631.31292 нм | 17000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[0] | Измерено | NIST | |
| 589.39929 нм | 16000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<1>).6p 2[1]* | Измерено | NIST | |
| 666.20777 нм | 15000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).8d 2[3] | Измерено | NIST | |
| 712.0036 нм | 15000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).7d 2[1] | Измерено | NIST | |
| 666.10964 нм | 14000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).9s 2[2] | Измерено | NIST | |
| 741.64587 нм | 14000 | I I | emission | 5s2.5p4.(3P<2>).5d 2[1] → 5s2.5p4.(3P<2>).5f 2[2]* | Измерено | NIST | |
| 595.6854 нм | 13000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).9d 2[3] | Измерено | NIST | |
| 598.4862 нм | 13000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).9d 2[2] | Измерено | NIST | |
| 637.16776 нм | 12000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[3] | Измерено | NIST | |
| 486.23094 нм | 11000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<2>).7p 2[3]* | Измерено | NIST | |
| 491.69357 нм | 11000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<2>).7p 2[2]* | Измерено | NIST | |
| 520.41202 нм | 11000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<2>).7p 2[1]* | Измерено | NIST | |
| 629.39502 нм | 11000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<0>).6p 2[1]* | Измерено | NIST | |
| 633.0376 нм | 11000 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[2] | Измерено | NIST | |
| 523.45653 нм | 10000 | I I | emission | 5s2.5p4.(3P<2>).6s 2[2] → 5s2.5p4.(3P<2>).7p 2[3]* | Измерено | NIST | |
| 533.82 нм | 10000 | I II | emission | 5s2.5p3.(2D*).6s 3D* → 5s2.5p3.(2D*).6p 3F | Измерено | NIST | |
| 562.569 нм | 10000 | I II | emission | 5s2.5p3.(4S*).6s 3S* → 5s2.5p3.(4S*).6p 3P | Измерено | NIST | |
| 707.78407 нм | 9700 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).7d 2[1] | Измерено | NIST | |
| 598.4207 нм | 8900 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).9d 2[3] | Измерено | NIST | |
| 742.00062 нм | 8300 | I I | emission | 5s2.5p4.(3P<2>).5d 2[4] → 5s2.5p4.(3P<2>).6f 2[4]* | Измерено | NIST | |
| 596.8258 нм | 7900 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).10d 2[4] | Измерено | NIST | |
| 698.97761 нм | 7800 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).9s 2[2] | Измерено | NIST | |
| 658.05101 нм | 7600 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).6f 2[3]* | Измерено | NIST | |
| 673.20067 нм | 7600 | I I | emission | 5s2.5p4.(3P<2>).5d 2[1] → 5s2.5p4.(3P<2>).6f 2[3]* | Измерено | NIST | |
| 595.4372 нм | 6700 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).9d 2[3] | Измерено | NIST | |
| 741.1195 нм | 6700 | I I | emission | 5s2.5p4.(3P<2>).5d 2[1] → 5s2.5p4.(3P<2>).5f 2[3]* | Измерено | NIST | |
| 656.08006 нм | 6600 | I I | emission | 5s2.5p4.(3P<2>).6p 2[3]* → 5s2.5p4.(3P<2>).8d 2[2] | Измерено | NIST | |
| 723.49797 нм | 6600 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).5f 2[4]* | Измерено | NIST | |
| 633.35136 нм | 6300 | I I | emission | 5s2.5p4.(3P<2>).6p 2[2]* → 5s2.5p4.(3P<2>).8d 2[1] | Измерено | NIST | |
| 723.17992 нм | 6200 | I I | emission | 5s2.5p4.(3P<2>).5d 2[3] → 5s2.5p4.(3P<2>).5f 2[3]* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 386.85 K |
| Температура кипения | 457.55 K |
| Критическая точка (температура) | 819.15 K |
| Тройная точка (температура) | 386.75 K |
| Тройная точка (давление) | 12.11 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (11)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.0609 |
| 2 | p | 4.1526 |
| 2 | s | 13.933 |
| 3 | d | 14.0993 |
| 3 | p | 18.1586 |
| 3 | s | 18.2126 |
| 4 | d | 32.066 |
| 4 | p | 28.9704 |
| 4 | s | 27.7028 |
| 5 | p | 41.3885 |
Детализация кристаллических радиусов (5)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| -1 | VI | 206 | Ahrens (1952) ionic radius, | |
| 5 | IIIPY | 58 | ||
| 5 | VI | 109 | ||
| 7 | IV | 56 | ||
| 7 | VI | 67 |
Режимы распада изотопов (82)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 106 | A | — |
| 107 | A | — |
| 108 | A | 99.5% |
| 108 | p | 0.5% |
| 108 | B+ | — |
| 108 | B+p | — |
| 109 | p | 100% |
| 109 | A | 0% |
| 110 | B+ | 83% |
| 110 | A | 17% |
Факторы рассеяния X‑лучей (508)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 7.8167 |
| 10.1617 | — | 7.56781 |
| 10.3261 | — | 7.32685 |
| 10.4931 | — | 7.08081 |
| 10.6628 | — | 6.8332 |
| 10.8353 | — | 6.78435 |
| 11.0106 | — | 6.80888 |
| 11.1886 | — | 7.27334 |
| 11.3696 | — | 7.86775 |
| 11.5535 | — | 8.52786 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
4.5×10-1 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
6×10-2 milligrams per liter
Источники (1)
Sources
Sources of this element.
Ultrapure iodine can be obtained from the reaction of potassium iodide with copper sulfate. Several other methods of isolating the element are known.
Источники (1)
- [6] Iodine https://periodic.lanl.gov/53.shtml
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
131I (with a half-life of about 8 days) and 129I are both fission products; 129I is a long-lived fission product with a half-life of 1.7×107 years that can be helpful in the detection of the movement of radiation after a radioactive event, such as occurred at the Japanese reactors at Fukushima. In nuclear reactors and weapons tests, uranium and plutonium undergo fission processes in which one of the fission products is the long-lived isotope 129I. This isotope has been used as a groundwater tracer to determine evidence of nuclear fission, and it can also be tracked in rainwater as evidence of a fission event in the air (weapons explosion; Fig. IUPAC.53.1) [390] [390] D. Elmore, H. E. Gove, R. Ferraro, L. R. Kilius, H. W. Lee, K. H. Chang, R. P. Beukens, A. E. Litherland, C. J. Russo, K. H. Purser, M. T. Murrell, R. C. Finkel. Nature286, 138 (1980).[390] D. Elmore, H. E. Gove, R. Ferraro, L. R. Kilius, H. W. Lee, K. H. Chang, R. P. Beukens, A. E. Litherland, C. J. Russo, K. H. Purser, M. T. Murrell, R. C. Finkel. Nature286, 138 (1980)., [391] [391] G. Snyder, U. Fehn. Nucl. Instrum. Methods Phys. Res. B223, 579 (2004).[391] G. Snyder, U. Fehn. Nucl. Instrum. Methods Phys. Res. B223, 579 (2004)., [392] [392] G. Snyder, A. Aldahan, G. Possnert. Geochem. Geophys.11, Q04010 (2010).[392] G. Snyder, A. Aldahan, G. Possnert. Geochem. Geophys.11, Q04010 (2010)..
Источники (4)
- [390] D. Elmore, H. E. Gove, R. Ferraro, L. R. Kilius, H. W. Lee, K. H. Chang, R. P. Beukens, A. E. Litherland, C. J. Russo, K. H. Purser, M. T. Murrell, R. C. Finkel. Nature286, 138 (1980).
- [391] G. Snyder, U. Fehn. Nucl. Instrum. Methods Phys. Res. B223, 579 (2004).
- [392] G. Snyder, A. Aldahan, G. Possnert. Geochem. Geophys.11, Q04010 (2010).
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Iodine.
The element property data was retrieved from publications.