Селен (Se)
НеметаллТвёрдое тело
Стандартный атомный вес
78.971 uЭлектронная конфигурация
[Ar] 4s2 3d10 4p4Температура плавления
220.5 °C (493.65 K)Температура кипения
684.85 °C (958 K)Плотность
4809 kg/m³Степени окисления
−2, −1, 0, +1, +2, +3, +4, +5, +6Электроотрицательность (Полинг)
2.55Энергия ионизации (1-я)
Год открытия
1817Атомный радиус
115 pmДополнительно
Селен — это халькоген между серой и теллуром, химия которого часто имеет параллели с обоими. Он является микроэлементом, необходимым многим организмам, поскольку входит в состав селенопротеинов, однако граница между потребностью в питании и токсичностью узка. В промышленности селен ценится за полупроводниковые и фотопроводящие свойства, за красный цвет в стекле, а также за роль в металлургии и производстве специальных химических веществ.
Селен существует в нескольких аллотропных формах, хотя обычно признают три из них. Селен может быть получен либо в аморфной, либо в кристаллической структуре. Цвет аморфного селена либо красный (в порошкообразной форме), либо чёрный (в стекловидной форме). Кристаллический моноклинный селен — тёмно-красный; кристаллический гексагональный селен, наиболее стабильная разновидность, — металлически серый.
Селен проявляет как фотовольтаическое действие, при котором свет непосредственно преобразуется в электричество, так и фотопроводимость, при которой электрическое сопротивление уменьшается с увеличением освещённости. Эти свойства делают селен полезным при производстве фотоэлементов и экспонометров для фотографического использования, а также солнечных элементов. Селен также способен преобразовывать переменный ток в постоянный и широко используется в выпрямителях. Ниже точки плавления селен является p-типом полупроводника и имеет множество применений в электронике и твердотельных устройствах.
Говорят, что элементарный селен практически нетоксичен и считается необходимым микроэлементом; однако селеноводород и другие соединения селена чрезвычайно токсичны и по своим физиологическим реакциям напоминают мышьяк.
Название происходит от греческой Селены, которая была греческой богиней Луны, поскольку этот элемент химически связан с теллуром (Теллус была римской богиней Земли). Селен был открыт шведским химиком Йёнсом Якобом Берцелиусом в 1817 году, когда он пытался выделить теллур из нечистого образца.
Селен был открыт Йёнсом Якобом Берцелиусом, шведским химиком, в 1817 году после анализа примеси, загрязнявшей серную кислоту (H2SO4), производившуюся на одном из заводов в Швеции. Сначала полагая, что это вещество является теллуром, Берцелиус в конце концов понял, что это на самом деле ранее неизвестный элемент. Селен встречается в таких минералах, как эвкаирит (CuAgSe), крукэсит (CuThSe) и клаусталит (PbSe), но эти минералы слишком редки, чтобы использовать их как основной источник селена. Сегодня большую часть селена получают как побочный продукт рафинирования меди.
От греческого слова Selene, луна. Открыт Берцелиусом в 1817 году, который обнаружил его в сочетании с теллуром (названным в честь Земли).
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
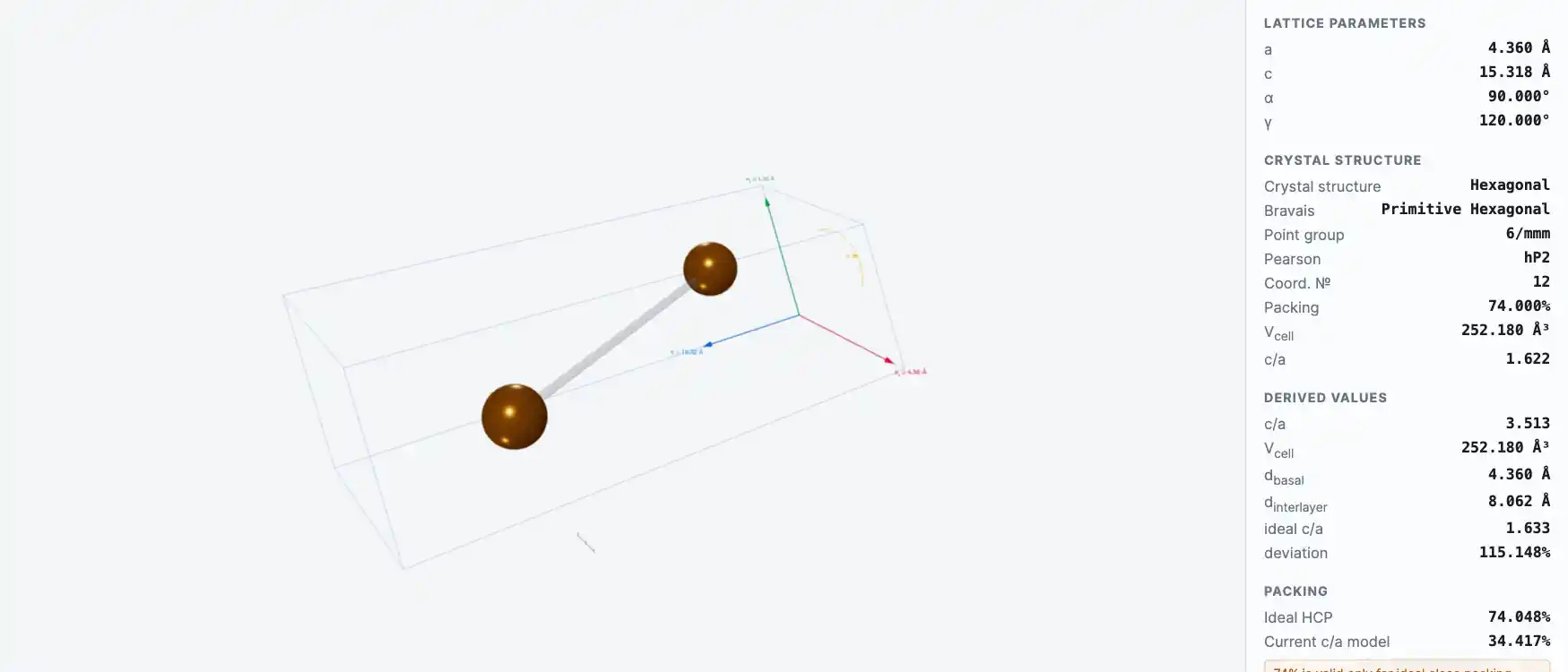
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Se: 3d¹⁰ 4s² 4p⁴[Ar] 3d¹⁰ 4s² 4p⁴1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁴Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 76 Стабильный | 75,919213704 ± 0,000000017 | 9.3700% | Стабильный |
| 77 Стабильный | 76,919914154 ± 0,000000067 | 7.6300% | Стабильный |
| 78 Стабильный | 77,91730928 ± 0,0000002 | 23.7700% | Стабильный |
| 80 Стабильный | 79,9165218 ± 0,0000013 | 49.6100% | Стабильный |
Фазовое состояние
Причина: на 195.5 °C ниже точки плавления (220.5 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 34 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Se I | 0 | 138 | 0 | 0 |
| Se II | +1 | 39 | 0 | 0 |
| Se III | +2 | 39 | 0 | 0 |
| Se IV | +3 | 22 | 0 | 0 |
| Se V | +4 | 17 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Se I | 0 | 173 |
| Se II | +1 | 78 |
| Se III | +2 | 53 |
| Se IV | +3 | 29 |
| Se V | +4 | 15 |
| Se VI | +5 | 7 |
| Se VII | +6 | 45 |
| Se VIII | +7 | 37 |
| Se IX | +8 | 2 |
| Se X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| -2 | 6 | N/A | 198 пм |
| +4 | 6 | N/A | 50 пм |
| +6 | 4 | N/A | 28.000000000000004 пм |
| +6 | 6 | N/A | 42 пм |
Соединения
Изотопы (4)
Naturally selenium contains six stable isotopes. Fifteen other isotopes have been characterized. The element is a member of the sulfur family and resembles sulfur both in its various forms and in its compounds.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 76 Стабильный | 75,919213704 ± 0,000000017 | 9.3700% ± 0.2900% | Стабильный | stable | |
| 77 Стабильный | 76,919914154 ± 0,000000067 | 7.6300% ± 0.1600% | Стабильный | stable | |
| 78 Стабильный | 77,91730928 ± 0,0000002 | 23.7700% ± 0.2800% | Стабильный | stable | |
| 80 Стабильный | 79,9165218 ± 0,0000013 | 49.6100% ± 0.4100% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура перехода | 453.15 K |
| Температура кипения | 958.15 K |
| Критическая точка (температура) | 1766.15 K |
| Температура плавления | 493.95 K |
| Температура кипения | 958.15 K |
| Критическая точка (температура) | 1766.15 K |
| Критическая точка (давление) | 27.2 MPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (8)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.7378 |
| 2 | p | 3.9348 |
| 2 | s | 9.1116 |
| 3 | d | 15.523 |
| 3 | p | 15.295 |
| 3 | s | 14.5966 |
| 4 | p | 25.7128 |
| 4 | s | 24.2424 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| -2 | VI | 184 | Pauling's (1960) crystal radius, | |
| 4 | VI | 64 | Ahrens (1952) ionic radius, | |
| 6 | IV | 42 | ||
| 6 | VI | 56 | calculated, |
Режимы распада изотопов (52)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 63 | B+ | 100% |
| 63 | B+p | 89% |
| 63 | 2p | 0.5% |
| 64 | B+ | — |
| 64 | B+p | — |
| 65 | B+ | 100% |
| 65 | B+p | 87% |
| 66 | B+ | 100% |
| 66 | B+p | — |
| 67 | B+ | 100% |
Факторы рассеяния X‑лучей (506)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 5.20241 |
| 10.1617 | — | 5.36005 |
| 10.3261 | — | 5.52247 |
| 10.4931 | — | 5.63017 |
| 10.6628 | — | 5.66221 |
| 10.8353 | — | 5.69443 |
| 11.0106 | — | 5.71762 |
| 11.1886 | — | 5.72709 |
| 11.3696 | — | 5.73659 |
| 11.5535 | — | 5.7461 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
5×10-2 milligrams per kilogram
Источники (1)
- [5] Selenium https://education.jlab.org/itselemental/ele034.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
2×10-4 milligrams per liter
Источники (1)
- [5] Selenium https://education.jlab.org/itselemental/ele034.html
Production
Production of this element (from raw materials or other compounds containing the element).
Selenium is found in a few rare minerals such as crooksite and clausthalite. In years past it has been obtained from flue dusts remaining from processing copper sulfide ores, but the anode metal from electrolytic copper refineries now provide the source of most of the world's selenium. Selenium is recovered by roasting the mud with soda or sulfuric acid, or by smelting them with soda and niter.
Источники (1)
- [6] Selenium https://periodic.lanl.gov/34.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Selenium.
The element property data was retrieved from publications.