Мышьяк (As)
ПолуметаллТвёрдое тело
Стандартный атомный вес
74.921595 uЭлектронная конфигурация
[Ar] 4s2 3d10 4p3Температура плавления
816.85 °C (1090 K)Температура кипения
613.85 °C (887 K)Плотность
5776 kg/m³Степени окисления
−3, −2, −1, 0, +1, +2, +3, +4, +5Электроотрицательность (Полинг)
2.18Энергия ионизации (1-я)
Год открытия
1250Атомный радиус
115 pmДополнительно
Мышьяк — металлоид группы 15, химически родственный фосфору и сурьме. Он встречается главным образом в сульфидных минералах и в арсенидных или сульфосольных рудах, а не в виде самородного элемента. Его химия определяется степенями окисления +3 и +5, причем среди различных форм существуют важные различия в подвижности и токсичности. Мышьяк полезен в технологическом отношении в малых количествах, особенно в соединениях-полупроводниках, но более известен токсичностью многих своих неорганических соединений.
Элемент представляет собой стально-серое, очень хрупкое, кристаллическое, полуметаллическое твёрдое вещество; на воздухе оно тускнеет, а при нагревании быстро окисляется до мышьяковистого оксида, который пахнет чесноком. Мышьяк и его соединения ядовиты.
Название происходит от латинского arsenicium и греческого arsenikos, означающих «мужской» или «самец», поскольку древние считали, что металлы имеют разные полы. Мышьяк был известен в доисторические времена благодаря своим ядовитым сульфидам. Считается, что немецкий ученый и философ Альберт фон Болльштедт (Альберт Великий, или Альбертус Магнус) получил металл около 1250 года.
Хотя соединения мышьяка добывались древними китайской, греческой и египетской цивилизациями, считается, что сам мышьяк впервые был идентифицирован Альбертусом Магнусом, немецким алхимиком, в 1250 году. Мышьяк встречается в свободном виде в природе, но чаще всего обнаруживается в минералах арсенопирите (FeAsS), реальгаре (AsS) и аурипигменте (As2S3). Сегодня большую часть коммерческого мышьяка получают нагреванием арсенопирита.
От латинского слова arsenicum, греч. arsenikon. Элементарный мышьяк существует в двух твердых модификациях: желтой и серой, или металлической, с удельными плотностями 1,97 и 5,73 соответственно. Считается, что Альбертус Магнус получил этот элемент в 1250 году н. э. В 1649 году Шрёдер опубликовал два метода получения элемента. Миспикель арсенопирит, (FeSAs), является наиболее распространенным минералом, из которого при нагревании мышьяк сублимируется, оставляя сульфид железа.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
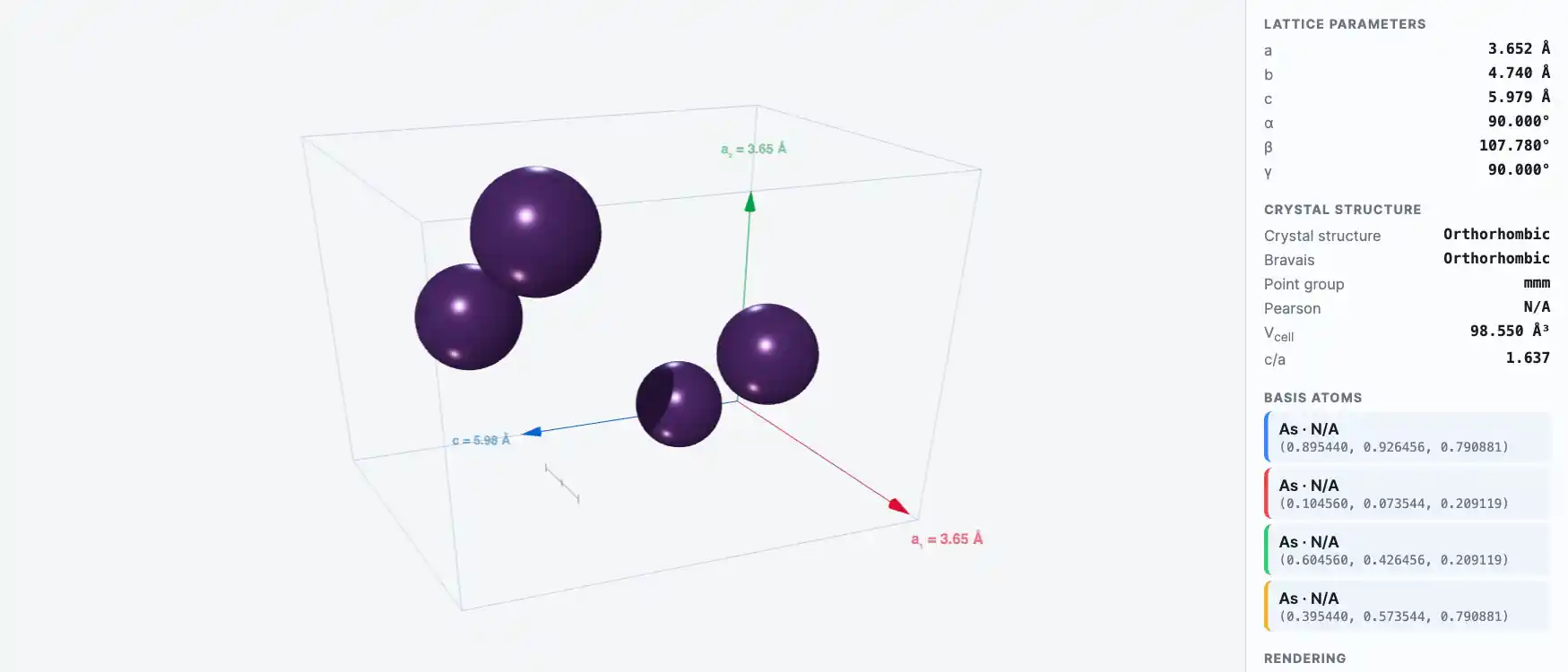
Кристаллическая структура
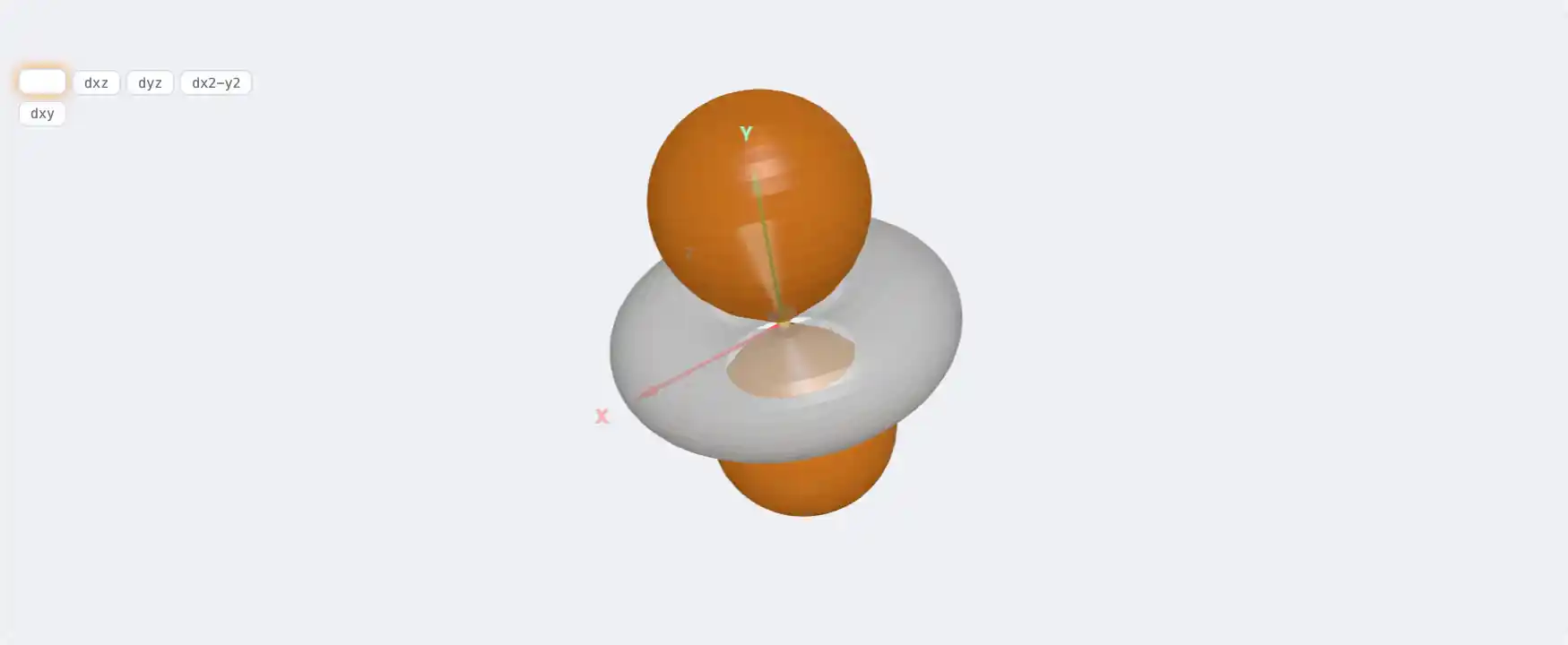
Электронная структура
Идентификаторы
Электронная конфигурация Measured
As: 3d¹⁰ 4s² 4p³[Ar] 3d¹⁰ 4s² 4p³1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p³Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 75 Стабильный | 74,92159457 ± 0,00000095 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 588.9 °C ниже точки сублимации (613.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 33 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| As I | 0 | 52 | 14 | 51 |
| As II | +1 | 86 | 0 | 0 |
| As III | +2 | 14 | 0 | 0 |
| As IV | +3 | 8 | 0 | 0 |
| As V | +4 | 9 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| As I | 0 | 116 |
| As II | +1 | 167 |
| As III | +2 | 22 |
| As IV | +3 | 34 |
| As V | +4 | 9 |
| As VI | +5 | 44 |
| As VII | +6 | 50 |
| As VIII | +7 | 2 |
| As IX | +8 | 2 |
| As X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 57.99999999999999 пм |
| +5 | 4 | N/A | 33.5 пм |
| +5 | 6 | N/A | 46 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 75 Стабильный | 74,92159457 ± 0,00000095 | 100.0000% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1090.15 K |
| Температура кипения | 889.15 K |
| Критическая точка (температура) | 1673.15 K |
| Критическая точка (давление) | 22.3 MPa |
| Тройная точка (температура) | 1090.15 K |
| Тройная точка (давление) | 3700 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (8)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.7217 |
| 2 | p | 3.9264 |
| 2 | s | 8.873 |
| 3 | d | 15.6216 |
| 3 | p | 15.1503 |
| 3 | s | 14.4045 |
| 4 | p | 25.5508 |
| 4 | s | 24.056 |
Детализация кристаллических радиусов (3)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 72 | Ahrens (1952) ionic radius, | |
| 5 | IV | 47.5 | from r^3 vs V plots, | |
| 5 | VI | 60 | calculated, |
Режимы распада изотопов (50)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 60 | p | — |
| 61 | p | — |
| 62 | p | — |
| 63 | p | — |
| 64 | B+ | 100% |
| 64 | B+p | — |
| 65 | B+ | 100% |
| 65 | B+p | — |
| 66 | B+ | 100% |
| 67 | B+ | 100% |
Факторы рассеяния X‑лучей (506)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 4.62596 |
| 10.1617 | — | 4.67742 |
| 10.3261 | — | 4.72945 |
| 10.4931 | — | 4.78206 |
| 10.6628 | — | 4.83525 |
| 10.8353 | — | 4.88904 |
| 11.0106 | — | 4.94342 |
| 11.1886 | — | 4.99841 |
| 11.3696 | — | 5.05401 |
| 11.5535 | — | 5.11023 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.8 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
3.7-3 milligrams per liter
Источники (1)
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Arsenic.
The element property data was retrieved from publications.