Бром (Br)
ГалогенЖидкость
Стандартный атомный вес
79.904 u [79,901, 79,907]Электронная конфигурация
[Ar] 4s2 3d10 4p5Температура плавления
-7.2 °C (265.95 K)Температура кипения
58.8 °C (331.95 K)Плотность
3102.8 kg/m³Степени окисления
−1, +1, +2, +3, +4, +5, +7Электроотрицательность (Полинг)
2.96Энергия ионизации (1-я)
Год открытия
1825Атомный радиус
115 pmДополнительно
Бром — галоген, элемент группы 17, и единственный неметалл, жидкий при комнатной температуре или близкой к ней. Элементарный бром существует как двухатомный Br₂ и представляет собой плотное, летучее, сильно окисляющее вещество. В природе бром встречается главным образом в виде ионов бромида в морской воде, соленых озерах и подземных рассолах. Его химия занимает промежуточное положение между хлором и йодом; он играет важную роль в антипиренах, буровых жидкостях, фармацевтике и фотохимии.
Бром — единственный неметаллический жидкий элемент. Это тяжёлая, подвижная, красновато-бурая жидкость, легко улетучивающаяся при комнатной температуре с образованием красного пара с резким неприятным запахом, напоминающим хлор, и оказывающая сильное раздражающее действие на глаза и горло; он легко растворим в воде или сероуглероде с образованием красного раствора, менее активен, чем хлор, но более активен, чем йод; он легко соединяется со многими элементами и обладает отбеливающим действием; при попадании на кожу вызывает болезненные язвы. Он представляет серьёзную опасность для здоровья, и при работе с ним следует принимать максимальные меры безопасности.
Название происходит от греческого bromos, означающего «дурной запах» или «зловоние». Впервые он был получен немецким химиком Карлом Лёвигом в 1825 году, но впервые публично объявлен в 1826 году французским химиком и фармацевтом Антуаном-Жеромом Баларом, и потому открытие, таким образом, приписывается ему.
Единственный неметаллический элемент, который является жидкостью при обычной комнатной температуре, бром был получен Карлом Лёвигом, молодым студентом-химиком, летом перед началом его первого курса в Гейдельберге. Когда он показал своему профессору, Леопольду Гмелину, красную, дурно пахнущую жидкость, которую он получил, Гмелин понял, что это неизвестное вещество, и побудил Лёвига получить его больше, чтобы можно было подробно изучить его. К сожалению, зимние экзамены и каникулы задержали работу Лёвига настолько, что другой химик, Антуан-Жером Балар, успел опубликовать в 1826 году статью, описывающую новый элемент. Балару было приписано открытие, и он назвал его по греческому слову, означающему зловоние, bromos. Сегодня бром в основном получают обработкой рассолов из скважин в Мичигане и Арканзасе хлором.
От греческого слова bromos, зловоние. Открыт Баларом в 1826 году, но в заметных количествах не получался до 1860 года.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
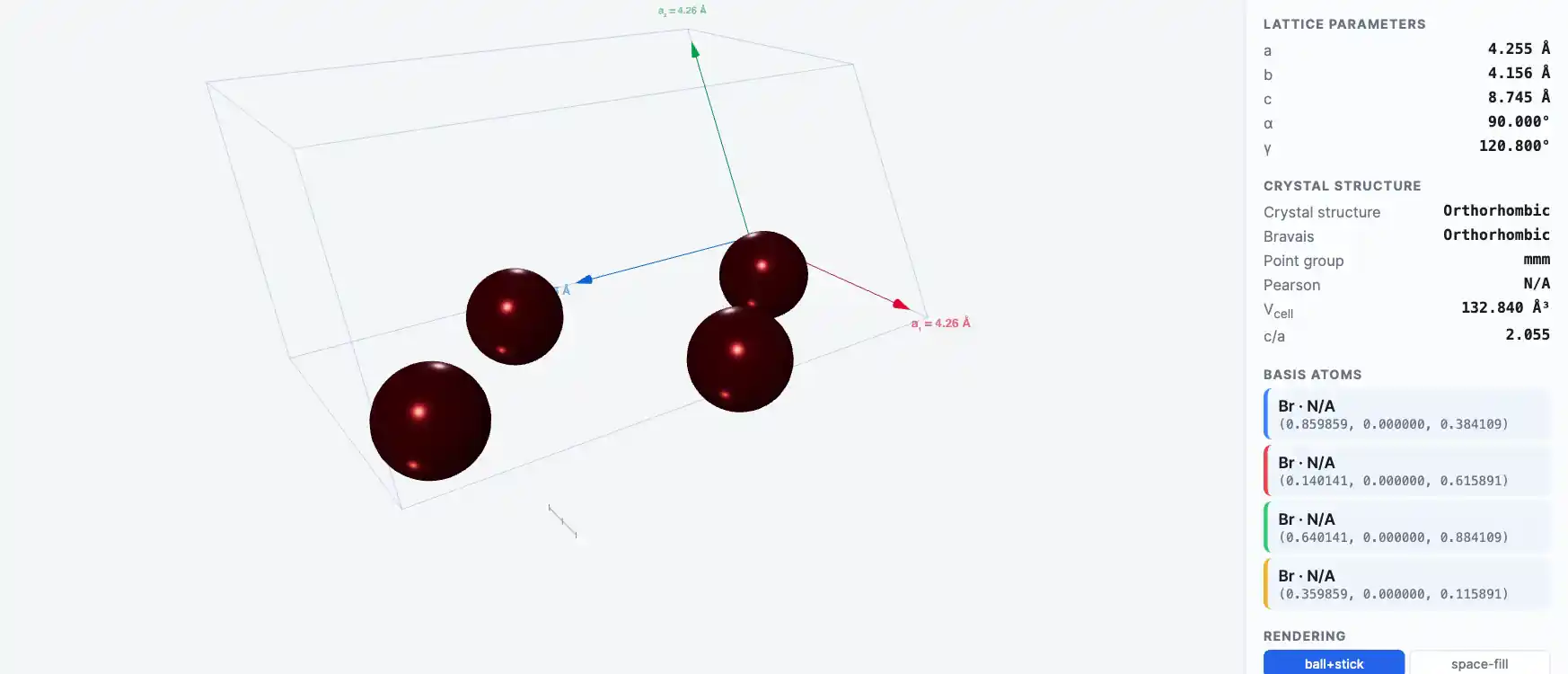
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Br: 3d¹⁰ 4s² 4p⁵[Ar] 3d¹⁰ 4s² 4p⁵1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁵Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 79 Стабильный | 78,9183376 ± 0,0000014 | 50.6900% | Стабильный |
| 81 Стабильный | 80,9162897 ± 0,0000014 | 49.3100% | Стабильный |
Фазовое состояние
Причина: между точкой плавления (-7.2 °C) и точкой кипения (58.8 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Недоступна для жидкой фазы
Дополнительно
Атомные спектры
Показано 10 из 35 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Br I | 0 | 170 | 54 | 170 |
| Br II | +1 | 118 | 3 | 0 |
| Br III | +2 | 75 | 0 | 0 |
| Br IV | +3 | 136 | 0 | 136 |
| Br V | +4 | 22 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Br I | 0 | 265 |
| Br II | +1 | 132 |
| Br III | +2 | 53 |
| Br IV | +3 | 43 |
| Br V | +4 | 10 |
| Br VI | +5 | 12 |
| Br VII | +6 | 6 |
| Br VIII | +7 | 12 |
| Br IX | +8 | 5 |
| Br X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| -1 | 6 | N/A | 196 пм |
| +3 | 4 | N/A | 59 пм |
| +5 | 3 | N/A | 31 пм |
| +7 | 4 | N/A | 25 пм |
| +7 | 6 | N/A | 39 пм |
Соединения
Изотопы (2)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 79 Стабильный | 78,9183376 ± 0,0000014 | 50.6900% ± 0.0700% | Стабильный | stable | |
| 81 Стабильный | 80,9162897 ± 0,0000014 | 49.3100% ± 0.0700% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 265.95 K |
| Температура кипения | 331.95 K |
| Критическая точка (температура) | 588.15 K |
| Критическая точка (давление) | 10.34 MPa |
| Тройная точка (температура) | 265.9 K |
| Тройная точка (давление) | 5.88 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (8)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.7529 |
| 2 | p | 3.9436 |
| 2 | s | 9.3566 |
| 3 | d | 15.4409 |
| 3 | p | 15.4292 |
| 3 | s | 14.7815 |
| 4 | p | 25.972 |
| 4 | s | 24.4472 |
Детализация кристаллических радиусов (5)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| -1 | VI | 182 | Pauling's (1960) crystal radius, | |
| 3 | IVSQ | 73 | ||
| 5 | IIIPY | 45 | ||
| 7 | IV | 39 | ||
| 7 | VI | 53 | Ahrens (1952) ionic radius, |
Режимы распада изотопов (54)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 65 | p | — |
| 66 | p | — |
| 67 | p | — |
| 68 | p | — |
| 69 | p | 100% |
| 70 | B+ | 100% |
| 70 | B+p | — |
| 71 | B+ | 100% |
| 72 | B+ | 100% |
| 73 | B+ | 100% |
Факторы рассеяния X‑лучей (506)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 5.16199 |
| 10.1617 | — | 5.31855 |
| 10.3261 | — | 5.47986 |
| 10.4931 | — | 5.64606 |
| 10.6628 | — | 5.8173 |
| 10.8353 | — | 5.99373 |
| 11.0106 | — | 6.17552 |
| 11.1886 | — | 6.36281 |
| 11.3696 | — | 6.5558 |
| 11.5535 | — | 6.75463 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.4 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
6.73×101 milligrams per liter
Источники (1)
Sources
Sources of this element.
A member of the halogen group, bromine is obtained from natural brines from wells in Michigan and Arkansas. Some bromine is extracted today from seawater, which contains only about 85 ppm.
Источники (1)
- [6] Bromine https://periodic.lanl.gov/35.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
Much of the bromine output in the U.S. was used in the production of ethylene dibromide, a lead scavenger used in making gasoline anti-knock compounds. Lead in gasoline, however, has been drastically reduced due to environmental considerations. This will greatly affect future production of bromine.
Источники (1)
- [6] Bromine https://periodic.lanl.gov/35.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Bromine.
The element property data was retrieved from publications.