Гелий (He)
Благородный газГаз
Стандартный атомный вес
4.002602 uЭлектронная конфигурация
1s2Температура плавления
-272.2 °C (0.95 K)Температура кипения
-268.93 °C (4.22 K)Плотность
0.1785 kg/m³Степени окисления
0Электроотрицательность (Полинг)
N/AЭнергия ионизации (1-я)
Год открытия
1868Атомный радиус
120 pmДополнительно
Гелий — благородный газ и второй элемент периодической таблицы. Он химически инертен в обычных условиях, поскольку его 1s-электронная оболочка заполнена, и существует в виде одноатомного He, а не молекулы. Его низкая плотность, очень низкая температура кипения, высокая теплопроводность и негорючесть делают его технологически важным. На Земле он редко встречается в атмосфере, но может накапливаться в некоторых залежах природного газа в результате радиоактивного распада урана и тория.
Гелий имеет самую низкую температуру плавления среди всех элементов и широко используется в криогенных исследованиях, поскольку его температура кипения близка к абсолютному нулю. Кроме того, этот элемент имеет важное значение в изучении сверхпроводимости.
С использованием жидкого гелия Курти, его сотрудники и другие исследователи сумели получить температуры в несколько микрокельвинов путём адиабатического размагничивания ядер меди.
Гелий обладает и другими необычными свойствами: это единственная жидкость, которую нельзя перевести в твёрдое состояние понижением температуры. При обычных давлениях он остаётся жидким вплоть до абсолютного нуля, но легко затвердевает при повышении давления. Твёрдые 3He и 4He необычны тем, что объём обоих может изменяться более чем на 30% при приложении давления.
Удельная теплоёмкость газообразного гелия необычно высока. Плотность паров гелия при нормальной температуре кипения также очень высока, при этом пар значительно расширяется при нагревании до комнатной температуры. Сосуды, заполненные гелием при 5–10 K, следует рассматривать так, как если бы они содержали жидкий гелий, из-за значительного повышения давления при нагревании газа до комнатной температуры.
Хотя гелий обычно имеет валентность 0, по-видимому, он проявляет слабую тенденцию к соединению с некоторыми другими элементами. Изучались способы получения дифторида гелия, а также исследовались такие частицы, как HeNe и молекулярные ионы He+ и He++.
Название происходит от греческого helios, «солнце». Элемент был обнаружен спектроскопически во время солнечного затмения в хромосфере Солнца французским астрономом Пьером-Жюлем-Сезаром Жансеном в 1868 году. Независимо его открыл и назвал гелием английский астроном Джозеф Норман Локьер.
Считалось, что гелий является только солнечной составляющей, пока позднее шотландский химик Уильям Рамзай в 1895 году не обнаружил, что он идентичен гелию в урановой руде клевеите. Шведские химики Пер Теодор Клеве и Нильс Абрахам Лангет независимо обнаружили гелий в клевеите примерно в то же время.
Гелий, второй по распространенности элемент во Вселенной, был обнаружен на Солнце раньше, чем на Земле. Пьер-Жюль-Сезар Жансен, французский астроном, заметил желтую линию в спектре Солнца, изучая полное солнечное затмение в 1868 году. Сэр Норман Локьер, английский астроном, понял, что эта линия с длиной волны 587,49 нанометра не может быть обусловлена ни одним известным в то время элементом. Было выдвинуто предположение, что за это таинственное желтое излучение отвечает новый элемент на Солнце. Этот неизвестный элемент Локьер назвал гелием. Поиски гелия на Земле завершились в 1895 году. Сэр Уильям Рамзай, шотландский химик, провел эксперимент с минералом, содержащим уран, под названием клевеит. Он обработал клевеит минеральными кислотами и собрал выделившиеся газы. Затем он отправил образец этих газов двум ученым, Локьеру и сэру Уильяму Круксу, которые смогли идентифицировать содержащийся в них гелий. Два шведских химика, Нильс Ланглет и Пер Теодор Клеве, независимо обнаружили гелий в клевеите примерно в то же время, что и Рамзай.
Гелий составляет около 0,0005% атмосферы Земли. Это следовое количество гелия не удерживается Землей гравитационно и постоянно уходит в космическое пространство. Атмосферный гелий Земли пополняется за счет распада радиоактивных элементов в земной коре. Альфа-распад, один из видов радиоактивного распада, приводит к образованию частиц, называемых альфа-частицами. Альфа-частица может стать атомом гелия после того, как захватит два электрона из окружающей среды. Этот вновь образовавшийся гелий со временем может попасть в атмосферу через трещины в коре.
От греческого слова helios — солнце. Жансен получил первые доказательства существования гелия во время солнечного затмения 1868 года, когда обнаружил новую линию в солнечном спектре. Локьер и Франкланд предложили название гелий для нового элемента. В 1895 году Рамзай открыл гелий в урановом минерале клевеите, в то время как примерно в то же время шведские химики Клеве и Ланглет независимо обнаружили его в клевеите. Резерфорд и Ройдс в 1907 году показали, что альфа-частицы являются ядрами гелия.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
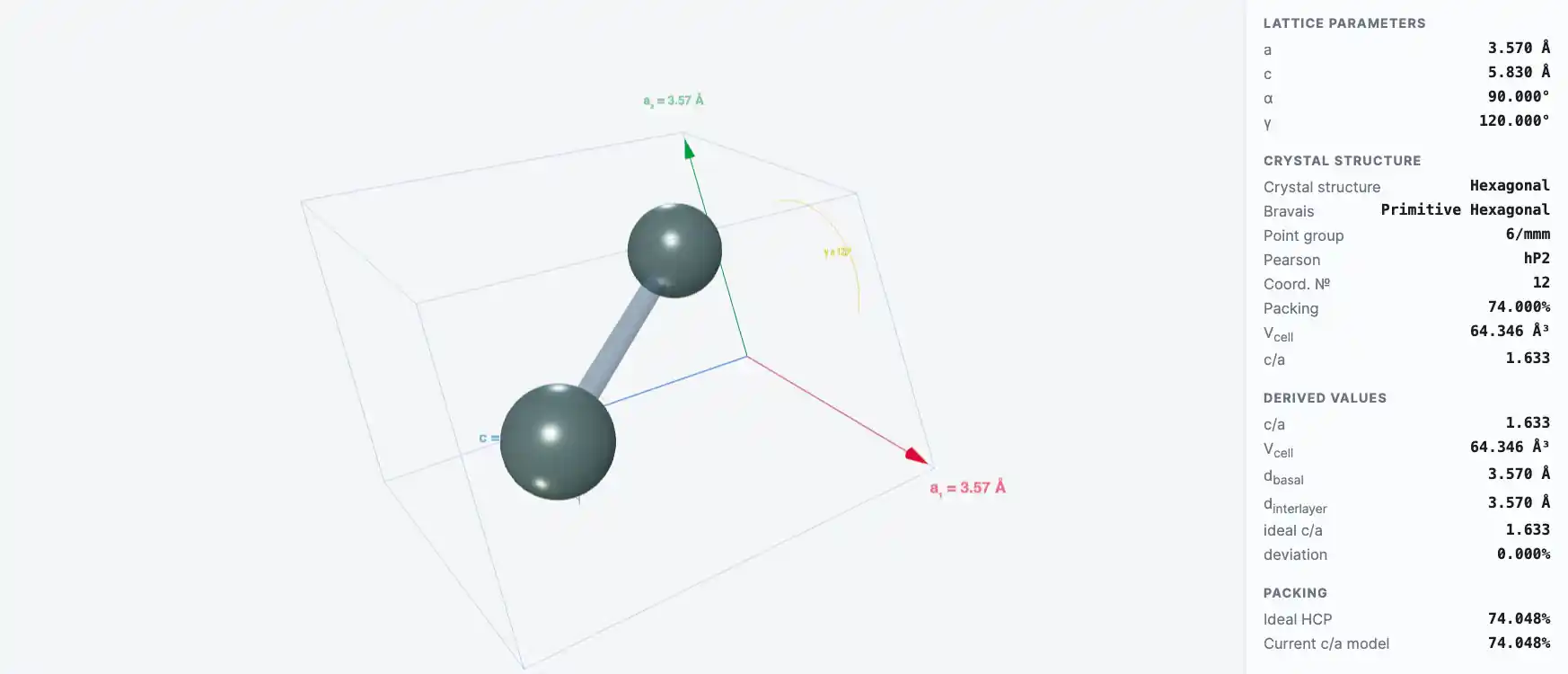
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
He: 1s²1s²1s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 3 Стабильный | 3,0160293201 ± 0,0000000025 | 0.0001% | Стабильный |
| 4 Стабильный | 4,00260325413 ± 0,00000000006 | 99.9999% | Стабильный |
Фазовое состояние
Причина: на 293.9 °C выше точки кипения (-268.93 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Расчёт по уравнению идеального газа при текущей T
Дополнительно
Атомные спектры
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| 3He I Изотоп | 0 | 2289 | 0 | 2289 |
| He I | 0 | 2300 | 2289 | 2300 |
| He II | +1 | 140 | 140 | 140 |
| 3He II Изотоп | +1 | 140 | 140 | 140 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| 3He I Изотоп | 0 | 188 |
| He I | 0 | 843 |
| He II | +1 | 149 |
| 3He II Изотоп | +1 | 149 |
Соединения
Изотопы (2)
Seven isotopes of helium are known: Liquid helium (He-4) exists in two forms: He-4I and He-4II, with a sharp transition point at 2.174K. He-4I (above this temperature) is a normal liquid, but He-4II (below it) is unlike any other known substance. It expands on cooling, its conductivity for heat is enormous, and neither its heat conduction nor viscosity obeys normal rules.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 3 Стабильный | 3,0160293201 ± 0,0000000025 | 0.0001% ± 0.0000% | Стабильный | stable | |
| 4 Стабильный | 4,00260325413 ± 0,00000000006 | 99.9999% ± 0.0000% | Стабильный | stable |
Спектральные линии
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 381.9601975 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 381.9602773 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 381.9602828 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 381.9613129 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 381.9613927 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 381.975731 нм | 1 | He I | emission | 1s.2p 3P* → 1s.6d 3D | Измерено | NIST | |
| 383.3548713 нм | 0 | He I | emission | 1s.2p 1P* → 1s.10d 1D | Измерено | NIST | |
| 383.8100125 нм | N/A | He I | emission | 1s.2p 1P* → 1s.10s 1S | Измерено | NIST | |
| 386.7472343 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6s 3S | Измерено | NIST | |
| 386.7483778 нм | N/A | He I | emission | 1s.2p 3P* → 1s.6s 3S | Измерено | NIST | |
| 386.7631595 нм | 1 | He I | emission | 1s.2p 3P* → 1s.6s 3S | Измерено | NIST | |
| 387.1786406 нм | 1 | He I | emission | 1s.2p 1P* → 1s.9d 1D | Измерено | NIST | |
| 387.8176858 нм | N/A | He I | emission | 1s.2p 1P* → 1s.9s 1S | Измерено | NIST | |
| 388.8604644 нм | N/A | He I | emission | 1s.2s 3S → 1s.3p 3P* | Измерено | NIST | |
| 388.864559 нм | N/A | He I | emission | 1s.2s 3S → 1s.3p 3P* | Измерено | NIST | |
| 388.8648915 нм | N/A | He I | emission | 1s.2s 3S → 1s.3p 3P* | Измерено | NIST | |
| 392.6544387 нм | 1 | He I | emission | 1s.2p 1P* → 1s.8d 1D | Измерено | NIST | |
| 393.5945223 нм | 0 | He I | emission | 1s.2p 1P* → 1s.8s 1S | Измерено | NIST | |
| 396.4728829 нм | 20 | He I | emission | 1s.2s 1S → 1s.4p 1P* | Измерено | NIST | |
| 397.2015454 нм | N/A | He I | emission | 1s.2s 1S → 1s.4d 1D | Измерено | NIST | |
| 400.9256516 нм | 1 | He I | emission | 1s.2p 1P* → 1s.7d 1D | Измерено | NIST | |
| 402.3979795 нм | 1 | He I | emission | 1s.2p 1P* → 1s.7s 1S | Измерено | NIST | |
| 402.6184368 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 402.6185901 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 402.6186005 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 402.619676 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 402.6198294 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 402.6356959 нм | 5 | He I | emission | 1s.2p 3P* → 1s.5d 3D | Измерено | NIST | |
| 412.0810765 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5s 3S | Измерено | NIST | |
| 412.0823747 нм | N/A | He I | emission | 1s.2p 3P* → 1s.5s 3S | Измерено | NIST | |
| 412.0991564 нм | 2 | He I | emission | 1s.2p 3P* → 1s.5s 3S | Измерено | NIST | |
| 414.1332157 нм | N/A | He I | emission | 1s.2p 1P* → 1s.6p 1P* | Измерено | NIST | |
| 414.3759059 нм | 3 | He I | emission | 1s.2p 1P* → 1s.6d 1D | Измерено | NIST | |
| 416.8971512 нм | 1 | He I | emission | 1s.2p 1P* → 1s.6s 1S | Измерено | NIST | |
| 438.3278555 нм | N/A | He I | emission | 1s.2p 1P* → 1s.5p 1P* | Измерено | NIST | |
| 438.7929143 нм | 10 | He I | emission | 1s.2p 1P* → 1s.5d 1D | Измерено | NIST | |
| 443.7553428 нм | 3 | He I | emission | 1s.2p 1P* → 1s.5s 1S | Измерено | NIST | |
| 447.1470373 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 447.1474077 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 447.1474317 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 447.1485658 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 447.1489362 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 447.1683251 нм | 25 | He I | emission | 1s.2p 3P* → 1s.4d 3D | Измерено | NIST | |
| 468.537685 нм | N/A | He II | emission | 3p 2P* → 4d 2D | Измерено | NIST | |
| 468.5407226 нм | N/A | He II | emission | 3s 2S → 4p 2P* | Измерено | NIST | |
| 468.5524404 нм | N/A | He II | emission | 3p 2P* → 4s 2S | Измерено | NIST | |
| 468.5568006 нм | N/A | He II | emission | 3s 2S → 4p 2P* | Измерено | NIST | |
| 468.570385 нм | N/A | He II | emission | 3d 2D → 4f 2F* | Измерено | NIST | |
| 468.570438 нм | N/A | He II | emission | 3p 2P* → 4d 2D | Измерено | NIST | |
| 468.575708 нм | N/A | He II | emission | 3d 2D → 4p 2P* | Измерено | NIST | |
| 468.5757975 нм | N/A | He II | emission | 3p 2P* → 4d 2D | Измерено | NIST | |
| 468.5804092 нм | N/A | He II | emission | 3d 2D → 4f 2F* | Измерено | NIST | |
| 468.583089 нм | N/A | He II | emission | 3d 2D → 4f 2F* | Измерено | NIST | |
| 468.5884123 нм | N/A | He II | emission | 3d 2D → 4p 2P* | Измерено | NIST | |
| 468.5905553 нм | N/A | He II | emission | 3p 2P* → 4s 2S | Измерено | NIST | |
| 468.5917885 нм | N/A | He II | emission | 3d 2D → 4p 2P* | Измерено | NIST | |
| 471.3139173 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4s 3S | Измерено | NIST | |
| 471.3156155 нм | N/A | He I | emission | 1s.2p 3P* → 1s.4s 3S | Измерено | NIST | |
| 471.3375684 нм | 4 | He I | emission | 1s.2p 3P* → 1s.4s 3S | Измерено | NIST | |
| 491.074748 нм | N/A | He I | emission | 1s.2p 1P* → 1s.4p 1P* | Измерено | NIST | |
| 492.0612726 нм | N/A | He I | emission | 1s.2p 1P* → 1s.4f 1F* | Измерено | NIST | |
| 492.1931036 нм | 20 | He I | emission | 1s.2p 1P* → 1s.4d 1D | Измерено | NIST | |
| 501.567801 нм | 100 | He I | emission | 1s.2s 1S → 1s.3p 1P* | Измерено | NIST | |
| 504.208749 нм | N/A | He I | emission | 1s.2s 1S → 1s.3d 1D | Измерено | NIST | |
| 504.773857 нм | 10 | He I | emission | 1s.2p 1P* → 1s.4s 1S | Измерено | NIST | |
| 587.443388 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 1D | Измерено | NIST | |
| 587.446026 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 1D | Измерено | NIST | |
| 587.559871 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 587.561397 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 587.561484 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 587.56251 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 587.564036 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 587.596628 нм | 100 | He I | emission | 1s.2p 3P* → 1s.3d 3D | Измерено | NIST | |
| 655.976872 нм | N/A | He II | emission | 4p 2P* → 6d 2D | Измерено | NIST | |
| 655.979395 нм | N/A | He II | emission | 4s 2S → 6p 2P* | Измерено | NIST | |
| 655.98544 нм | N/A | He II | emission | 4p 2P* → 6s 2S | Измерено | NIST | |
| 655.988733 нм | N/A | He II | emission | 4s 2S → 6p 2P* | Измерено | NIST | |
| 656.005227 нм | N/A | He II | emission | 4d 2D → 6f 2F* | Измерено | NIST | |
| 656.005274 нм | N/A | He II | emission | 4p 2P* → 6d 2D | Измерено | NIST | |
| 656.008318 нм | N/A | He II | emission | 4d 2D → 6p 2P* | Измерено | NIST | |
| 656.008387 нм | N/A | He II | emission | 4p 2P* → 6d 2D | Измерено | NIST | |
| 656.01416 нм | N/A | He II | emission | 4f 2F* → 6g 2G | Измерено | NIST | |
| 656.014176 нм | N/A | He II | emission | 4d 2D → 6f 2F* | Измерено | NIST | |
| 656.015708 нм | N/A | He II | emission | 4f 2F* → 6d 2D | Измерено | NIST | |
| 656.015732 нм | N/A | He II | emission | 4d 2D → 6f 2F* | Измерено | NIST | |
| 656.016955 нм | N/A | He II | emission | 4p 2P* → 6s 2S | Измерено | NIST | |
| 656.017657 нм | N/A | He II | emission | 4d 2D → 6p 2P* | Измерено | NIST | |
| 656.018478 нм | N/A | He II | emission | 4f 2F* → 6g 2G | Измерено | NIST | |
| 656.01882 нм | N/A | He II | emission | 4f 2F* → 6d 2D | Измерено | NIST | |
| 656.018823 нм | N/A | He II | emission | 4d 2D → 6p 2P* | Измерено | NIST | |
| 656.019412 нм | N/A | He II | emission | 4f 2F* → 6g 2G | Измерено | NIST | |
| 656.02096 нм | N/A | He II | emission | 4f 2F* → 6d 2D | Измерено | NIST | |
| 663.190187 нм | N/A | He I | emission | 1s.2p 1P* → 1s.3p 1P* | Измерено | NIST | |
| 667.815174 нм | 100 | He I | emission | 1s.2p 1P* → 1s.3d 1D | Измерено | NIST | |
| 667.967687 нм | N/A | He I | emission | 1s.2p 1P* → 1s.3d 3D | Измерено | NIST | |
| 706.517716 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3s 3S | Измерено | NIST | |
| 706.521532 нм | N/A | He I | emission | 1s.2p 3P* → 1s.3s 3S | Измерено | NIST | |
| 706.570863 нм | 30 | He I | emission | 1s.2p 3P* → 1s.3s 3S | Измерено | NIST | |
| 716.055563 нм | N/A | He I | emission | 1s.3s 3S → 1s.10p 3P* | Измерено | NIST | |
| 716.055907 нм | N/A | He I | emission | 1s.3s 3S → 1s.10p 3P* | Измерено | NIST | |
| 716.055935 нм | N/A | He I | emission | 1s.3s 3S → 1s.10p 3P* | Измерено | NIST | |
| 728.13508 нм | 50 | He I | emission | 1s.2p 1P* → 1s.3s 1S | Измерено | NIST | |
| 729.803204 нм | N/A | He I | emission | 1s.3s 3S → 1s.9p 3P* | Измерено | NIST | |
| 729.803696 нм | N/A | He I | emission | 1s.3s 3S → 1s.9p 3P* | Измерено | NIST | |
| 729.803736 нм | N/A | He I | emission | 1s.3s 3S → 1s.9p 3P* | Измерено | NIST | |
| 749.984714 нм | N/A | He I | emission | 1s.3s 3S → 1s.8p 3P* | Измерено | NIST | |
| 749.985457 нм | N/A | He I | emission | 1s.3s 3S → 1s.8p 3P* | Измерено | NIST | |
| 749.985518 нм | N/A | He I | emission | 1s.3s 3S → 1s.8p 3P* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Риск поставок и экономика
Свойства инертного газа
Фазовые переходы и аллотропы
| Температура кипения | 4.22 K |
| Критическая точка (температура) | 5.19 K |
| Критическая точка (давление) | 0.23 MPa |
| Тройная точка (температура) | 2.18 K |
| Тройная точка (давление) | 5.04 kPa |
Расширенные справочные данные
Константы экранирования (1)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.3125 |
Режимы распада изотопов (9)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 5 | n | 100% |
| 6 | B- | 100% |
| 6 | B-d | 0% |
| 7 | n | 100% |
| 8 | B- | 100% |
| 8 | B-n | 16% |
| 8 | B-t | 0.9% |
| 9 | n | 100% |
| 10 | 2n | 100% |
Факторы рассеяния X‑лучей (501)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0 |
| 10.1617 | — | 0 |
| 10.3261 | — | 0 |
| 10.4931 | — | 0 |
| 10.6628 | — | 0 |
| 10.8353 | — | 0 |
| 11.0106 | — | 0 |
| 11.1886 | — | 0 |
| 11.3696 | — | 0 |
| 11.5535 | — | 0 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
8×10-3 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
7×10-6 milligrams per liter
Источники (1)
Sources
Sources of this element.
Except for hydrogen, helium is the most abundant element found in the universe. Helium is extracted from natural gas. In fact, all natural gas contains at least trace quantities of helium.
It has been detected spectroscopically in great abundance, especially in the hotter stars, and it is an important component in both the proton-proton reaction and the carbon cycle, which account for the energy of the sun and stars.
The helium content of the atmosphere is about 1 part in 200,000. While it is present in various radioactive minerals as a decay product, the bulk of the Free World's supply is obtained from wells in Texas, Oklahoma, and Kansas. Outside the United States, the only known helium extraction plants, in 1984 were in Eastern Europe (Poland), the USSR, and a few in India.
Источники (1)
- [6] Helium https://periodic.lanl.gov/2.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Helium.
The element property data was retrieved from publications.