Водород (H)
НеметаллГаз
Стандартный атомный вес
1.008 u [1,00784, 1,00811]Электронная конфигурация
1s1Температура плавления
-259.34 °C (13.81 K)Температура кипения
-252.87 °C (20.28 K)Плотность
0.08988 kg/m³Степени окисления
−1, +1Электроотрицательность (Полинг)
2.2Энергия ионизации (1-я)
Год открытия
1766Атомный радиус
25 pmДополнительно
Самый легкий химический элемент, водород, расположен над щелочными металлами, но при обычных условиях является неметаллом. Его единственный протон и один электрон делают его простейшим атомом и отправной точкой для значительной части химии. На Земле он обычно связан в воде и органическом веществе, тогда как в промышленности используется как химическое сырье, восстановитель, топливо и носитель энергии.
Бесцветный, без запаха газообразный химический элемент. Легчайший и наиболее распространённый элемент во Вселенной. Содержится в воде и во всех органических соединениях. Химически реагирует с большинством элементов. Открыт Генри Кавендишем в 1776 году.
Название происходит от греческих hydro, означающего «вода», и genes, «образующий», поскольку он при горении в воздухе образует воду. Водород был открыт английским физиком Генри Кавендишем в 1766 году.
Ученые производили водород в течение многих лет до того, как его признали элементом. Письменные источники указывают, что Роберт Бойль получал водород уже в 1671 году, экспериментируя с железом и кислотами. Водород был впервые признан отдельным элементом Генри Кавендишем в 1766 году. Состоящий из одного протона и одного электрона, водород является простейшим и самым распространенным элементом во Вселенной. Оценивается, что 90% видимой Вселенной состоит из водорода.
Водород — это сырьевой топливный материал, который большинство звезд «сжигают» для получения энергии. Тот же процесс, известный как термоядерный синтез, изучается как возможный источник энергии для использования на Земле. Ожидается, что запасов водорода на Солнце хватит еще на 5 миллиардов лет.
От греческого слова hydro (вода) и genes (образующий). Водород был признан отдельным веществом Генри Кавендишем в 1776 году. Схема простого атома водорода.
Водород — самый распространенный из всех элементов во Вселенной. Более тяжелые элементы первоначально были образованы из атомов водорода или из других элементов, которые первоначально были образованы из атомов водорода.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
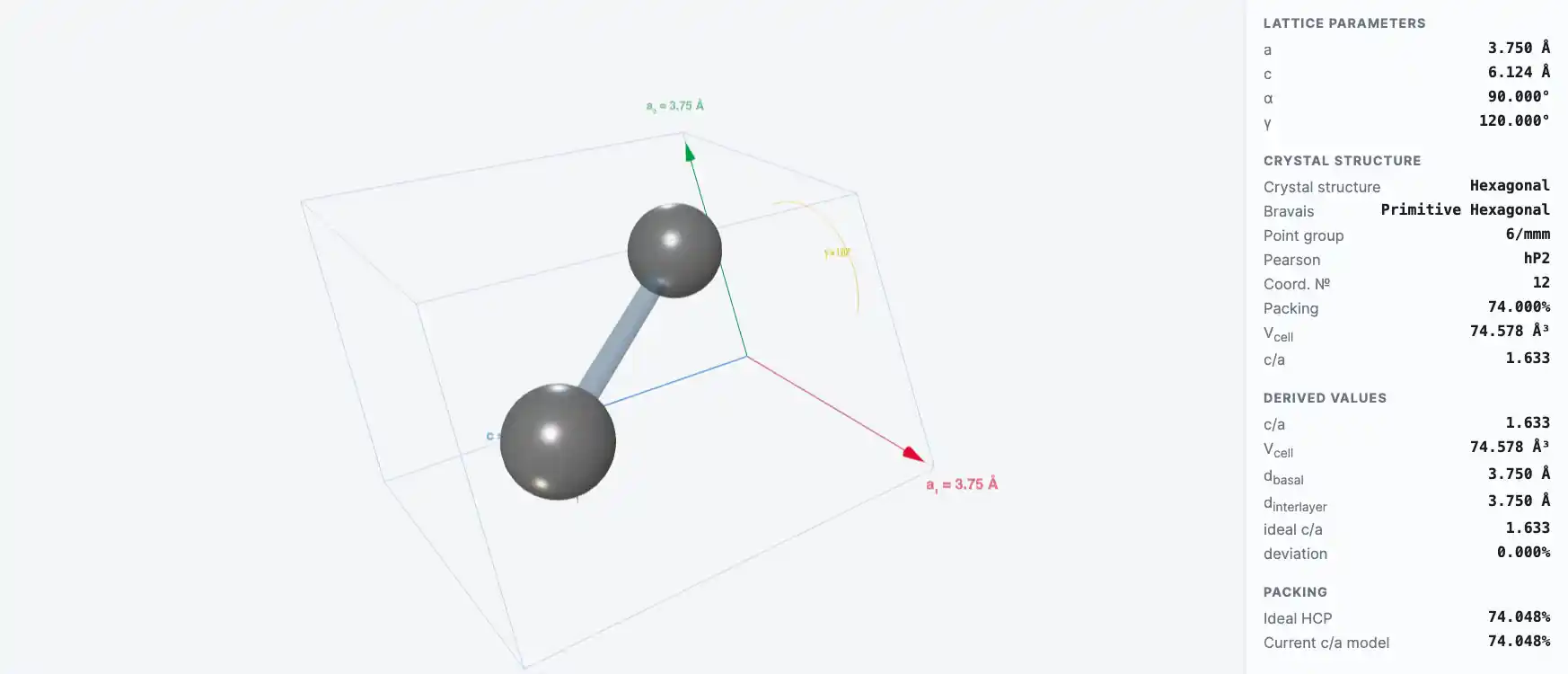
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
H: 1s¹1s¹1s¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 1 Стабильный | 1,00782503223 ± 0,00000000009 | 99.9885% | Стабильный |
| 2 Стабильный | 2,01410177812 ± 0,00000000012 | 0.0115% | Стабильный |
Фазовое состояние
Причина: на 277.9 °C выше точки кипения (-252.87 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Расчёт по уравнению идеального газа при текущей T
Дополнительно
Атомные спектры
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| D I Изотоп | 0 | 364 | 161 | 341 |
| H I | 0 | 568 | 441 | 535 |
| T I Изотоп | 0 | 11 | 11 | 11 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| D I Изотоп | 0 | 78 |
| H I | 0 | 106 |
| T I Изотоп | 0 | 10 |
Соединения
Изотопы (2)
Обычный изотоп водорода, H, известен как протий; два других изотопа — дейтерий (протон и нейтрон) и тритий (протон и два нейтрона). Водород — единственный элемент, изотопы которого получили разные названия. Дейтерий и тритий используются как топливо в термоядерных реакторах. Один атом дейтерия приходится примерно на 6000 обычных атомов водорода.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 1 Стабильный | 1,00782503223 ± 0,00000000009 | 99.9885% ± 0.0070% | Стабильный | stable | |
| 2 Стабильный | 2,01410177812 ± 0,00000000012 | 0.0115% ± 0.0070% | Стабильный | stable |
Спектральные линии
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 383.5355892 нм | N/A | H I | emission | 2p 2P* → 9d 2D | Измерено | NIST | |
| 383.5356424 нм | N/A | H I | emission | 2p 2P* → 9s 2S | Измерено | NIST | |
| 383.53587 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 383.5361082 нм | N/A | H I | emission | 2s 2S → 9p 2P* | Измерено | NIST | |
| 383.5361616 нм | N/A | H I | emission | 2s 2S → 9s 2S | Измерено | NIST | |
| 383.5361673 нм | N/A | H I | emission | 2s 2S → 9p 2P* | Измерено | NIST | |
| 383.53839 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 383.53909 нм | 30000 | H I | emission | 2 → 9 | Измерено | NIST | |
| 383.5409535 нм | N/A | H I | emission | 2p 2P* → 9d 2D | Измерено | NIST | |
| 383.54096 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 383.5409732 нм | N/A | H I | emission | 2p 2P* → 9d 2D | Измерено | NIST | |
| 383.5410263 нм | N/A | H I | emission | 2p 2P* → 9s 2S | Измерено | NIST | |
| 388.9019815 нм | N/A | H I | emission | 2p 2P* → 8d 2D | Измерено | NIST | |
| 388.9020595 нм | N/A | H I | emission | 2p 2P* → 8s 2S | Измерено | NIST | |
| 388.90227 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 388.9024865 нм | N/A | H I | emission | 2s 2S → 8d 2D | Измерено | NIST | |
| 388.9025152 нм | N/A | H I | emission | 2s 2S → 8p 2P* | Измерено | NIST | |
| 388.9025154 нм | N/A | H I | emission | 2s 2S → 8d 2D | Измерено | NIST | |
| 388.9025933 нм | N/A | H I | emission | 2s 2S → 8s 2S | Измерено | NIST | |
| 388.9026017 нм | N/A | H I | emission | 2s 2S → 8p 2P* | Измерено | NIST | |
| 388.90486 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 388.90557 нм | 70000 | H I | emission | 2 → 8 | Измерено | NIST | |
| 388.9074883 нм | N/A | H I | emission | 2p 2P* → 8d 2D | Измерено | NIST | |
| 388.90749 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 388.9075172 нм | N/A | H I | emission | 2p 2P* → 8d 2D | Измерено | NIST | |
| 388.9075951 нм | N/A | H I | emission | 2p 2P* → 8s 2S | Измерено | NIST | |
| 397.0041763 нм | N/A | H I | emission | 2p 2P* → 7d 2D | Измерено | NIST | |
| 397.0042976 нм | N/A | H I | emission | 2p 2P* → 7s 2S | Измерено | NIST | |
| 397.00448 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 397.0047325 нм | N/A | H I | emission | 2s 2S → 7p 2P* | Измерено | NIST | |
| 397.0048539 нм | N/A | H I | emission | 2s 2S → 7s 2S | Измерено | NIST | |
| 397.004867 нм | N/A | H I | emission | 2s 2S → 7p 2P* | Измерено | NIST | |
| 397.00719 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 397.00788 нм | 30000 | H I | emission | 2 → 7 | Измерено | NIST | |
| 397.0099002 нм | N/A | H I | emission | 2p 2P* → 7d 2D | Измерено | NIST | |
| 397.00991 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 397.009945 нм | N/A | H I | emission | 2p 2P* → 7d 2D | Измерено | NIST | |
| 397.0100663 нм | N/A | H I | emission | 2p 2P* → 7s 2S | Измерено | NIST | |
| 410.1702284 нм | N/A | H I | emission | 2p 2P* → 6d 2D | Измерено | NIST | |
| 410.1704339 нм | N/A | H I | emission | 2p 2P* → 6s 2S | Измерено | NIST | |
| 410.17056 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 410.1707462 нм | N/A | H I | emission | 2s 2S → 6d 2D | Измерено | NIST | |
| 410.1708218 нм | N/A | H I | emission | 2s 2S → 6p 2P* | Измерено | NIST | |
| 410.1710277 нм | N/A | H I | emission | 2s 2S → 6s 2S | Измерено | NIST | |
| 410.1710499 нм | N/A | H I | emission | 2s 2S → 6p 2P* | Измерено | NIST | |
| 410.17346 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 410.17415 нм | 70000 | H I | emission | 2 → 6 | Измерено | NIST | |
| 410.17631 нм | N/A | H I | emission | 2p 2P* → 6d 2D | Измерено | NIST | |
| 410.17632 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 410.176386 нм | N/A | H I | emission | 2p 2P* → 6d 2D | Измерено | NIST | |
| 410.1765915 нм | N/A | H I | emission | 2p 2P* → 6s 2S | Измерено | NIST | |
| 434.0426937 нм | N/A | H I | emission | 2p 2P* → 5d 2D | Измерено | NIST | |
| 434.04309 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 434.0430904 нм | N/A | H I | emission | 2p 2P* → 5s 2S | Измерено | NIST | |
| 434.0433568 нм | N/A | H I | emission | 2s 2S → 5p 2P* | Измерено | NIST | |
| 434.0437554 нм | N/A | H I | emission | 2s 2S → 5s 2S | Измерено | NIST | |
| 434.0437982 нм | N/A | H I | emission | 2s 2S → 5p 2P* | Измерено | NIST | |
| 434.04634 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 434.0471 нм | 90000 | H I | emission | 2 → 5 | Измерено | NIST | |
| 434.0494419 нм | N/A | H I | emission | 2p 2P* → 5d 2D | Измерено | NIST | |
| 434.04947 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 434.0495889 нм | N/A | H I | emission | 2p 2P* → 5d 2D | Измерено | NIST | |
| 434.0499857 нм | N/A | H I | emission | 2p 2P* → 5s 2S | Измерено | NIST | |
| 486.1278624 нм | N/A | H I | emission | 2p 2P* → 4d 2D | Измерено | NIST | |
| 486.1283363 нм | N/A | H I | emission | 2s 2S → 4d 2D | Измерено | NIST | |
| 486.12841 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 486.1286949 нм | N/A | H I | emission | 2s 2S → 4p 2P* | Измерено | NIST | |
| 486.128837 нм | N/A | H I | emission | 2p 2P* → 4s 2S | Измерено | NIST | |
| 486.1296711 нм | N/A | H I | emission | 2s 2S → 4s 2S | Измерено | NIST | |
| 486.1297761 нм | N/A | H I | emission | 2s 2S → 4p 2P* | Измерено | NIST | |
| 486.1325 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 486.1333 нм | 180000 | H I | emission | 2 → 4 | Измерено | NIST | |
| 486.1361516 нм | N/A | H I | emission | 2p 2P* → 4d 2D | Измерено | NIST | |
| 486.13622 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 486.1365118 нм | N/A | H I | emission | 2p 2P* → 4d 2D | Измерено | NIST | |
| 486.1374864 нм | N/A | H I | emission | 2p 2P* → 4s 2S | Измерено | NIST | |
| 656.27097 нм | N/A | H I | emission | 2p 2P* → 3d 2D | Измерено | NIST | |
| 656.2714 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.2722 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.272483 нм | N/A | H I | emission | 2s 2S → 3p 2P* | Измерено | NIST | |
| 656.275181 нм | N/A | H I | emission | 2p 2P* → 3s 2S | Измерено | NIST | |
| 656.276701 нм | N/A | H I | emission | 2s 2S → 3s 2S | Измерено | NIST | |
| 656.277 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.277153 нм | N/A | H I | emission | 2s 2S → 3p 2P* | Измерено | NIST | |
| 656.2795 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.2819 нм | 500000 | H I | emission | 2 → 3 | Измерено | NIST | |
| 656.285177 нм | N/A | H I | emission | 2p 2P* → 3d 2D | Измерено | NIST | |
| 656.28533 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.2854 нм | N/A | H I | emission | N/A | Измерено | NIST | |
| 656.286734 нм | N/A | H I | emission | 2p 2P* → 3d 2D | Измерено | NIST | |
| 656.290944 нм | N/A | H I | emission | 2p 2P* → 3s 2S | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Фазовые переходы и аллотропы
| Температура плавления | 13.99 K |
| Температура кипения | 20.27 K |
| Критическая точка (температура) | 32.94 K |
| Критическая точка (давление) | 1.29 MPa |
| Тройная точка (температура) | 13.8 K |
| Тройная точка (давление) | 7.04 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (1)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0 |
Детализация кристаллических радиусов (2)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 1 | I | -24 | ||
| 1 | II | -4 |
Режимы распада изотопов (6)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 3 | B- | 100% |
| 4 | n | 100% |
| 5 | 2n | 100% |
| 6 | n | — |
| 6 | 3n | — |
| 7 | 2n | — |
Факторы рассеяния X‑лучей (501)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0 |
| 10.1617 | — | 0 |
| 10.3261 | — | 0 |
| 10.4931 | — | 0 |
| 10.6628 | — | 0 |
| 10.8353 | — | 0 |
| 11.0106 | — | 0 |
| 11.1886 | — | 0 |
| 11.3696 | — | 0 |
| 11.5535 | — | 0 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.40×103 milligrams per kilogram
Источники (1)
- [5] Hydrogen https://education.jlab.org/itselemental/ele001.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.08×105 milligrams per liter
Источники (1)
- [5] Hydrogen https://education.jlab.org/itselemental/ele001.html
Sources
Sources of this element.
Hydrogen is estimated to make up more than 90% of all the atoms three quarters of the mass of the universe! This element is found in the stars, and plays an important part in powering the universe through both the proton-proton reaction and carbon-nitrogen cycle. Stellar hydrogen fusion processes release massive amounts of energy by combining hydrogens to form helium.
Production of hydrogen in the U.S. alone amounts to about 3 billion cubic feet per year. Hydrogen is prepared by
▸ steam on heated carbon,
▸ decomposition of certain hydrocarbons with heat,
▸ reaction of sodium or potassium hydroxide on aluminum
▸ electrolysis of water, or
▸ displacement from acids by certain metals.
Liquid hydrogen is important in cryogenics and in the study of superconductivity, as its melting point is only 20 degrees above absolute zero.
Tritium is readily produced in nuclear reactors and is used in the production of the hydrogen bomb.
Hydrogen is the primary component of Jupiter and the other gas giant planets. At some depth in the planet's interior the pressure is so great that solid molecular hydrogen is converted to solid metallic hydrogen.
In 1973, a group of Russian experimenters may have produced metallic hydrogen at a pressure of 2.8 Mbar. At the transition the density changed from 1.08 to 1.3 g/cm3. Earlier, in 1972, at Livermore, California, a group also reported on a similar experiment in which they observed a pressure-volume point centered at 2 Mbar. Predictions say that metallic hydrogen may be metastable; others have predicted it would be a superconductor at room temperature.
Источники (1)
- [6] Hydrogen https://periodic.lanl.gov/1.shtml
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
Measurements of relative 2H abundances are used to determine the breeding grounds of many species of migrant songbirds. These species of songbirds only grow their feathers before migration, and they grow them on or close to their breeding grounds. Therefore, the isotopic composition of a bird’s feathers correlates to the isotopic composition of the growing season’s precipitation [18] [18] Z. D. Sharp, V. Atudorei, H. O. Panarello, J. Fernández, C. Douthitt. J. Archaeolog. Sci.30, 1709 (2003).[18] Z. D. Sharp, V. Atudorei, H. O. Panarello, J. Fernández, C. Douthitt. J. Archaeolog. Sci.30, 1709 (2003)., [19] [19] K. A. Hobson. Oecologia120, 314 (1999).[19] K. A. Hobson. Oecologia120, 314 (1999)., [20] [20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996).[20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996)..
Measurements of relative 2H abundances of human hair samples collected at archeological sites are used to determine the geographic region in which a subject lived based on the hydrogen isotopic composition of the water they drank. This is possible because hair stores a daily record of the hydrogen isotopic composition of intake water, which correlates to local meteoric water [18] [18] Z. D. Sharp, V. Atudorei, H. O. Panarello, J. Fernández, C. Douthitt. J. Archaeolog. Sci.30, 1709 (2003).[18] Z. D. Sharp, V. Atudorei, H. O. Panarello, J. Fernández, C. Douthitt. J. Archaeolog. Sci.30, 1709 (2003)., [21] [21] T. B. Coplen, H. Qi. Forensic Sci. Int.266, 222 (2016).[21] T. B. Coplen, H. Qi. Forensic Sci. Int.266, 222 (2016)..
Источники (5)
- [18] Z. D. Sharp, V. Atudorei, H. O. Panarello, J. Fernández, C. Douthitt. J. Archaeolog. Sci.30, 1709 (2003).
- [19] K. A. Hobson. Oecologia120, 314 (1999).
- [20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996).
- [21] T. B. Coplen, H. Qi. Forensic Sci. Int.266, 222 (2016).
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Hydrogen.
The element property data was retrieved from publications.