Хлор (Cl)
ГалогенГаз
Стандартный атомный вес
35.45 u [35,446, 35,457]Электронная конфигурация
[Ne] 3s2 3p5Температура плавления
-101.5 °C (171.65 K)Температура кипения
-34.04 °C (239.11 K)Плотность
3.214 kg/m³Степени окисления
−1, +1, +2, +3, +4, +5, +6, +7Электроотрицательность (Полинг)
3.16Энергия ионизации (1-я)
Год открытия
1774Атомный радиус
100 pmДополнительно
Хлор — это реакционноспособный галоген и жёлто-зелёный двухатомный газ Cl₂ в обычных условиях. Он является сильным окислителем и в природе встречается главным образом в виде хлоридных солей, особенно в морской воде и минералах эвапоритов. Химия хлора имеет центральное значение для дезинфекции воды, неорганических хлоридов, хлорированных растворителей, полимеров и многих промышленных процессов окисления и замещения. Элемент имеет два стабильных изотопа, ³⁵Cl и ³⁷Cl.
Он относится к группе галогенов (солеобразующих) элементов и получают его из хлоридов действием окислителей, а чаще электролизом; это зеленовато-жёлтый газ, непосредственно соединяющийся почти со всеми элементами. При 10°C один объём воды растворяет 3.10 объёма хлора, при 30°C — только 1.77 объёма.
Название происходит от греческого chloros, означающего «бледно-зеленый» или «зеленовато-желтый» цвет элемента. Он был открыт шведским аптекарем и химиком Карлом-Вильгельмом Шееле в 1774 году. В 1810 году английский химик Хамфри Дэви доказал, что это элемент.
Поскольку хлор непосредственно соединяется почти с каждым элементом, в природе он никогда не встречается в свободном виде. Хлор впервые был получен Карлом Вильгельмом Шееле, шведским химиком, когда он соединил минерал пиролюзит (MnO2) с соляной кислотой (HCl) в 1774 году. Хотя Шееле считал, что полученный в его эксперименте газ содержит кислород, сэр Хамфри Дэви в 1810 году доказал, что это на самом деле отдельный элемент. Сегодня большую часть хлора получают путем электролиза водного раствора хлорида натрия (NaCl).
От греческого слова chloro, зеленовато-желтый. Открыт в 1774 году Шееле, который считал, что он содержит кислород. Хлор был назван в 1810 году Дэви, который настаивал, что это элемент.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
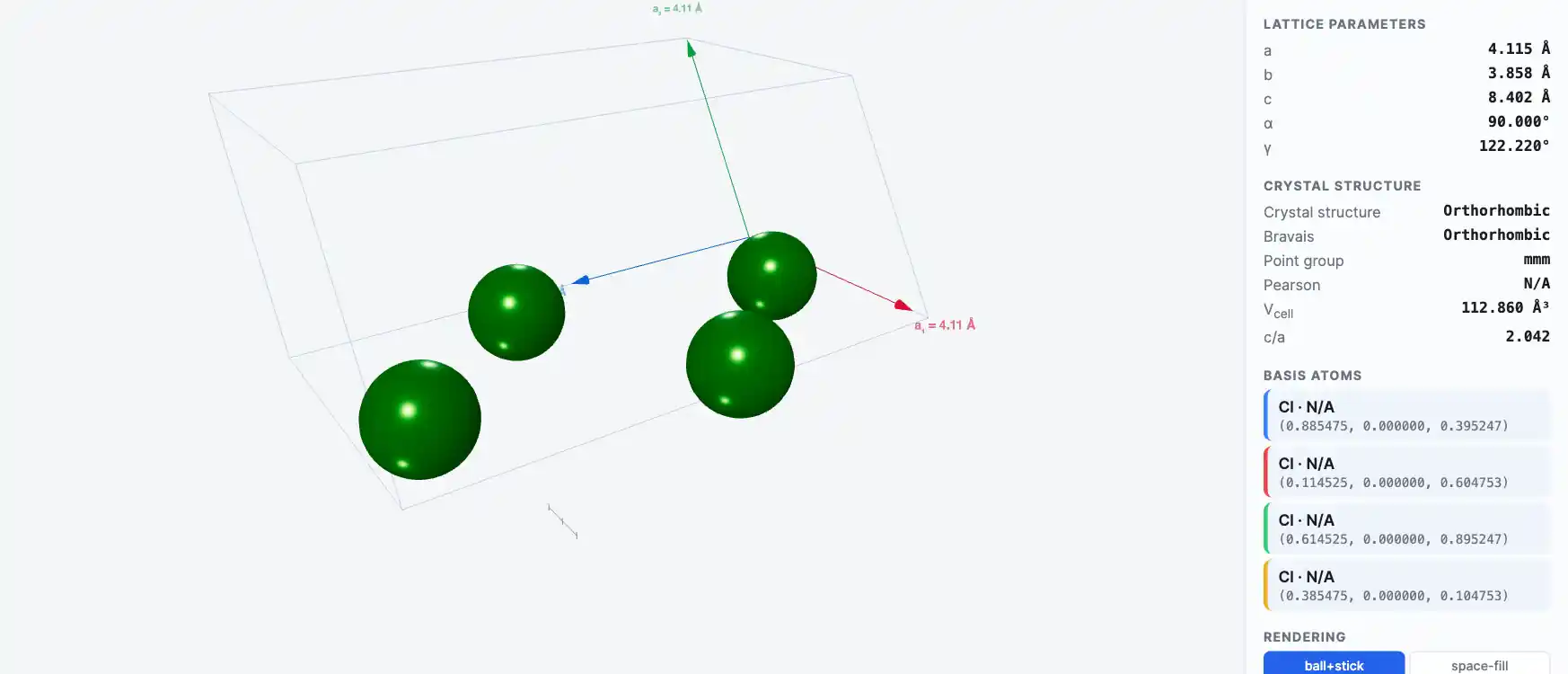
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Cl: 3s² 3p⁵[Ne] 3s² 3p⁵1s² 2s² 2p⁶ 3s² 3p⁵Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 35 Стабильный | 34,968852682 ± 0,000000037 | 75.7600% | Стабильный |
| 37 Стабильный | 36,965902602 ± 0,000000055 | 24.2400% | Стабильный |
Фазовое состояние
Причина: на 59.0 °C выше точки кипения (-34.04 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Расчёт по уравнению идеального газа при текущей T
Дополнительно
Атомные спектры
Показано 10 из 17 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Cl I | 0 | 221 | 99 | 100 |
| Cl II | +1 | 292 | 221 | 221 |
| Cl III | +2 | 192 | 166 | 166 |
| Cl IV | +3 | 73 | 42 | 45 |
| Cl V | +4 | 27 | 6 | 6 |
| Cl VI | +5 | 1 | 1 | 1 |
| Cl VII | +6 | 28 | 28 | 28 |
| Cl VIII | +7 | 5 | 5 | 5 |
| Cl IX | +8 | 3 | 3 | 3 |
| Cl X | +9 | 11 | 11 | 11 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Cl I | 0 | 379 |
| Cl II | +1 | 275 |
| Cl III | +2 | 83 |
| Cl IV | +3 | 41 |
| Cl V | +4 | 29 |
| Cl VI | +5 | 67 |
| Cl VII | +6 | 47 |
| Cl VIII | +7 | 29 |
| Cl IX | +8 | 57 |
| Cl X | +9 | 15 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| -1 | 6 | N/A | 181 пм |
| +5 | 3 | N/A | 12 пм |
| +7 | 4 | N/A | 8 пм |
| +7 | 6 | N/A | 27 пм |
Соединения
Изотопы (2)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 35 Стабильный | 34,968852682 ± 0,000000037 | 75.7600% ± 0.1000% | Стабильный | stable | |
| 37 Стабильный | 36,965902602 ± 0,000000055 | 24.2400% ± 0.1000% | Стабильный | stable |
Спектральные линии
Показано 50 из 207 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 479.4556 нм | 99000 | Cl II | emission | 3s2.3p3.(4S*).4s 5S* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 542.3257 нм | 99000 | Cl II | emission | 3s2.3p3.(4S*).3d 5D* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 489.6783 нм | 81000 | Cl II | emission | 3s2.3p3.(2D*).4s 3D* → 3s2.3p3.(2D*).4p 3F | Измерено | NIST | |
| 521.7945 нм | 56000 | Cl II | emission | 3s2.3p3.(4S*).4s 3S* → 3s2.3p3.(4S*).4p 3P | Измерено | NIST | |
| 490.4776 нм | 47000 | Cl II | emission | 3s2.3p3.(2D*).4s 3D* → 3s2.3p3.(2D*).4p 3F | Измерено | NIST | |
| 481.007 нм | 29000 | Cl II | emission | 3s2.3p3.(4S*).4s 5S* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 491.773 нм | 26000 | Cl II | emission | 3s2.3p3.(2D*).4s 3D* → 3s2.3p3.(2D*).4p 3F | Измерено | NIST | |
| 507.8267 нм | 26000 | Cl II | emission | 3s2.3p3.(2D*).4s 3D* → 3s2.3p3.(2D*).4p 3D | Измерено | NIST | |
| 386.0828 нм | 25000 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 522.1362 нм | 23000 | Cl II | emission | 3s2.3p3.(4S*).4s 3S* → 3s2.3p3.(4S*).4p 3P | Измерено | NIST | |
| 544.3375 нм | 19000 | Cl II | emission | 3s2.3p3.(4S*).3d 5D* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 481.948 нм | 16000 | Cl II | emission | 3s2.3p3.(4S*).4s 5S* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 539.2125 нм | 15000 | Cl II | emission | 3s2.3p3.(2D*).4s 1D* → 3s2.3p3.(2D*).4p 1F | Измерено | NIST | |
| 478.132 нм | 13000 | Cl II | emission | 3s2.3p3.(2P*).4s 3P* → 3s2.3p3.(2P*).4p 3D | Измерено | NIST | |
| 385.0988 нм | 10000 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 499.5473 нм | 10000 | Cl II | emission | 3s2.3p3.(2D*).3d 3F* → 3s2.3p3.(2D*).4p 3D | Измерено | NIST | |
| 542.3516 нм | 10000 | Cl II | emission | 3s2.3p3.(4S*).3d 5D* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 544.4217 нм | 10000 | Cl II | emission | 3s2.3p3.(4S*).3d 5D* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 385.1374 нм | 7900 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 725.6618 нм | 7500 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).4p 4S* | Измерено | NIST | |
| 545.7037 нм | 5600 | Cl II | emission | 3s2.3p3.(4S*).3d 5D* → 3s2.3p3.(4S*).4p 5P | Измерено | NIST | |
| 741.4118 нм | 5000 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).4p 2P* | Измерено | NIST | |
| 386.099 нм | 4400 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 476.8651 нм | 4300 | Cl II | emission | 3s2.3p3.(2P*).4s 3P* → 3s2.3p3.(2P*).4p 3D | Измерено | NIST | |
| 384.5639 нм | 3900 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 384.5362 нм | 3100 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 380.5174 нм | 1900 | Cl II | emission | 3s2.3p3.(2D*).4p 3D → 3s2.3p3.(2D*).4d 3F* | Измерено | NIST | |
| 609.468 нм | 1900 | Cl II | emission | 3s2.3p3.(2D*).4s 1D* → 3s2.3p3.(2D*).4p 1P | Измерено | NIST | |
| 384.5788 нм | 1500 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 391.3866 нм | 1500 | Cl II | emission | 3s2.3p3.(2D*).4p 3F → 3s2.3p3.(2D*).4d 3F* | Измерено | NIST | |
| 380.9459 нм | 1300 | Cl II | emission | 3s2.3p3.(2D*).4p 3D → 3s2.3p3.(2D*).4d 3F* | Измерено | NIST | |
| 385.1651 нм | 1200 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 391.6632 нм | 1100 | Cl II | emission | 3s2.3p3.(2D*).4p 3F → 3s2.3p3.(2D*).4d 3F* | Измерено | NIST | |
| 386.1378 нм | 1000 | Cl II | emission | 3s2.3p3.(4S*).4p 5P → 3s2.3p3.(4S*).4d 5D* | Измерено | NIST | |
| 399.1367 нм | 700 | Cl III | emission | 3s2.3p2.(3P).3d 4P → 3s2.3p2.(3P).4p 4P* | Измерено | NIST | |
| 401.8351 нм | 600 | Cl III | emission | 3s2.3p2.(3P).3d 4P → 3s2.3p2.(3P).4p 4P* | Измерено | NIST | |
| 405.893 нм | 600 | Cl III | emission | 3s2.3p2.(3P).3d 4P → 3s2.3p2.(3P).4p 4P* | Измерено | NIST | |
| 410.4082 нм | 500 | Cl III | emission | 3s2.3p2.(3P).3d 4P → 3s2.3p2.(3P).4p 4P* | Измерено | NIST | |
| 410.6764 нм | 500 | Cl III | emission | 3s2.3p2.(3P).3d 4P → 3s2.3p2.(3P).4p 4P* | Измерено | NIST | |
| 436.3268 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4D* | Измерено | NIST | |
| 436.9498 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 2D* | Измерено | NIST | |
| 437.9896 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4D* | Измерено | NIST | |
| 438.9751 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4D* | Измерено | NIST | |
| 443.8488 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4P* | Измерено | NIST | |
| 452.6182 нм | 100 | Cl I | emission | 3s2.3p4.(3P).4s 2P → 3s2.3p4.(3P).5p 2P* | Измерено | NIST | |
| 439.0403 нм | 90 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4D* | Измерено | NIST | |
| 440.302 нм | 90 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 4P* | Измерено | NIST | |
| 447.5304 нм | 90 | Cl I | emission | 3s2.3p4.(3P).4s 4P → 3s2.3p4.(3P).5p 2D* | Измерено | NIST | |
| 460.0977 нм | 80 | Cl I | emission | 3s2.3p4.(3P).4s 2P → 3s2.3p4.(3P).5p 2P* | Измерено | NIST | |
| 466.1208 нм | 80 | Cl I | emission | 3s2.3p4.(3P).4s 2P → 3s2.3p4.(3P).5p 2P* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 171.65 K |
| Температура кипения | 239.11 K |
| Критическая точка (температура) | 417.05 K |
| Критическая точка (давление) | 7.99 MPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (5)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.4761 |
| 2 | p | 4.0068 |
| 2 | s | 5.5696 |
| 3 | p | 10.8839 |
| 3 | s | 9.9317 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| -1 | VI | 167 | Pauling's (1960) crystal radius, | |
| 5 | IIIPY | 26 | ||
| 7 | IV | 22 | ||
| 7 | VI | 41 | Ahrens (1952) ionic radius, |
Режимы распада изотопов (45)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 28 | p | 100% |
| 29 | p | 100% |
| 30 | p | 100% |
| 31 | B+ | 100% |
| 31 | B+p | 2.4% |
| 32 | B+ | 100% |
| 32 | B+A | 0.1% |
| 32 | B+p | 0% |
| 33 | B+ | 100% |
| 34 | B+ | 100% |
Факторы рассеяния X‑лучей (504)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.46938 |
| 10.1617 | — | 1.6922 |
| 10.3261 | — | 1.9488 |
| 10.4931 | — | 2.24432 |
| 10.6628 | — | 2.51303 |
| 10.8353 | — | 2.73153 |
| 11.0106 | — | 2.95549 |
| 11.1886 | — | 3.19416 |
| 11.3696 | — | 3.48881 |
| 11.5535 | — | 3.87618 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.45×102 milligrams per kilogram
Источники (1)
- [5] Chlorine https://education.jlab.org/itselemental/ele017.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.94×104 milligrams per liter
Источники (1)
- [5] Chlorine https://education.jlab.org/itselemental/ele017.html
Sources
Sources of this element.
In nature it is found in the combined state only, chiefly with sodium as common salt (NaCl), carnallite, and sylvite.
Источники (1)
- [6] Chlorine https://periodic.lanl.gov/17.shtml
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
Analyses of chlorine isotopes and other environmental tracers can help to identify whether an environmental contaminant is of anthropogenic origin or naturally occurring. For example, perchlorate (ClO4 -) can be of anthropogenic origin and is also found naturally. Perchlorate is a widespread groundwater contaminant that can interfere with hormone production in the thyroid gland by displacing iodide. Both the stable chlorine isotope-amount ratio n(37Cl)/n(35Cl) and the mole fraction of 36Cl, n(36Cl)/n(Cl), can provide useful information about origins of perchlorate in the environment (Fig. IUPAC.17.2). Such information may be important for legal reasons and for remediation of contaminated areas [152] [152] M. A. Stewart, A. J. Spivack. Rev. Mineral. Geochem.55, 231 (2004).[152] M. A. Stewart, A. J. Spivack. Rev. Mineral. Geochem.55, 231 (2004).[152] M. A. Stewart, A. J. Spivack. Rev. Mineral. Geochem.55, 231 (2004).[152] M. A. Stewart, A. J. Spivack. Rev. Mineral. Geochem.55, 231 (2004)., [153] [153] J. K. Böhlke, N. C. Sturchio, B. Gu, J. Horita, G. M. Brown, W. A. Jackson, J. R. Batista, P. B. Hatzinger. Anal. Chem.77, 7838 (2005).[153] J. K. Böhlke, N. C. Sturchio, B. Gu, J. Horita, G. M. Brown, W. A. Jackson, J. R. Batista, P. B. Hatzinger. Anal. Chem.77, 7838 (2005)..
Источники (4)
- [152] M. A. Stewart, A. J. Spivack. Rev. Mineral. Geochem.55, 231 (2004).
- [153] J. K. Böhlke, N. C. Sturchio, B. Gu, J. Horita, G. M. Brown, W. A. Jackson, J. R. Batista, P. B. Hatzinger. Anal. Chem.77, 7838 (2005).
- [154] J. K. Böhlke, P. Hatzinger, N. C. Sturchio, B. Gu, I. J. Abbene, S. J. Mroczkowski. Environ. Sci. Technol.43, 5619 (2009).
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Chlorine.
The element property data was retrieved from publications.