Кислород (O)
НеметаллГаз
Стандартный атомный вес
15.999 u [15,99903, 15,99977]Электронная конфигурация
[He] 2s2 2p4Температура плавления
-218.79 °C (54.36 K)Температура кипения
-182.95 °C (90.2 K)Плотность
1.429 kg/m³Степени окисления
−2, −1, 0, +1, +2Электроотрицательность (Полинг)
3.44Энергия ионизации (1-я)
Год открытия
1771Атомный радиус
60 pmДополнительно
Кислород — реакционноспособный неметалл и халькоген, встречающийся главным образом в виде двухатомного газа O₂ и, реже, в виде озона O₃. Он необходим для аэробного дыхания и является основным компонентом воды, силикатных минералов, карбонатов и многих биологических молекул. Его высокая электроотрицательность и способность образовывать прочные связи делают окислительную химию центральной для горения, коррозии, метаболизма и промышленной переработки.
Газ бесцветен, не имеет запаха и вкуса. Жидкая и твёрдая формы имеют бледно-голубой цвет и являются сильно парамагнитными.
Название происходит от греческих слов oxys — «кислый» и genes — «образующий», поскольку французский химик Антуан-Лоран Лавуазье когда-то считал, что кислород является обязательной составной частью всех кислот.
Кислород был независимо открыт шведским аптекарем и химиком Карлом-Вильгельмом Шееле в 1771 году и английским священником и химиком Джозефом Пристли в 1774 году. «Химический трактат о воздухе и огне» Шееле был опубликован лишь в 1777 году, поэтому заслуга открытия приписывается Пристли, поскольку он опубликовал результаты первым.
Кислород был получен несколькими химиками ещё до его открытия в 1774 году, однако они не распознали его как отдельный элемент. Джозеф Пристли и Карл Вильгельм Шееле оба независимо открыли кислород, но обычно открытие приписывают Пристли. Оба смогли получить кислород нагреванием оксида ртути (HgO). Пристли называл газ, полученный в его опытах, «дефлогистированным воздухом», а Шееле — «огненным воздухом». Название «кислород» было введено Антуаном Лавуазье, который ошибочно считал, что кислород необходим для образования всех кислот. Кислород является третьим по распространённости элементом во Вселенной и составляет почти 21% атмосферы Земли. На кислород приходится почти половина массы земной коры, две трети массы человеческого тела и девять десятых массы воды. Большие количества кислорода могут быть извлечены из сжиженного воздуха с помощью процесса, известного как фракционная перегонка. Кислород также можно получить путём электролиза воды или нагреванием хлората калия (KClO3).
От греческого слова oxys — кислый, и genes — образующий. Поведение кислорода и азота как компонентов воздуха привело к развитию теории флогистона горения, которая на столетие захватила умы химиков.
Джозефу Пристли обычно приписывают его открытие, хотя Шееле также открыл его независимо.
Его атомный вес использовался в качестве эталона сравнения для всех других элементов до 1961 года, когда Международный союз теоретической и прикладной химии принял углерод-12 в качестве новой основы.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
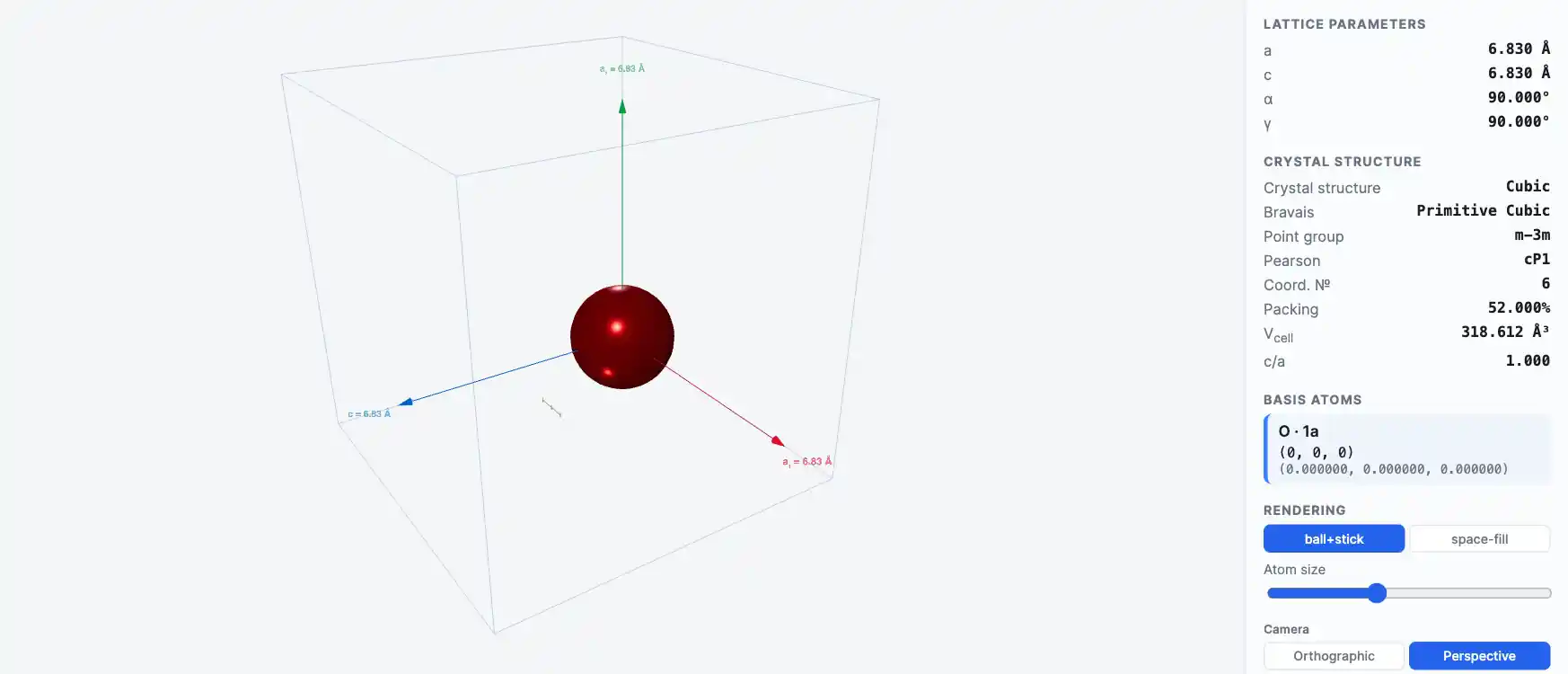
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
O: 2s² 2p⁴[He] 2s² 2p⁴1s² 2s² 2p⁴Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 16 Стабильный | 15,99491461957 ± 0,00000000017 | 99.7570% | Стабильный |
| 17 Стабильный | 16,9991317565 ± 0,00000000069 | 0.0380% | Стабильный |
| 18 Стабильный | 17,99915961286 ± 0,00000000076 | 0.2050% | Стабильный |
Фазовое состояние
Причина: на 207.9 °C выше точки кипения (-182.95 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Плотность
При нормальных условиях
Расчёт по уравнению идеального газа при текущей T
Дополнительно
Атомные спектры
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| O I | 0 | 910 | 854 | 907 |
| O II | +1 | 1630 | 876 | 1630 |
| O III | +2 | 1005 | 974 | 974 |
| O IV | +3 | 1525 | 1521 | 1523 |
| O V | +4 | 391 | 385 | 385 |
| O VI | +5 | 157 | 126 | 157 |
| O VII | +6 | 189 | 188 | 189 |
| O VIII | +7 | 137 | 137 | 137 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| O I | 0 | 614 |
| O II | +1 | 287 |
| O III | +2 | 188 |
| O IV | +3 | 219 |
| O V | +4 | 172 |
| O VI | +5 | 148 |
| O VII | +6 | 149 |
| O VIII | +7 | 149 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| -2 | 2 | N/A | 135 пм |
| -2 | 3 | N/A | 136 пм |
| -2 | 4 | N/A | 138 пм |
| -2 | 6 | N/A | 140 пм |
| -2 | 8 | N/A | 142 пм |
Соединения
Изотопы (3)
Oxygen has nine isotopes. Natural oxygen is a mixture of three isotopes.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 16 Стабильный | 15,99491461957 ± 0,00000000017 | 99.7570% ± 0.0160% | Стабильный | stable | |
| 17 Стабильный | 16,9991317565 ± 0,00000000069 | 0.0380% ± 0.0010% | Стабильный | stable | |
| 18 Стабильный | 17,99915961286 ± 0,00000000076 | 0.2050% ± 0.0140% | Стабильный | stable |
Спектральные линии
Показано 50 из 1013 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 615.8187 нм | 490 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).4d 5D* | Измерено | NIST | |
| 615.6778 нм | 450 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).4d 5D* | Измерено | NIST | |
| 700.223 нм | 450 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).4d 3D* | Измерено | NIST | |
| 725.4448 нм | 450 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).5s 3S* | Измерено | NIST | |
| 615.5971 нм | 400 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).4d 5D* | Измерено | NIST | |
| 645.5977 нм | 400 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).5s 5S* | Измерено | NIST | |
| 725.4154 нм | 400 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).5s 3S* | Измерено | NIST | |
| 645.4444 нм | 360 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).5s 5S* | Измерено | NIST | |
| 700.1922 нм | 360 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).4d 3D* | Измерено | NIST | |
| 645.3602 нм | 320 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).5s 5S* | Измерено | NIST | |
| 725.4531 нм | 320 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).5s 3S* | Измерено | NIST | |
| 715.6701 нм | 210 | O I | emission | 2s2.2p3.(2D*).3s 1D* → 2s2.2p3.(2D*).3p 1D | Измерено | NIST | |
| 396.1573 нм | 200 | O III | emission | 2s2.2p.(2P*).3p 1D → 2s2.2p.(2P*).3d 1F* | Измерено | NIST | |
| 533.0741 нм | 190 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).5d 5D* | Измерено | NIST | |
| 604.6438 нм | 190 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).6s 3S* | Измерено | NIST | |
| 394.72949 нм | 185 | O I | emission | 2s2.2p3.(4S*).3s 5S* → 2s2.2p3.(4S*).4p 5P | Измерено | NIST | |
| 394.74813 нм | 160 | O I | emission | 2s2.2p3.(4S*).3s 5S* → 2s2.2p3.(4S*).4p 5P | Измерено | NIST | |
| 532.9681 нм | 160 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).5d 5D* | Измерено | NIST | |
| 604.6233 нм | 160 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).6s 3S* | Измерено | NIST | |
| 394.75862 нм | 140 | O I | emission | 2s2.2p3.(4S*).3s 5S* → 2s2.2p3.(4S*).4p 5P | Измерено | NIST | |
| 543.6862 нм | 135 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).6s 5S* | Измерено | NIST | |
| 559.789 нм | 130 | O V | emission | 1s2.2s.3p 3P* → 1s2.2s.3d 3D | Измерено | NIST | |
| 650.024 нм | 130 | O V | emission | 1s2.2p.(2P*<3/2>).3p 3D → 1s2.2p.(2P*<3/2>).3d 3F* | Измерено | NIST | |
| 382.34136 нм | 120 | O I | emission | 2s2.2p3.(2D*).3s 3D* → 2s2.2p3.(2P*).3p 3D | Измерено | NIST | |
| 557.7339 нм | 120 | O I | emission | 2s2.2p4 1D → 2s2.2p4 1S | Измерено | NIST | |
| 543.5775 нм | 110 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).6s 5S* | Измерено | NIST | |
| 559.2252 нм | 110 | O III | emission | 2s2.2p.(2P*).3s 1P* → 2s2.2p.(2P*).3p 1P | Измерено | NIST | |
| 604.6495 нм | 110 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(4S*).6s 3S* | Измерено | NIST | |
| 395.46067 нм | 100 | O I | emission | 2s2.2p3.(4S*).3p 3P → 2s2.2p3.(2P*).3s 3P* | Измерено | NIST | |
| 412.396 нм | 100 | O V | emission | 1s2.2p.(2P*<3/2>).3s 3P* → 1s2.2p.(2P*<3/2>).3p 3D | Измерено | NIST | |
| 436.8258 нм | 100 | O I | emission | 2s2.2p3.(4S*).3s 3S* → 2s2.2p3.(4S*).4p 3P | Измерено | NIST | |
| 543.5178 нм | 90 | O I | emission | 2s2.2p3.(4S*).3p 5P → 2s2.2p3.(4S*).6s 5S* | Измерено | NIST | |
| 423.3274 нм | 80 | O I | emission | 2s2.2p3.(4S*).4p 3P → 2s2.2p3.(2D*<3/2>).3d 3P* | Измерено | NIST | |
| 441.4899 нм | 27 | O II | emission | 2s2.2p2.(3P).3s 2P → 2s2.2p2.(3P).3p 2D* | Измерено | NIST | |
| 672.1388 нм | 26 | O II | emission | 2s2.2p2.(3P).3s 2P → 2s2.2p2.(3P).3p 2S* | Измерено | NIST | |
| 441.6975 нм | 25 | O II | emission | 2s2.2p2.(3P).3s 2P → 2s2.2p2.(3P).3p 2D* | Измерено | NIST | |
| 397.3256 нм | 24 | O II | emission | 2s2.2p2.(3P).3s 2P → 2s2.2p2.(3P).3p 2P* | Измерено | NIST | |
| 407.58617 нм | 24 | O II | emission | 2s2.2p2.(3P).3p 4D* → 2s2.2p2.(3P).3d 4F | Измерено | NIST | |
| 464.91347 нм | 24 | O II | emission | 2s2.2p2.(3P).3s 4P → 2s2.2p2.(3P).3p 4D* | Измерено | NIST | |
| 664.1031 нм | 24 | O II | emission | 2s2.2p2.(3P).3s 2P → 2s2.2p2.(3P).3p 2S* | Измерено | NIST | |
| 407.21525 нм | 23 | O II | emission | 2s2.2p2.(3P).3p 4D* → 2s2.2p2.(3P).3d 4F | Измерено | NIST | |
| 434.9426 нм | 23 | O II | emission | 2s2.2p2.(3P).3s 4P → 2s2.2p2.(3P).3p 4P* | Измерено | NIST | |
| 411.92165 нм | 22 | O II | emission | 2s2.2p2.(3P).3p 4P* → 2s2.2p2.(3P).3d 4D | Измерено | NIST | |
| 459.0974 нм | 22 | O II | emission | 2s2.2p2.(1D).3s 2D → 2s2.2p2.(1D).3p 2F* | Измерено | NIST | |
| 464.18103 нм | 22 | O II | emission | 2s2.2p2.(3P).3s 4P → 2s2.2p2.(3P).3p 4D* | Измерено | NIST | |
| 689.5102 нм | 22 | O II | emission | 2s2.2p2.(3P).3d 4F → 2s2.2p2.(3P).4p 4D* | Измерено | NIST | |
| 406.98819 нм | 21 | O II | emission | 2s2.2p2.(3P).3p 4D* → 2s2.2p2.(3P).3d 4F | Измерено | NIST | |
| 435.126 нм | 21 | O II | emission | 2s2.2p2.(1D).3s 2D → 2s2.2p2.(1D).3p 2D* | Измерено | NIST | |
| 466.16324 нм | 21 | O II | emission | 2s2.2p2.(3P).3s 4P → 2s2.2p2.(3P).3p 4D* | Измерено | NIST | |
| 470.5346 нм | 21 | O II | emission | 2s2.2p2.(3P).3p 2D* → 2s2.2p2.(3P).3d 2F | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Фазовые переходы и аллотропы
| Температура плавления | 54.36 K |
| Температура кипения | 90.19 K |
| Критическая точка (температура) | 154.58 K |
| Критическая точка (давление) | 5.04 MPa |
| Тройная точка (температура) | 54.36 K |
| Тройная точка (давление) | 0.15 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (3)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.3421 |
| 2 | p | 3.5468 |
| 2 | s | 3.5084 |
Детализация кристаллических радиусов (5)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| -2 | II | 121 | ||
| -2 | III | 122 | ||
| -2 | IV | 124 | ||
| -2 | VI | 126 | ||
| -2 | VIII | 128 |
Режимы распада изотопов (22)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 11 | 2p | 100% |
| 12 | 2p | 100% |
| 13 | B+ | 100% |
| 13 | B+p | 10.9% |
| 14 | B+ | 100% |
| 15 | B+ | 100% |
| 19 | B- | 100% |
| 20 | B- | 100% |
| 21 | B- | 100% |
| 21 | B-n | — |
Факторы рассеяния X‑лучей (502)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.70328 |
| 10.1617 | — | 0.70723 |
| 10.3261 | — | 0.70738 |
| 10.4931 | — | 0.70753 |
| 10.6628 | — | 0.70768 |
| 10.8353 | — | 0.70783 |
| 11.0106 | — | 0.70798 |
| 11.1886 | — | 0.70813 |
| 11.3696 | — | 0.70828 |
| 11.5535 | — | 0.70843 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
4.61×105 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
8.57×105 milligrams per liter
Источники (1)
Sources
Sources of this element.
Oxygen is the third most abundant element found in the sun, and it plays a part in the carbon-nitrogen cycle, the process once thought to give the sun and stars their energy. Oxygen under excited conditions is responsible for the bright red and yellow-green colors of the Aurora Borealis.
A gaseous element, oxygen forms 21% of the atmosphere by volume and is obtained by liquefaction and fractional distillation. The atmosphere of Mars contains about 0.15% oxygen. The element and its compounds make up 49.2%, by weight, of the earth's crust. About two thirds of the human body and nine tenths of water is oxygen.
In the laboratory it can be prepared by the electrolysis of water or by heating potassium chlorate with manganese dioxide as a catalyst.
Источники (1)
- [6] Oxygen https://periodic.lanl.gov/8.shtml
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
Measurements of relative 18O abundances have been used to determine the breeding grounds of many species of migrant songbirds. These species of songbirds only grow their feathers before migration, and they grow them on or close to their breeding grounds. Therefore, the isotopic composition of a bird’s feathers correlates to the isotopic signature of the growing season’s precipitation [19] [19] K. A. Hobson. Oecologia120, 314 (1999).[19] K. A. Hobson. Oecologia120, 314 (1999)., [20] [20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996).[20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996)..
Measurements of relative 18O abundances of human hair or nail samples collected at archeological sites have been used to determine the geographic region in which a subject lived based on the oxygen isotopic composition of the water they drank (Fig. IUPAC.8.3). This is possible because hair stores a daily record of oxygen isotopic composition of intake water, which correlates to local meteoric water [92] [92] D. M. O’Brien, M. J. Woller. Rapid Commun. Mass Spectrom.21, 2422 (2007).[92] D. M. O’Brien, M. J. Woller. Rapid Commun. Mass Spectrom.21, 2422 (2007)..
Источники (7)
- [14] W. Dansgaard. Tellus16, 436 (1964).
- [15] I. D. Clark, P. Fritz. Environmental Isotopes in Hydrogeology, p. 328, Lewis Publishers, New York (1997).
- [19] K. A. Hobson. Oecologia120, 314 (1999).
- [20] K. A. Hobson, L. I. Wassenaar. Oecologia.109, 142 (1996).
- [92] D. M. O’Brien, M. J. Woller. Rapid Commun. Mass Spectrom.21, 2422 (2007).
- [93] I. Fraser, W. Meier-Augenstein, R. M. Kalin. Rapid Commun. Mass Spectrom.20, 1109 (2006).
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Oxygen.
The element property data was retrieved from publications.