Золото (Au)
Переходный металлТвёрдое тело
Стандартный атомный вес
196.966569 uЭлектронная конфигурация
[Xe] 6s1 4f14 5d10Температура плавления
1064.18 °C (1337.33 K)Температура кипения
2855.85 °C (3129 K)Плотность
1.928200e+4 kg/m³Степени окисления
−3, −2, −1, 0, +1, +2, +3, +5Электроотрицательность (Полинг)
2.54Энергия ионизации (1-я)
Год открытия
N/AАтомный радиус
135 pmДополнительно
Золото — плотный, мягкий переходный металл с исключительной устойчивостью к окислению и коррозии. Обычно оно встречается в самородном виде или в сплавах с серебром и другими драгоценными металлами, а не как обычные простые руды. Его химия определяется релятивистскими эффектами, которые, в частности, обусловливают желтый цвет металла и влияют на устойчивые степени окисления. Золото сочетает высокую электропроводность, ковкость, химическую благородность и культурную ценность таким образом, который недостижим для большинства элементов.
Оценивается, что всё золото мира, уже очищенное, можно было бы поместить в один куб со стороной 60 ft. Из всех элементов золото в чистом состоянии, несомненно, является самым красивым. Оно металлическое, имеющее жёлтый цвет в массиве, но в тонкодисперсном состоянии может быть чёрным, рубиновым или пурпурным. Пурпур Кассия является чувствительной пробой на аурическое золото. Это самый ковкий и тягучий металл; 1 oz. золота можно расковать в лист площадью 300 ft2. Это мягкий металл, и обычно его легируют, чтобы придать ему большую прочность. Он хорошо проводит тепло и электричество и не подвергается действию воздуха и большинства реагентов.
Название происходит от санскритского jval — «сиять», германского слова gulth — «сияющий металл» и англосаксонского gold неизвестного происхождения. Символ Au происходит от латинского aurum, связанного с Авророй, богиней зари. Золото было известно и высоко ценилось в доисторические времена.
Привлекательный и высокоценимый металл, золото известно по меньшей мере 5500 лет. Золото иногда встречается в природе в свободном виде, но обычно оно встречается в сочетании с серебром, кварцем (SiO2), кальцитом (CaCO3), свинцом, теллуром, цинком или медью. Примерно 1 миллиграмм золота растворен в каждой тонне морской воды, хотя его извлечение в настоящее время стоит дороже, чем само золото. Было оценено, что все золото, которое в настоящее время было рафинировано, можно было бы поместить в куб со стороной 20 метров.
Известное и высоко ценимое с древнейших времен, золото встречается в природе в виде свободного металла и в теллуридах; оно очень широко распространено и почти всегда связано с кварцем или пиритом.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
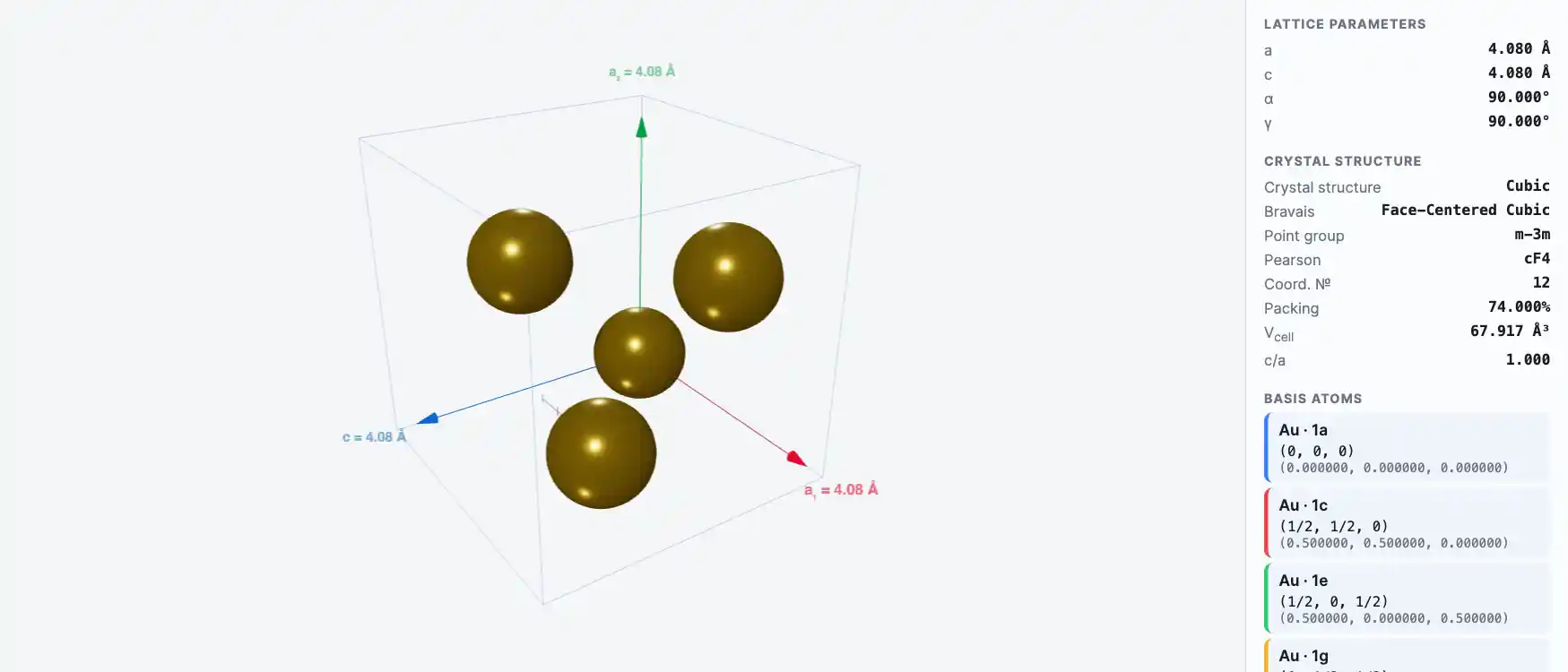
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Au: 4f¹⁴ 5d¹⁰ 6s¹[Xe] 4f¹⁴ 5d¹⁰ 6s¹1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹⁰ 6s¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 197 Стабильный | 196,96656879 ± 0,00000071 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 1039.2 °C ниже точки плавления (1064.18 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 79 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Au I | 0 | 191 | 20 | 90 |
| Au II | +1 | 111 | 0 | 10 |
| Au III | +2 | 150 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Au I | 0 | 75 |
| Au II | +1 | 48 |
| Au III | +2 | 2 |
| Au IV | +3 | 2 |
| Au V | +4 | 2 |
| Au VI | +5 | 2 |
| Au VII | +6 | 2 |
| Au VIII | +7 | 2 |
| Au IX | +8 | 2 |
| Au X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +1 | 6 | N/A | 137 пм |
| +3 | 4 | N/A | 68 пм |
| +3 | 6 | N/A | 85 пм |
| +5 | 6 | N/A | 56.99999999999999 пм |
Соединения
Изотопы (1)
The most common gold compounds are auric chloride and chlorauric acid, the latter being used in photography for toning the silver image. Gold has 18 isotopes; 198Au, with a half-life of 2.7 days, is used for treating cancer and other diseases. Disodium aurothiomalate is administered intramuscularly as a treatment for arthritis. A mixture of one part nitric acid with three of hydrochloric acid is called aqua regia (because it dissolved gold, the King of Metals). Gold is available commercially with a purity of 99.999+%. For many years the temperature assigned to the freezing point of gold has been 1063.0C; this has served as a calibration point for the International Temperature Scales (ITS-27 and ITS-48) and the International Practical Temperature Scale (IPTS-48). In 1968, a new International Practical Temperature Scale (IPTS-68) was adopted, which demands that the freezing point of gold be changed to 1064.43C. The specific gravity of gold has been found to vary considerably depending on temperature, how the metal is precipitated, and cold-worked.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 197 Стабильный | 196,96656879 ± 0,00000071 | 100.0000% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1337.33 K |
| Температура кипения | 3109.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (14)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.5239 |
| 2 | p | 4.4868 |
| 2 | s | 20.6302 |
| 3 | d | 13.4917 |
| 3 | p | 22.297 |
| 3 | s | 23.2372 |
| 4 | d | 37.472 |
| 4 | f | 38.3504 |
| 4 | p | 35.4532 |
| 4 | s | 34.5868 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 1 | VI | 151 | Ahrens (1952) ionic radius, | |
| 3 | IVSQ | 82 | ||
| 3 | VI | 99 | Ahrens (1952) ionic radius, | |
| 5 | VI | 71 |
Режимы распада изотопов (71)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 168 | p | — |
| 169 | p | — |
| 169 | A | — |
| 169 | B+ | — |
| 170 | p | 89% |
| 170 | A | 11% |
| 171 | p | 100% |
| 171 | A | — |
| 172 | A | 100% |
| 172 | p | — |
Факторы рассеяния X‑лучей (506)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.73645 |
| 10.1617 | — | 1.81425 |
| 10.3261 | — | 1.89553 |
| 10.4931 | — | 1.98045 |
| 10.6628 | — | 2.06919 |
| 10.8353 | — | 2.16029 |
| 11.0106 | — | 2.25522 |
| 11.1886 | — | 2.35433 |
| 11.3696 | — | 2.45698 |
| 11.5535 | — | 2.56237 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
4×10-3 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
4×10-6 milligrams per liter
Источники (1)
Sources
Sources of this element.
It occurs in veins and alluvial deposits, and is often separated from rocks and other minerals by mining and panning operations. About two thirds of the world's gold output comes from South Africa, and about two thirds of the total U.S. production comes from South Dakota and Nevada. The metal is recovered from its ores by cyaniding, amalgamating, and smelting processes. Refining is also frequently done by electrolysis. Gold occurs in sea water to the extent of 0.1 to 2 mg/ton, depending on the location where the sample is taken. As yet, no method has been found for recovering gold from sea water profitably.
Источники (1)
- [6] Gold https://periodic.lanl.gov/79.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Gold.
The element property data was retrieved from publications.