Лютеций (Lu)
ЛантаноидТвёрдое тело
Стандартный атомный вес
174.9668 uЭлектронная конфигурация
[Xe] 6s2 4f14 5d1Температура плавления
1662.85 °C (1936 K)Температура кипения
3401.85 °C (3675 K)Плотность
9840 kg/m³Степени окисления
0, +1, +2, +3Электроотрицательность (Полинг)
1.27Энергия ионизации (1-я)
Год открытия
1907Атомный радиус
175 pmДополнительно
Лютеций — плотный серебристый лантаноид и последний элемент 4f-ряда. В химии он почти исключительно трехвалентен, при этом ион Lu³⁺ имеет заполненную 4f-оболочку и сравнительно малый ионный радиус по сравнению с другими лантаноидами. Он встречается вместе с редкоземельными элементами в минералах, таких как монацит и ксенотим, но является одним из наименее распространенных лантаноидов. Его основная технологическая ценность связана со специализированными сцинтилляторами, катализаторами и медицинскими радиоизотопами, а не с массовым конструкционным применением.
Лютеций содержится в очень малых количествах почти во всех минералах, содержащих иттрий, и присутствует в монаците в количестве около 0.003%, что является промышленным источником. Чистый металл был выделен лишь в последние годы и является одним из самых трудных для получения. Его можно получить восстановлением безводных LuCl3 или LuF3 щелочным или щёлочноземельным металлом. Металл серебристо-белый и относительно стабилен на воздухе. 176Lu встречается в природе (2.6%) наряду с 175Lu (97.4%). Он радиоактивен с периодом полураспада около 3 x 1010 лет.
Название происходит от Lutetia, древнего названия города Парижа. Открытие лютеция приписывается французскому химику Жоржу Урбену в 1907 году, хотя ранее и независимо его выделил австрийский химик Карл Ауэр (барон фон Вельсбах) из образца иттербия.
Фон Вельсбах назвал элемент кассиопием в честь созвездия Кассиопеи. Однако, поскольку Урбен опубликовал свои результаты раньше Ауэра, его название элемента было принято ИЮПАК в 1949 году.
Минерал гадолинит ((Ce, La, Nd, Y)2FeBe2Si2O10), обнаруженный в карьере близ города Иттербю, Швеция, послужил источником большого числа редкоземельных элементов. В 1843 году Карл Густав Мосандер, шведский химик, смог разделить гадолинит на три фракции, которые он назвал иттрией, эрбией и тербией. Как и следовало ожидать, учитывая сходство их названий и свойств, ученые вскоре перепутали эрбию и тербию и к 1877 году поменяли их названия местами. То, что Мосандер называл эрбией, теперь называется тербией и наоборот. В 1878 году Жан Шарль Галиссар де Мариньяк, швейцарский химик, обнаружил, что сама эрбия состоит из двух компонентов. Один компонент Мариньяк назвал иттербией, тогда как второй сохранил название эрбия. Мариньяк считал, что иттербия представляет собой соединение нового элемента, который он назвал иттербием. Другие химики получали иттербий и проводили с ним эксперименты, пытаясь определить некоторые его свойства. К сожалению, разные ученые получали разные результаты в одних и тех же экспериментах. Хотя некоторые ученые считали, что эти несогласованные результаты вызваны плохой методикой или неисправным оборудованием, Жорж Урбен, французский химик, полагал, что иттербий вообще не является элементом, а представляет собой смесь двух элементов. В 1907 году Урбену удалось разделить иттербий на два элемента. Один из элементов Урбен назвал неоиттербием (новым иттербием), а другой — лютецием. Карл Ауэр фон Вельсбах, австрийский химик, работавший независимо от Урбена, почти в то же время пришел к тем же выводам. Вельсбах выбрал для этих элементов названия альдебараний и кассиопий. В конечном итоге открытие элементов было приписано Урбену, и он получил право дать им названия, хотя позднее химики изменили название неоиттербий обратно на иттербий и изменили написание lutecium на lutetium. Сегодня лютеций в основном получают методом ионного обмена из монацитового песка ((Ce, La, Th, Nd, Y)PO4), материала, богатого редкоземельными элементами.
Lutetia — древнее название Парижа. В 1907 году Урбен описал процесс, с помощью которого иттербий Мариньяка (1879) мог быть разделен на два элемента — иттербий (неоиттербий) и лютеций. Эти элементы были тождественны «альдебаранию» и «кассиопию», независимо открытым в это же время. Написание названия элемента было изменено с lutecium на lutetium в 1949 году.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
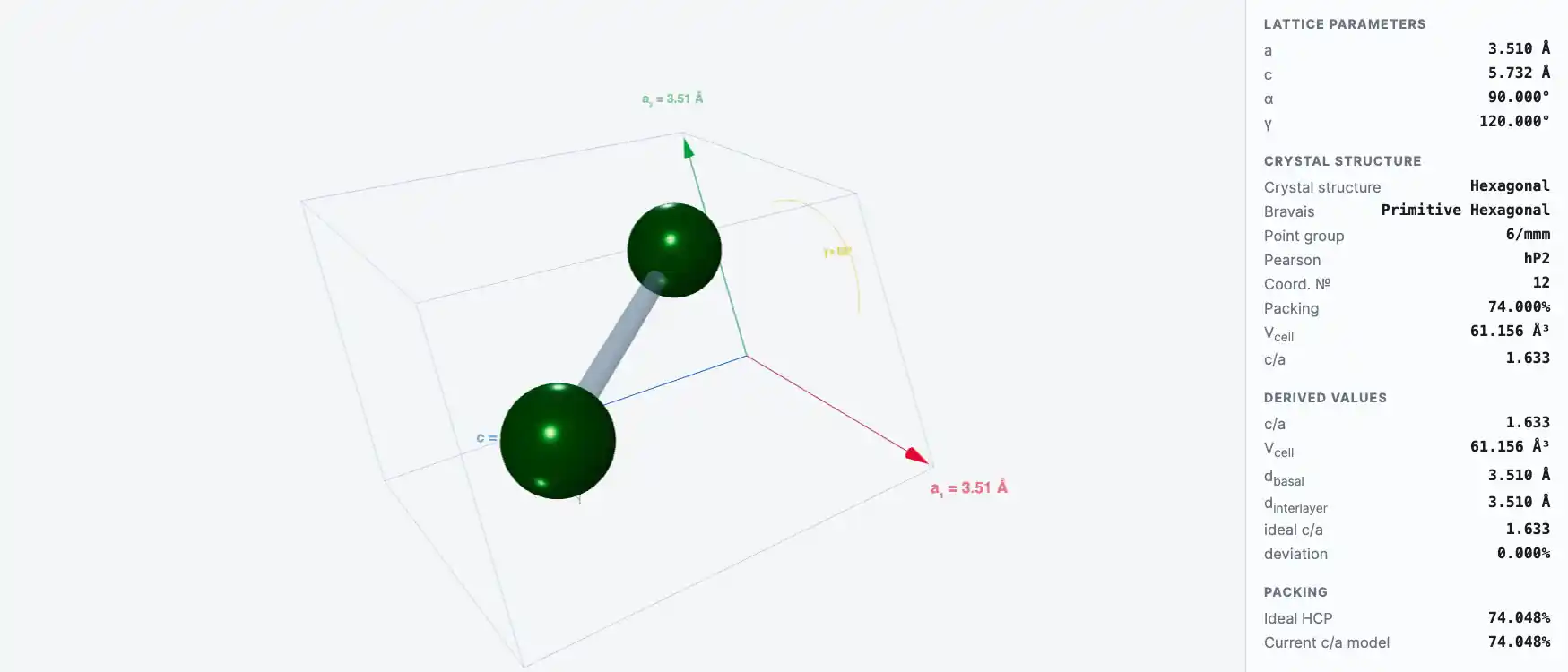
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Lu: 4f¹⁴ 5d¹ 6s²[Xe] 4f¹⁴ 5d¹ 6s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹ 6s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 175 Стабильный | 174,9407752 ± 0,000002 | 97.4010% | Стабильный |
Фазовое состояние
Причина: на 1637.8 °C ниже точки плавления (1662.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 71 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Lu I | 0 | 133 | 44 | 108 |
| Lu II | +1 | 79 | 9 | 17 |
| Lu III | +2 | 64 | 0 | 0 |
| Lu IV | +3 | 100 | 0 | 0 |
| Lu V | +4 | 64 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Lu I | 0 | 234 |
| Lu II | +1 | 40 |
| Lu III | +2 | 29 |
| Lu IV | +3 | 62 |
| Lu V | +4 | 40 |
| Lu VI | +5 | 2 |
| Lu VII | +6 | 2 |
| Lu VIII | +7 | 2 |
| Lu IX | +8 | 2 |
| Lu X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 86.1 пм |
| +3 | 8 | N/A | 97.7 пм |
| +3 | 9 | N/A | 103.2 пм |
Соединения
Изотопы (1)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 175 Стабильный | 174,9407752 ± 0,000002 | 97.4010% ± 0.0130% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1936.15 K |
| Температура кипения | 3675.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (14)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.3805 |
| 2 | p | 4.389 |
| 2 | s | 18.5502 |
| 3 | d | 13.5812 |
| 3 | p | 20.8337 |
| 3 | s | 21.4655 |
| 4 | d | 35.7108 |
| 4 | f | 40.0688 |
| 4 | p | 33.8096 |
| 4 | s | 32.7308 |
Детализация кристаллических радиусов (3)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 100.1 | from r^3 vs V plots, | |
| 3 | VIII | 111.7 | from r^3 vs V plots, | |
| 3 | IX | 117.2 | from r^3 vs V plots, |
Режимы распада изотопов (53)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 150 | p | 100% |
| 150 | B+ | — |
| 151 | p | — |
| 151 | B+ | — |
| 152 | B+ | 100% |
| 152 | B+p | 15% |
| 153 | A | — |
| 153 | B+ | — |
| 153 | p | 0% |
| 154 | B+ | — |
Факторы рассеяния X‑лучей (514)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.67493 |
| 10.1617 | — | 1.63824 |
| 10.3261 | — | 1.60236 |
| 10.4931 | — | 1.56726 |
| 10.6628 | — | 1.53293 |
| 10.8353 | — | 1.49935 |
| 11.0106 | — | 1.46651 |
| 11.1886 | — | 1.43538 |
| 11.3696 | — | 1.42424 |
| 11.5535 | — | 1.41319 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
8×10-1 milligrams per kilogram
Источники (1)
- [5] Lutetium https://education.jlab.org/itselemental/ele071.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.5×10-7 milligrams per liter
Источники (1)
- [5] Lutetium https://education.jlab.org/itselemental/ele071.html
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Lutetium.
The element property data was retrieved from publications.