Углерод (C)
НеметаллТвёрдое тело
Стандартный атомный вес
12.011 u [12,0096, 12,0116]Электронная конфигурация
[He] 2s2 2p2Температура плавления
3549.85 °C (3823 K)Температура кипения
3824.85 °C (4098 K)Плотность
2267 kg/m³Степени окисления
−4, −3, −2, −1, 0, +1, +2, +3, +4Электроотрицательность (Полинг)
2.55Энергия ионизации (1-я)
Год открытия
1797Атомный радиус
70 pmДополнительно
Углерод — неметалл группы 14 и определяющий элемент органической химии. Его небольшие атомы образуют прочные ковалентные связи с углеродом и многими другими элементами, что позволяет формировать цепи, кольца, сетки и кратные связи огромного разнообразия. Он встречается в природе в виде графита, алмаза, аморфных углеродсодержащих материалов, карбонатных минералов, ископаемого углерода, растворенных углеродных форм и как центральный элемент живого вещества.
Углерод относится к 14-й группе периодической таблицы. Он имеет три аллотропные формы: алмаз, графит и фуллерит. ¹⁴C широко используется в радиометрическом датировании. Углерод присутствует во всей органической жизни и является основой органической химии. Углерод обладает интересным химическим свойством образовывать связи с самим собой и с широким разнообразием других элементов.
Название происходит от латинского carbo, «древесный уголь». Он был известен в доисторические времена в форме древесного угля и сажи. В 1797 году английский химик Смитсон Теннант доказал, что алмаз является чистым углеродом.
Углерод, шестой по распространенности элемент во Вселенной, известен с древних времен. Углерод чаще всего получают из угольных месторождений, хотя его обычно необходимо перерабатывать в форму, пригодную для коммерческого использования. Известно, что существуют три природных аллотропа углерода: аморфный, графит и алмаз.
От латинского слова carbo: древесный уголь. Углерод, элемент доисторического происхождения, чрезвычайно широко распространен в природе. Он в изобилии встречается на Солнце, звездах, кометах и в атмосферах большинства планет. Углерод в форме микроскопических алмазов обнаруживается в некоторых метеоритах.
Природные алмазы встречаются в кимберлите древних вулканических «трубок», найденных в Южной Африке, Арканзасе и в других местах. В настоящее время алмазы также извлекают со дна океана у мыса Доброй Надежды. Около 30% всех промышленных алмазов, используемых в США, теперь производится синтетически.
Энергию Солнца и звезд можно приписать, по крайней мере частично, известному углеродно-азотному циклу.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
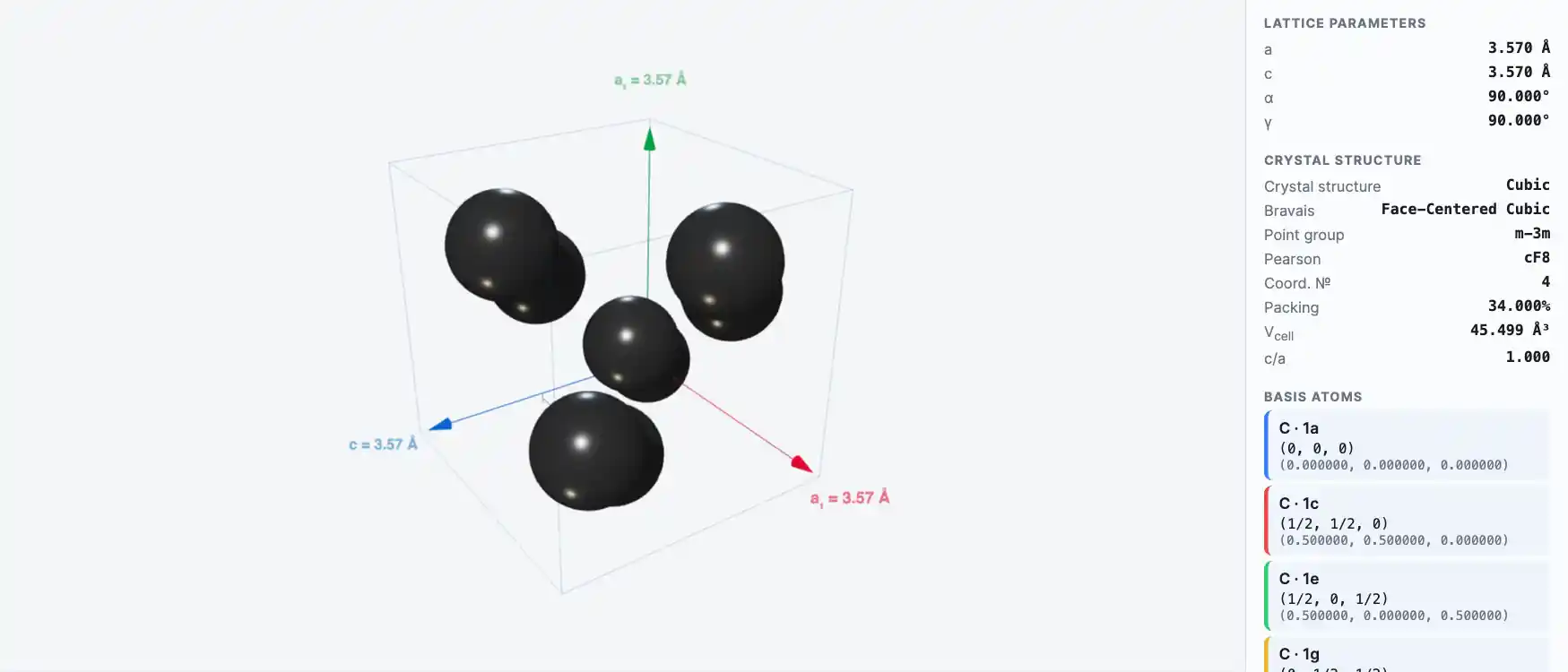
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
C: 2s² 2p²[He] 2s² 2p²1s² 2s² 2p²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 12 Стабильный | 12 | 98.9300% | Стабильный |
| 13 Стабильный | 13,00335483507 ± 0,00000000023 | 1.0700% | Стабильный |
Фазовое состояние
Причина: на 3799.8 °C ниже точки сублимации (3824.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 11 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| C I | 0 | 2102 | 1616 | 2102 |
| 12C I Изотоп | 0 | 89 | 0 | 89 |
| 13C I Изотоп | 0 | 89 | 0 | 89 |
| 12C II Изотоп | +1 | 187 | 0 | 187 |
| 14C II Изотоп | +1 | 187 | 0 | 187 |
| C II | +1 | 1605 | 1433 | 1605 |
| 13C II Изотоп | +1 | 187 | 0 | 187 |
| C III | +2 | 882 | 878 | 878 |
| C IV | +3 | 259 | 224 | 255 |
| C V | +4 | 149 | 146 | 147 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| C I | 0 | 435 |
| 12C I Изотоп | 0 | 33 |
| 13C I Изотоп | 0 | 33 |
| 12C II Изотоп | +1 | 36 |
| 14C II Изотоп | +1 | 36 |
| C II | +1 | 415 |
| 13C II Изотоп | +1 | 36 |
| C III | +2 | 201 |
| C IV | +3 | 107 |
| C V | +4 | 156 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +4 | 4 | N/A | 15 пм |
| +4 | 6 | N/A | 16 пм |
Соединения
Изотопы (2)
Carbon has seven isotopes. In 1961 the International Union of Pure and Applied Chemistry adopted the isotope carbon-12 as the basis for atomic weights. Carbon-14, an isotope with a half-life of 5715 years, has been widely used to date such materials as wood, archaeological specimens, etc.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 12 Стабильный | 12 | 98.9300% ± 0.0800% | Стабильный | stable | |
| 13 Стабильный | 13,00335483507 ± 0,00000000023 | 1.0700% ± 0.0800% | Стабильный | stable |
Спектральные линии
Показано 50 из 993 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 505.214927 нм | 160000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.4p 1D | Измерено | NIST | |
| 538.033014 нм | 120000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.4p 1P | Измерено | NIST | |
| 711.31656 нм | 110000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.4d 3F* | Измерено | NIST | |
| 493.202524 нм | 73000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.4p 1S | Измерено | NIST | |
| 477.173374 нм | 69000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.4p 3P | Измерено | NIST | |
| 711.697758 нм | 45000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5s 3P* | Измерено | NIST | |
| 658.76211 нм | 40000 | C I | emission | 2s2.2p.3p 1P → 2s2.2p.4d 1P* | Измерено | NIST | |
| 579.311495 нм | 38000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3P | Измерено | NIST | |
| 711.96559 нм | 37000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5s 3P* | Измерено | NIST | |
| 580.059993 нм | 35000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3P | Измерено | NIST | |
| 600.1123 нм | 35000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.6s 3P* | Измерено | NIST | |
| 477.589266 нм | 34000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.4p 3P | Измерено | NIST | |
| 437.13814 нм | 33000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.5p 1P | Измерено | NIST | |
| 711.145795 нм | 32000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.4d 3F* | Измерено | NIST | |
| 682.814076 нм | 27000 | C I | emission | 2s2.2p.3p 1P → 2s2.2p.4d 1D* | Измерено | NIST | |
| 504.149039 нм | 25000 | C I | emission | 2s.2p3 3D* → 2s2.2p.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 477.002376 нм | 24000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.4p 3P | Измерено | NIST | |
| 600.6012 нм | 23000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5d 3D* | Измерено | NIST | |
| 665.55294 нм | 20000 | C I | emission | 2s2.2p.3p 1P → 2s2.2p.5s 1P* | Измерено | NIST | |
| 710.011312 нм | 19000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5s 3P* | Измерено | NIST | |
| 566.894 нм | 18000 | C I | emission | 2s2.2p.3p 1P → 2s2.2p.5d 1P* | Измерено | NIST | |
| 596.933151 нм | 18000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3D | Измерено | NIST | |
| 708.782188 нм | 18000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.4d 3D* | Измерено | NIST | |
| 402.94119 нм | 16000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.5p 3P | Измерено | NIST | |
| 601.64487 нм | 16000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5d 3F* | Измерено | NIST | |
| 473.426281 нм | 15000 | C I | emission | 2s.2p3 3D* → 2s2.2p.5p 3P | Измерено | NIST | |
| 481.737213 нм | 15000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.4p 3S | Измерено | NIST | |
| 579.446608 нм | 15000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3P | Измерено | NIST | |
| 748.344451 нм | 15000 | C I | emission | 2s2.2p.3p 3S → 2s2.2p.4d 3P* | Измерено | NIST | |
| 406.52425 нм | 14000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.5p 3D | Измерено | NIST | |
| 580.52017 нм | 14000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3P | Измерено | NIST | |
| 601.4833 нм | 14000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.6s 3P* | Измерено | NIST | |
| 710.89263 нм | 14000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.5s 3P* | Измерено | NIST | |
| 400.9928 нм | 13000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.6p 1P | Измерено | NIST | |
| 422.83269 нм | 13000 | C I | emission | 2s2.2p.3s 1P* → 2s2.2p.5p 1S | Измерено | NIST | |
| 447.85821 нм | 13000 | C I | emission | 2s.2p3 3D* → 2s2.2p.(2P*<1/2>).5f 2[5/2] | Измерено | NIST | |
| 504.012903 нм | 12000 | C I | emission | 2s.2p3 3D* → 2s2.2p.(2P*<1/2>).4f 2[7/2] | Измерено | NIST | |
| 601.0669 нм | 12000 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.6s 3P* | Измерено | NIST | |
| 406.4264 нм | 11000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.5p 3D | Измерено | NIST | |
| 639.7965 нм | 11000 | C I | emission | 2s2.2p.3p 3S → 2s2.2p.6s 3P* | Измерено | NIST | |
| 666.3043 нм | 11000 | C I | emission | 2s2.2p.3p 3P → 2s2.2p.5d 3D* | Измерено | NIST | |
| 667.1849 нм | 11000 | C I | emission | 2s2.2p.3p 3P → 2s2.2p.6s 3P* | Измерено | NIST | |
| 403.180216 нм | 10000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.5p 3P | Измерено | NIST | |
| 482.679468 нм | 10000 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.4p 3S | Измерено | NIST | |
| 598.903753 нм | 10000 | C I | emission | 2s.2p3 3D* → 2s2.2p.4p 3D | Измерено | NIST | |
| 707.649944 нм | 9900 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.4d 3D* | Измерено | NIST | |
| 402.284321 нм | 9700 | C I | emission | 2s2.2p.3s 3P* → 2s2.2p.5p 3P | Измерено | NIST | |
| 555.1578 нм | 9600 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.7s 3P* | Измерено | NIST | |
| 600.7173 нм | 9600 | C I | emission | 2s2.2p.3p 3D → 2s2.2p.6s 3P* | Измерено | NIST | |
| 502.492938 нм | 9400 | C I | emission | 2s.2p3 3D* → 2s2.2p.(2P*<3/2>).4f 2[7/2] | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура кипения | 4098.15 K |
| Тройная точка (температура) | 4762.15 K |
| Тройная точка (давление) | 10300 kPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (3)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.3273 |
| 2 | p | 2.8642 |
| 2 | s | 2.7834 |
Детализация кристаллических радиусов (3)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 4 | III | 6 | ||
| 4 | IV | 29 | Pauling's (1960) crystal radius, | |
| 4 | VI | 30 | Ahrens (1952) ionic radius, |
Режимы распада изотопов (27)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 8 | 2p | 100% |
| 9 | B+ | 100% |
| 9 | B+p | 7.5% |
| 9 | B+A | 38.4% |
| 10 | B+ | 100% |
| 11 | B+ | 100% |
| 14 | B- | 100% |
| 15 | B- | 100% |
| 16 | B- | 100% |
| 16 | B-n | 99% |
Факторы рассеяния X‑лучей (502)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.80688 |
| 10.1617 | — | 0.85152 |
| 10.3261 | — | 0.89863 |
| 10.4931 | — | 0.94834 |
| 10.6628 | — | 1.0008 |
| 10.8353 | — | 1.05755 |
| 11.0106 | — | 1.12167 |
| 11.1886 | — | 1.18968 |
| 11.3696 | — | 1.26181 |
| 11.5535 | — | 1.33832 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.00×102 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
2.8×101 milligrams per liter
Источники (1)
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
Variations in the isotope-amount ratio n(13C)/n(12C) of biological products can be observed using isotope-ratio mass spectrometry (IRMS) to detect adulteration (the addition of inferior ingredients) in honey and other food products.
The isotope-amount ratio n(13C)/n(12C) can fluctuate between carbon sources, for example C3 plants (found in temperate climates and which use atmospheric carbon dioxide to make a 3-carbon molecule during photosynthesis — examples include rice, potatoes, tomatoes, and sugar beets), C4 plants (found in hot climates and which use atmospheric carbon dioxide to make a 4-carbon molecule during photosynthesis — examples include corn and sugar cane), animal carbon, atmospheric CO2, etc. This commonly makes it possible to detect whether these different carbon sources have been mixed by using isotope or mass balance to distinguish, for example, between beet sugar and cane sugar. Complications in source identification can arise with plants that open stomata at night to collect carbon dioxide to use a third mechanism to fix atmospheric carbon dioxide (CAM or crassulacean acid metabolism). The isotope-amount ratio n(13C)/n(12C) of CAM plants overlaps that of C3 or C4 plants — examples include pineapples and jade plants. The following adulterations are commonly detected using stable carbon isotope IRMS:
–Variations in the isotope-amount ratio n(13C)/n(12C) of honey are used to detect the addition (and potential adulteration) of high fructose corn syrup, corn, or sugar cane [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)..
–Variations in the isotope-amount ratio n(13C)/n(12C) of fruit juice have been used to detect the addition of a sugar [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)..
–Variations in the isotope-amount ratio n(13C)/n(12C) of natural vanilla extract have been used to detect the addition of artificial vanillin or p-hydroxybenzaldehyde [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)..
–Variations in the isotope-amount ratio n(13C)/n(12C) of beer are used to detect C4 carbon, which would indicate that a beer company may have added ingredients that are not traditionally used in brewing beer. Therefore, this ratio is used to detect the misrepresentation of a product as being pure [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)., [68] [68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).[68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002)..
Stable carbon IRMS has been used to determine if the botanical origin of an alcoholic spirit has been mislabeled and if chaptalization (the process of adding sugar to increase the alcoholic content) of wine has occurred [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)., [68] [68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).[68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).. 14C scintillation counting has been used to determine the age of wine and alcoholic spirits [67] [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).[67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002)., [68] [68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).[68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).. Variations in the isotope-amount ratio n(13C)/n(12C) of urine has been used to determine if steroids in urine are natural or of synthetic origin. These measurements enable anti-doping laboratories to perfect their methods for detecting steroid doping in athletes [69] [69] B. D. Ahrens, A. W. Butch. Drug Test Anal.5, 534 (2013).[69] B. D. Ahrens, A. W. Butch. Drug Test Anal.5, 534 (2013)., [70] [70] E. Bulska, D. Gorczyca, I. Zalewska, A. Pokrywka, D. Kwiatkowska. J. Pharm. Biomed. Anal.106, 159 (2015).[70] E. Bulska, D. Gorczyca, I. Zalewska, A. Pokrywka, D. Kwiatkowska. J. Pharm. Biomed. Anal.106, 159 (2015)., [71] [71] A. Casilli, T. Piper, F. A. de Oliveira, M. Costa Padilha, H. Marcelo Pereira, M. Thevis, F. R. de Aquino Neto. Drug Test Anal.8, 1204 (2016).[71] A. Casilli, T. Piper, F. A. de Oliveira, M. Costa Padilha, H. Marcelo Pereira, M. Thevis, F. R. de Aquino Neto. Drug Test Anal.8, 1204 (2016).. Variations in the isotope-amount ratio n(13C)/n(12C) of marijuana can provide information to determine if the plants were grown “inside” a building or greenhouse or were “open grown” (Fig. IUPAC.6.4). Plant carbon isotopic compositions are controlled by atmospheric CO2 and the supply and demand of CO2 in photosynthesis (the process used by plants to convert light energy from the sun into chemical energy). “Open grown” plants are grown in an area that is well ventilated and receives natural CO2. In contrast, plants grown “inside” receive supplemented CO2 and the photosynthesis process is more confined. Additionally, CO2 from a tank of compressed gas used to augment atmospheric CO2 to increase the growth of marijuana plants is commonly highly depleted in 13C as a refinery by-product. These differences change the carbon isotope ratios of the plants and the ratios vary enough to enable the determination of the growing and cultivation process of marijuana [72] [72] E. K. Shibuya, J. E. Souza Sarkis, O. N. Neto, M. Z. Moreira, R. L. Victoria. Forensic Sci. Int.160, 35 (2006).[72] E. K. Shibuya, J. E. Souza Sarkis, O. N. Neto, M. Z. Moreira, R. L. Victoria. Forensic Sci. Int.160, 35 (2006)., [73] [73] J. B. West, J. M. Hurley, J. R. Ehleringer. J Forensic Sci.54, 84 (2009).[73] J. B. West, J. M. Hurley, J. R. Ehleringer. J Forensic Sci.54, 84 (2009)..
Источники (9)
- [67] C. Cordella, I. Moussa, A. C. Martel, N. Sbirrazzuoli, L. Lizzani-Cuvelier. J. Agric. Food. Chem.50, 1751 (2002).
- [68] J. R. Brooks, N. Buchmann, S. Phillips, B. Ehleringer, R. D. Evans, M. Lott, L. A. Martinelli, W. T. Pockman, D. Sandquist, J. P. Sparks, L. Sperry, D. Williams, J. R. Ehleringer. J. Agric. Food. Chem.50, 6413 (2002).
- [69] B. D. Ahrens, A. W. Butch. Drug Test Anal.5, 534 (2013).
- [70] E. Bulska, D. Gorczyca, I. Zalewska, A. Pokrywka, D. Kwiatkowska. J. Pharm. Biomed. Anal.106, 159 (2015).
- [71] A. Casilli, T. Piper, F. A. de Oliveira, M. Costa Padilha, H. Marcelo Pereira, M. Thevis, F. R. de Aquino Neto. Drug Test Anal.8, 1204 (2016).
- [72] E. K. Shibuya, J. E. Souza Sarkis, O. N. Neto, M. Z. Moreira, R. L. Victoria. Forensic Sci. Int.160, 35 (2006).
- [73] J. B. West, J. M. Hurley, J. R. Ehleringer. J Forensic Sci.54, 84 (2009).
- [74] United States Drug Enforcement Administration. Marijuana-Indoor Marijuana Grow, United States Department of Justice (2014), Feb. 22; http://www.justice.gov/dea/pr/multimedia-library/image-gallery/images_marijuana.shtml.
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Carbon.
The element property data was retrieved from publications.