Рутений (Ru)
Переходный металлТвёрдое тело
Стандартный атомный вес
101.07 uЭлектронная конфигурация
[Kr] 5s1 4d7Температура плавления
2333.85 °C (2607 K)Температура кипения
4149.85 °C (4423 K)Плотность
1.210000e+4 kg/m³Степени окисления
−4, −2, +1, +2, +3, +4, +5, +6, +7, +8Электроотрицательность (Полинг)
2.2Энергия ионизации (1-я)
Год открытия
1828Атомный радиус
130 pmДополнительно
Рутений — твёрдый переходный металл платиновой группы с атомным номером 44. Он редко встречается в земной коре и главным образом извлекается вместе с платиновыми и никель-медноколчеданными рудами. Химически он примечателен широким диапазоном степеней окисления, особенно +2, +3, +4, +6 и +8, а также образованием множества координационных и металлоорганических соединений. Металлический рутений повышает твёрдость и коррозионную стойкость в некоторых сплавах платины и палладия, тогда как его оксиды и комплексы важны в катализе и электрохимии.
Рутений — твёрдый, белый металл, имеющий четыре кристаллические модификации. При комнатной температуре он не тускнеет, но взрывообразно окисляется. На него действуют галогены, гидроксиды и т. д. Рутений можно наносить электроосаждением или методами термического разложения. Этот металл является одним из наиболее эффективных упрочнителей платины и палладия; его легируют с этими металлами для изготовления электрических контактов, рассчитанных на сильный износ. Сообщается, что сплав рутения с молибденом является сверхпроводящим при 10,6 K. Коррозионная стойкость титана повышается в сто раз при добавлении 0,1% рутения. Он является универсальным катализатором. Сероводород может каталитически расщепляться под действием света при использовании водной суспензии частиц CdS, содержащих диоксид рутения. Предполагается, что это может найти применение для удаления H2S в нефтепереработке и других промышленных процессах. Обнаружены соединения по меньшей мере в восьми степенях окисления, однако наиболее распространены состояния +2, +3 и +4. Тетраоксид рутения, подобно тетраоксиду осмия, чрезвычайно токсичен. Кроме того, он может взрываться. Соединения рутения демонстрируют выраженное сходство с соединениями кадмия.
Название происходит от латинского ruthenia — старого названия России. Он был обнаружен в сырой платиновой руде русским химиком Готфридом Вильгельмом Оссаном в 1828 году. Оссан считал, что в образце он обнаружил три новых металла: pluranium, ruthenium и polinium. В 1844 году русский химик Карл Карлович Клаус смог показать, что ошибка Оссана была вызвана загрязненностью образца, и Клаус смог выделить металлический рутений.
Рутений был открыт Карлом Карловичем Клаусом, русским химиком, в 1844 году при анализе остатка образца платиновой руды, полученного с Уральских гор. По-видимому, Енджей Снядецкий, польский химик, получил рутений в 1807 году, но отказался от своего заявления об открытии после того, как другие ученые не смогли воспроизвести его результаты. Рутений обычно встречается вместе с месторождениями платины и в основном получают как побочный продукт добычи и рафинирования платины. Рутений также получают как побочный продукт при добыче никеля в районе Садбери в Онтарио, Канада.
От латинского слова Ruthenia — Россия. В 1827 году Берцелиус и Оссан исследовали остатки, оставшиеся после растворения сырой платины с Уральских гор в царской водке. Хотя Берцелиус не обнаружил необычных металлов, Оссан считал, что нашел три новых металла, один из которых он назвал ruthenium. В 1844 году Клаус, обычно признаваемый открывателем, показал, что оксид ruthenium Оссана был очень загрязнен и что он содержал новый металл. Клаус получил 6 г рутения из той части сырой платины, которая не растворяется в царской водке.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
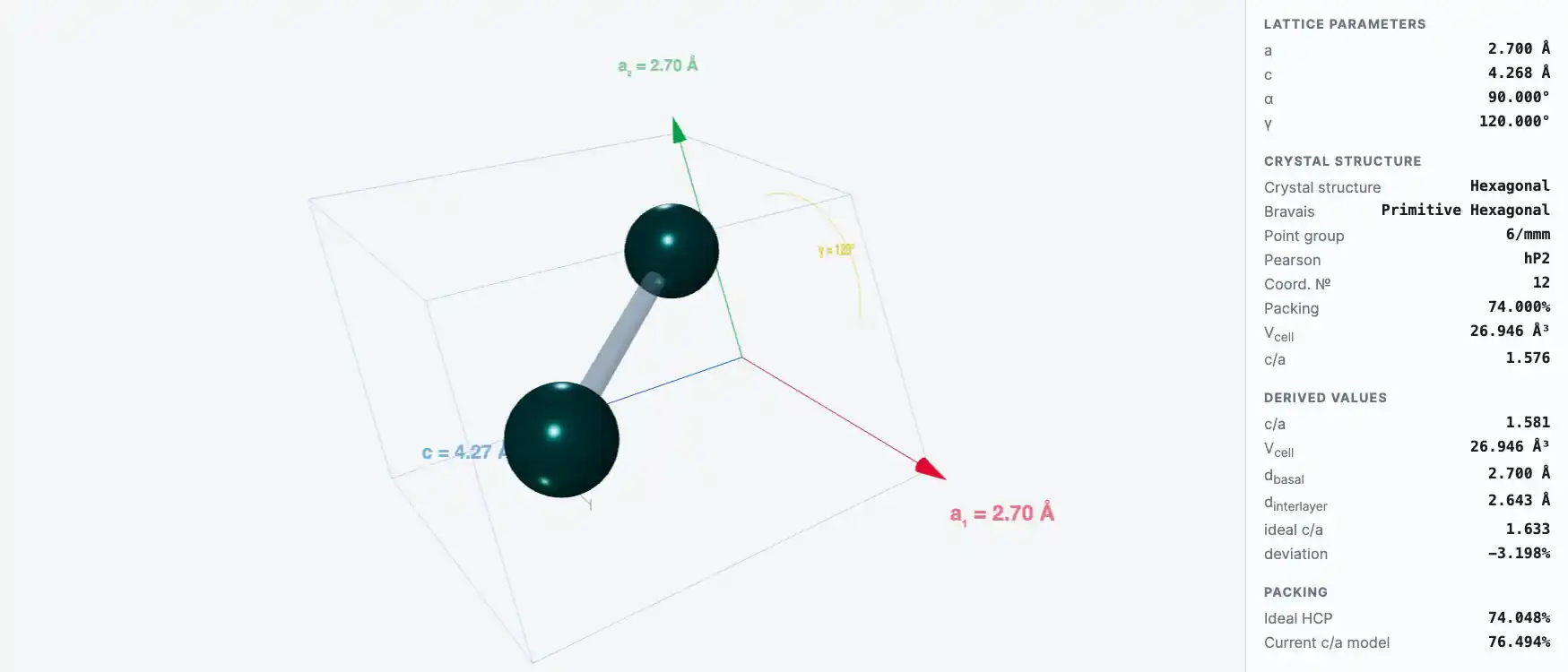
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Ru: 4d⁷ 5s¹[Kr] 4d⁷ 5s¹1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d⁷ 5s¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 98 Стабильный | 97,9052868 ± 0,0000069 | 1.8700% | Стабильный |
| 99 Стабильный | 98,9059341 ± 0,0000011 | 12.7600% | Стабильный |
| 100 Стабильный | 99,9042143 ± 0,0000011 | 12.6000% | Стабильный |
| 101 Стабильный | 100,9055769 ± 0,0000012 | 17.0600% | Стабильный |
| 102 Стабильный | 101,9043441 ± 0,0000012 | 31.5500% | Стабильный |
| 104 Стабильный | 103,9054275 ± 0,0000028 | 18.6200% | Стабильный |
Фазовое состояние
Причина: на 2308.8 °C ниже точки плавления (2333.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 44 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Ru I | 0 | 541 | 11 | 519 |
| Ru II | +1 | 59 | 8 | 59 |
| Ru III | +2 | 93 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Ru I | 0 | 329 |
| Ru II | +1 | 235 |
| Ru III | +2 | 26 |
| Ru IV | +3 | 2 |
| Ru V | +4 | 2 |
| Ru VI | +5 | 2 |
| Ru VII | +6 | 2 |
| Ru VIII | +7 | 2 |
| Ru IX | +8 | 2 |
| Ru X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +3 | 6 | N/A | 68 пм |
| +4 | 6 | N/A | 62 пм |
| +5 | 6 | N/A | 56.49999999999999 пм |
| +7 | 4 | N/A | 38 пм |
| +8 | 4 | N/A | 36 пм |
Соединения
Изотопы (6)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 98 Стабильный | 97,9052868 ± 0,0000069 | 1.8700% ± 0.0300% | Стабильный | stable | |
| 99 Стабильный | 98,9059341 ± 0,0000011 | 12.7600% ± 0.1400% | Стабильный | stable | |
| 100 Стабильный | 99,9042143 ± 0,0000011 | 12.6000% ± 0.0700% | Стабильный | stable | |
| 101 Стабильный | 100,9055769 ± 0,0000012 | 17.0600% ± 0.0200% | Стабильный | stable | |
| 102 Стабильный | 101,9043441 ± 0,0000012 | 31.5500% ± 0.1400% | Стабильный | stable | |
| 104 Стабильный | 103,9054275 ± 0,0000028 | 18.6200% ± 0.2700% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 2606.15 K |
| Температура кипения | 4420.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (10)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.9077 |
| 2 | p | 4.0492 |
| 2 | s | 11.6202 |
| 3 | d | 14.6411 |
| 3 | p | 16.7789 |
| 3 | s | 16.3988 |
| 4 | d | 31.1872 |
| 4 | p | 27.5652 |
| 4 | s | 26.344 |
| 5 | s | 37.5155 |
Детализация кристаллических радиусов (5)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 3 | VI | 82 | ||
| 4 | VI | 76 | from r^3 vs V plots, from metallic oxides, | |
| 5 | VI | 70.5 | estimated, from r^3 vs V plots, | |
| 7 | IV | 52 | ||
| 8 | IV | 50 |
Режимы распада изотопов (62)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 85 | B+ | — |
| 85 | B+p | — |
| 85 | p | — |
| 86 | B+ | — |
| 86 | B+p | — |
| 87 | B+ | — |
| 87 | B+p | — |
| 88 | B+ | 100% |
| 88 | B+p | 3.6% |
| 89 | B+ | 100% |
Факторы рассеяния X‑лучей (615)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.51919 |
| 10.1617 | — | 1.51438 |
| 10.3261 | — | 1.51486 |
| 10.4931 | — | 1.54335 |
| 10.6628 | — | 1.57238 |
| 10.8353 | — | 1.60195 |
| 11.0105 | — | 1.63207 |
| 11.1886 | — | 1.66277 |
| 11.3696 | — | 1.7032 |
| 11.5535 | — | 1.79614 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1×10-3 milligrams per kilogram
Источники (1)
- [5] Ruthenium https://education.jlab.org/itselemental/ele044.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
7×10-7 milligrams per liter
Источники (1)
- [5] Ruthenium https://education.jlab.org/itselemental/ele044.html
Sources
Sources of this element.
A member of the platinum group, ruthenium occurs native with other members of the group in ores found in the Ural mountains and in North and South America. It is also found along with other platinum metals in small but commercial quantities in pentlandite in the Sudbury, Ontario nickel-mining region, and in the pyroxinite deposits of South Africa.
Источники (1)
- [6] Ruthenium https://periodic.lanl.gov/44.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
The metal is isolated commercially by a complex chemical process, the final stage of which is the hydrogen reduction of ammonium ruthenium chloride, which yields a powder. The powder is consolidated by powder metallurgy techniques or by argon-arc welding.
Источники (1)
- [6] Ruthenium https://periodic.lanl.gov/44.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Ruthenium.
The element property data was retrieved from publications.