Цирконий (Zr)
Переходный металлТвёрдое тело
Стандартный атомный вес
91.224 uЭлектронная конфигурация
[Kr] 5s2 4d2Температура плавления
1854.85 °C (2128 K)Температура кипения
4408.85 °C (4682 K)Плотность
6520 kg/m³Степени окисления
+1, +2, +3, +4Электроотрицательность (Полинг)
1.33Энергия ионизации (1-я)
Год открытия
1789Атомный радиус
155 pmДополнительно
Цирконий — блестящий переходный металл группы 4, химически близкий к гафнию и титану. Он встречается главным образом в цирконе и родственных тяжелых минералах, почти всегда в сопровождении гафния. Металл ценится за очень низкое сечение захвата тепловых нейтронов и устойчивую, прочно сцепленную оксидную пленку, что обеспечивает ему центральную роль в материалах для ядерных реакторов и в коррозионностойких сплавах.
Зирконий ядерного качества практически не содержит гафния. Zircaloy(R) — важный сплав, разработанный специально для ядерных применений. Зирконий исключительно устойчив к коррозии под действием многих обычных кислот и щелочей, морской воды и других реагентов. В сплаве с цинком зирконий становится магнитным при температурах ниже 35°K.
Название происходит от арабского zargun, означающего «золотоподобный». Он был открыт в цирконии немецким химиком Мартином-Хайнрихом Клапротом в 1789 году. Цирконий впервые был выделен шведским химиком Йёнсом Якобом Берцелиусом в 1824 году в нечистом состоянии и окончательно — химиками Д. Лели-младшим и Л. Гамбургером в чистом виде в 1914 году.
Цирконий был открыт Мартином Хайнрихом Клапротом, немецким химиком, при анализе состава минерала жаргон (ZrSiO4) в 1789 году. Цирконий был выделен Йёнсом Якобом Берцелиусом, шведским химиком, в 1824 году и окончательно получен в чистой форме в 1914 году. Получение чистого циркония чрезвычайно затруднено, поскольку он химически сходен с гафнием — элементом, который всегда встречается в смеси с месторождениями циркония. Сегодня большую часть циркония получают из минералов циркона (ZrSiO4) и бадделеита (ZrO2) посредством процесса, известного как процесс Кролла.
От персидского zargun, «золотоподобный». Циркон, основной драгоценный камень циркония, также известен как жаргон, гиацинт, иацинт или лигур. Этот минерал или его разновидности упоминаются в библейских текстах. До тех пор пока Клапрот в 1789 году не проанализировал жаргон из Цейлона и не идентифицировал новый элемент, о том, что минерал содержит новый элемент, не было известно; Вернер назвал его цирконом (silex circonius), а Клапрот — Zirkonertz (циркония). Нечистый металл впервые был выделен Берцелиусом в 1824 году путём нагревания смеси калия и фторцирконата калия в небольшой установке разложения, которую они разработали.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
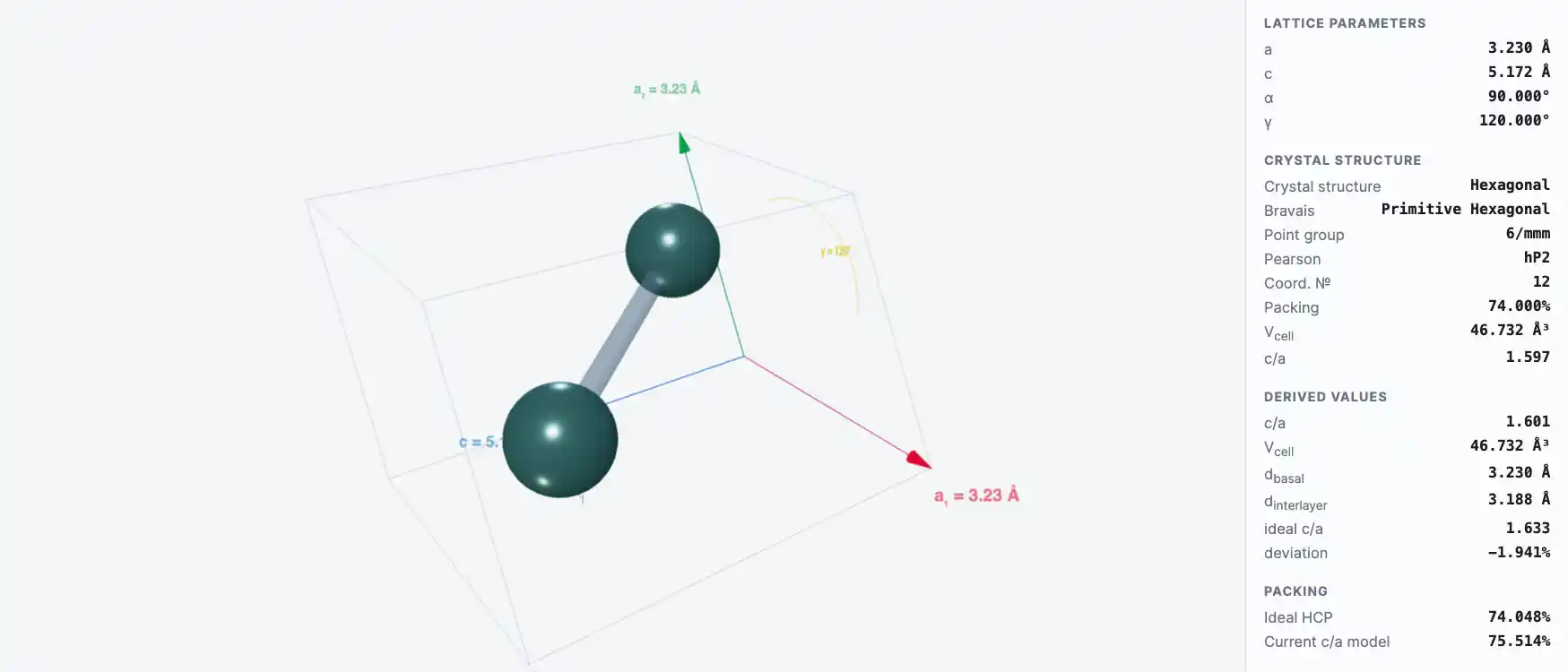
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Zr: 4d² 5s²[Kr] 4d² 5s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d² 5s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 90 Стабильный | 89,9046977 ± 0,000002 | 51.4500% | Стабильный |
| 91 Стабильный | 90,9056396 ± 0,000002 | 11.2200% | Стабильный |
| 92 Стабильный | 91,9050347 ± 0,000002 | 17.1500% | Стабильный |
Фазовое состояние
Причина: на 1829.8 °C ниже точки плавления (1854.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 40 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Zr I | 0 | 459 | 0 | 0 |
| Zr II | +1 | 207 | 0 | 0 |
| Zr III | +2 | 490 | 490 | 490 |
| Zr IV | +3 | 76 | 0 | 76 |
| Zr V | +4 | 104 | 0 | 0 |
| Zr VI | +5 | 427 | 427 | 427 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Zr I | 0 | 262 |
| Zr II | +1 | 136 |
| Zr III | +2 | 140 |
| Zr IV | +3 | 35 |
| Zr V | +4 | 102 |
| Zr VI | +5 | 97 |
| Zr VII | +6 | 2 |
| Zr VIII | +7 | 2 |
| Zr IX | +8 | 2 |
| Zr X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +4 | 4 | N/A | 59 пм |
| +4 | 5 | N/A | 66 пм |
| +4 | 6 | N/A | 72 пм |
| +4 | 7 | N/A | 78 пм |
| +4 | 8 | N/A | 84 пм |
| +4 | 9 | N/A | 89 пм |
Соединения
Изотопы (3)
Naturally occurring zirconium contains five isotopes. Fifteen other isotopes are known to exist. Zircon, ZrSiO4, the principal ore, is pure ZrO2 in crystalline form having a hafnium content of about 1%. Zirconium also occurs in some 30 other recognized mineral species. Zirconium is produced commercially by reduction of chloride with magnesium (the Kroll Process), and by other methods. It is a grayish-white lustrous metal. When finely divided, the metal may ignite spontaneously in air, especially at elevated temperatures. The solid metal is much more difficult to ignite. The inherent toxicity of zirconium compounds is low. Hafnium is invariably found in zirconium ores, and the separation is difficult.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 90 Стабильный | 89,9046977 ± 0,000002 | 51.4500% ± 0.4000% | Стабильный | stable | |
| 91 Стабильный | 90,9056396 ± 0,000002 | 11.2200% ± 0.0500% | Стабильный | stable | |
| 92 Стабильный | 91,9050347 ± 0,000002 | 17.1500% ± 0.0800% | Стабильный | stable |
Спектральные линии
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 382.0196 нм | 5 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 382.4611 нм | 250 | Zr III | emission | 4d.4f 3H* → 4d.(2D<3/2>).5g 2[9/2] | Измерено | NIST | |
| 382.7722 нм | 300 | Zr III | emission | 4d.4f 3F* → 4d.(2D<3/2>).5g 2[7/2] | Измерено | NIST | |
| 382.923 нм | 600 | Zr III | emission | 4d.4f 3H* → 4d.(2D<3/2>).5g 2[11/2] | Измерено | NIST | |
| 383.0087 нм | 250 | Zr III | emission | 4d.4f 1D* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 383.7038 нм | 10 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 384.2399 нм | 270 | Zr III | emission | 4d.4f 3F* → 4d.(2D<3/2>).5g 2[9/2] | Измерено | NIST | |
| 390.7626 нм | 5 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 391.0786 нм | 3 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[13/2] | Измерено | NIST | |
| 391.6928 нм | 100 | Zr III | emission | 4d.4f 3F* → 4d.(2D<3/2>).5g 2[9/2] | Измерено | NIST | |
| 392.0624 нм | 400 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[11/2] | Измерено | NIST | |
| 392.5804 нм | 200 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 392.694 нм | 120 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 393.1478 нм | 100 | Zr III | emission | 5s.5p 3P* → 4d.5d 3S | Измерено | NIST | |
| 396.3178 нм | 500 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[11/2] | Измерено | NIST | |
| 396.5231 нм | 10 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[11/2] | Измерено | NIST | |
| 397.1691 нм | 200 | Zr III | emission | 4d.4f 3G* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 397.3984 нм | 220 | Zr III | emission | 4d.4f 1D* → 4d.(2D<3/2>).5g 2[5/2] | Измерено | NIST | |
| 398.854 нм | 10 | Zr III | emission | 4d.4f 3D* → 4d.(2D<5/2>).5g 2[5/2] | Измерено | NIST | |
| 401.632 нм | 20 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[7/2] | Измерено | NIST | |
| 401.6949 нм | 35 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[7/2] | Измерено | NIST | |
| 401.7561 нм | 3 | Zr III | emission | 4d.4f 1F* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 401.8142 нм | 140 | Zr III | emission | 4d.4f 1F* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 403.2482 нм | 400 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[9/2] | Измерено | NIST | |
| 403.3591 нм | 180 | Zr III | emission | 4d.4f 3D* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 403.6779 нм | 200 | Zr III | emission | 4d.4f 1F* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 408.0264 нм | 5 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[11/2] | Измерено | NIST | |
| 408.7114 нм | 150 | Zr III | emission | 4d.4f 3D* → 4d.(2D<5/2>).5g 2[5/2] | Измерено | NIST | |
| 412.5432 нм | 200 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[11/2] | Измерено | NIST | |
| 412.6379 нм | 400 | Zr III | emission | 4d.4f 3D* → 4d.(2D<5/2>).5g 2[7/2] | Измерено | NIST | |
| 413.2087 нм | 200 | Zr III | emission | 4d.4f 3G* → 4d.(2D<3/2>).5g 2[9/2] | Измерено | NIST | |
| 413.7442 нм | 500 | Zr IV | emission | 4p6.5d 2D → 4p6.6p 2P* | Измерено | NIST | |
| 414.6654 нм | 20 | Zr III | emission | 4d.4f 3D* → 4d.(2D<5/2>).5g 2[9/2] | Измерено | NIST | |
| 415.3368 нм | 2 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[3/2] | Измерено | NIST | |
| 416.0827 нм | 250 | Zr III | emission | 4d.4f 3D* → 4d.(2D<3/2>).5g 2[5/2] | Измерено | NIST | |
| 416.5293 нм | 15 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[5/2] | Измерено | NIST | |
| 417.1353 нм | 20 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[3/2] | Измерено | NIST | |
| 417.2872 нм | 300 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[5/2] | Измерено | NIST | |
| 419.3504 нм | 275 | Zr III | emission | 4d.4f 3D* → 4d.(2D<3/2>).5g 2[5/2] | Измерено | NIST | |
| 419.7309 нм | 15 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[3/2] | Измерено | NIST | |
| 419.8266 нм | 3000 | Zr IV | emission | 4p6.5d 2D → 4p6.6p 2P* | Измерено | NIST | |
| 420.3546 нм | 200 | Zr III | emission | 4d.4f 3P* → 4d.(2D<5/2>).5g 2[5/2] | Измерено | NIST | |
| 423.5695 нм | 275 | Zr III | emission | 4d.4f 1F* → 4d.(2D<3/2>).5g 2[7/2] | Измерено | NIST | |
| 431.7077 нм | 2000 | Zr IV | emission | 4p6.5d 2D → 4p6.6p 2P* | Измерено | NIST | |
| 434.2686 нм | 400 | Zr III | emission | 4d.4f 1H* → 4d.(2D<5/2>).5g 2[13/2] | Измерено | NIST | |
| 440.7385 нм | 20 | Zr III | emission | 4d.4f 1H* → 4d.(2D<5/2>).5g 2[11/2] | Измерено | NIST | |
| 456.1637 нм | 50 | Zr III | emission | 4d.4f 1P* → 4d.(2D<5/2>).5g 2[3/2] | Измерено | NIST | |
| 456.922 нм | 1800 | Zr IV | emission | 4p6.5g 2G → 4p6.6h 2H* | Измерено | NIST | |
| 456.927 нм | 1800 | Zr IV | emission | 4p6.5g 2G → 4p6.6h 2H* | Измерено | NIST | |
| 460.8973 нм | 60 | Zr III | emission | 4d.4f 1H* → 4d.(2D<3/2>).5g 2[11/2] | Измерено | NIST | |
| 500.71 нм | N/A | ID 803 | emission | 2p 2P* → 2s 2S | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 2127.15 K |
| Температура кипения | 4679.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (10)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.841 |
| 2 | p | 4.0072 |
| 2 | s | 10.6262 |
| 3 | d | 14.4331 |
| 3 | p | 16.1545 |
| 3 | s | 15.6385 |
| 4 | d | 26.9284 |
| 4 | p | 26.54 |
| 4 | s | 25.0984 |
| 5 | s | 33.5545 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 4 | IV | 73 | from r^3 vs V plots, | |
| 4 | V | 80 | calculated, | |
| 4 | VI | 86 | from r^3 vs V plots, | |
| 4 | VII | 92 | ||
| 4 | VIII | 98 | ||
| 4 | IX | 103 |
Режимы распада изотопов (56)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 77 | B+ | — |
| 77 | B+p | — |
| 77 | p | — |
| 78 | B+ | — |
| 78 | B+p | — |
| 79 | B+ | 100% |
| 79 | B+p | — |
| 80 | B+ | 100% |
| 81 | B+ | 100% |
| 81 | B+p | 0.1% |
Факторы рассеяния X‑лучей (724)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 1 | — | 0.18706 |
| 1.0149 | — | 0.19051 |
| 1.0299 | — | 0.19402 |
| 1.0452 | — | 0.1976 |
| 1.0608 | — | 0.20124 |
| 1.0765 | — | 0.20499 |
| 1.0925 | — | 0.20885 |
| 1.1087 | — | 0.21277 |
| 1.1252 | — | 0.21677 |
| 1.142 | — | 0.22085 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
1.65×102 milligrams per kilogram
Источники (1)
- [5] Zirconium https://education.jlab.org/itselemental/ele040.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
3×10-5 milligrams per liter
Источники (1)
- [5] Zirconium https://education.jlab.org/itselemental/ele040.html
Sources
Sources of this element.
Zirconium is produced from the mineral zircon (ZrSiO4). It is found in abundance in S-type stars, and has been identified in the sun and meteorites. Analysis of lunar rock samples obtained during the various Apollo missions to the moon show a surprisingly high zirconium oxide content, compared with terrestrial rocks.
Источники (1)
- [6] Zirconium https://periodic.lanl.gov/40.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Zirconium.
The element property data was retrieved from publications.