Стронций (Sr)
Щелочноземельный металлТвёрдое тело
Стандартный атомный вес
87.62 uЭлектронная конфигурация
[Kr] 5s2Температура плавления
776.85 °C (1050 K)Температура кипения
1381.85 °C (1655 K)Плотность
2640 kg/m³Степени окисления
+1, +2Электроотрицательность (Полинг)
0.95Энергия ионизации (1-я)
Год открытия
1792Атомный радиус
200 pmДополнительно
Стронций — щелочноземельный металл, расположенный в группе 2 ниже кальция и выше бария. Природный стронций стабилен и встречается главным образом в минералах целестине и стронцианите, а не в виде свободного металла. Его химия определяется ионом Sr²⁺, который близок к Ca²⁺, но крупнее и легче образует нерастворимые сульфатные и карбонатные соли. Стронций наиболее известен в технологическом отношении благодаря красной пиротехнической окраске, ферритовым магнитам, стеклянным добавкам и радиоактивному изотопу ⁹⁰Sr.
Стронций мягче кальция и более энергично разлагает воду. Он не поглощает азот ниже 380°C. Его следует хранить под керосином для предотвращения окисления. Свежесрезанный стронций имеет серебристый вид, но быстро приобретает желтоватую окраску вследствие образования оксида. Мелкоизмельчённый металл самовоспламеняется на воздухе. Летучие соли стронция придают пламени красивую малиновую окраску, и эти соли используются в пиротехнике и при производстве сигнальных огней. Природный стронций представляет собой смесь четырёх стабильных изотопов.
Название происходит от Стронтиана, города в Шотландии. Минерал стронцианит встречается в рудниках Стронтиана. Элемент был открыт в 1792 году шотландским химиком и врачом Томасом Чарльзом Хоупом, который наблюдал ярко-красную окраску пламени стронция. Впервые он был выделен в 1808 году английским химиком Хамфри Дэви.
Стронций был открыт ирландским химиком Адаром Кроуфордом в 1790 году при изучении минерала витерита (BaCO3). Когда он смешал витерит с соляной кислотой (HCl), он не получил ожидаемого результата. Он предположил, что его образец витерита был загрязнён неизвестным минералом, который он назвал стронцианитом (SrCO3). Стронций был впервые выделен сэром Хамфри Дэви, английским химиком, в 1808 году посредством электролиза смеси хлорида стронция (SrCl2) и оксида ртути (HgO). Сегодня стронций получают из двух его наиболее распространённых руд — целестина (SrSO4) и стронцианита (SrCO3) — путём обработки их соляной кислотой с образованием хлорида стронция. Затем хлорид стронция, обычно смешанный с хлоридом калия (KCl), расплавляют и подвергают электролизу, образуя стронций и газообразный хлор (Cl2).
Назван в честь Стронтиана, города в Шотландии. Выделен Дэви электролизом в 1808 году; однако Адар Кроуфорд в 1790 году распознал новый минерал (стронцианит) как отличающийся от других бариевых минералов.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
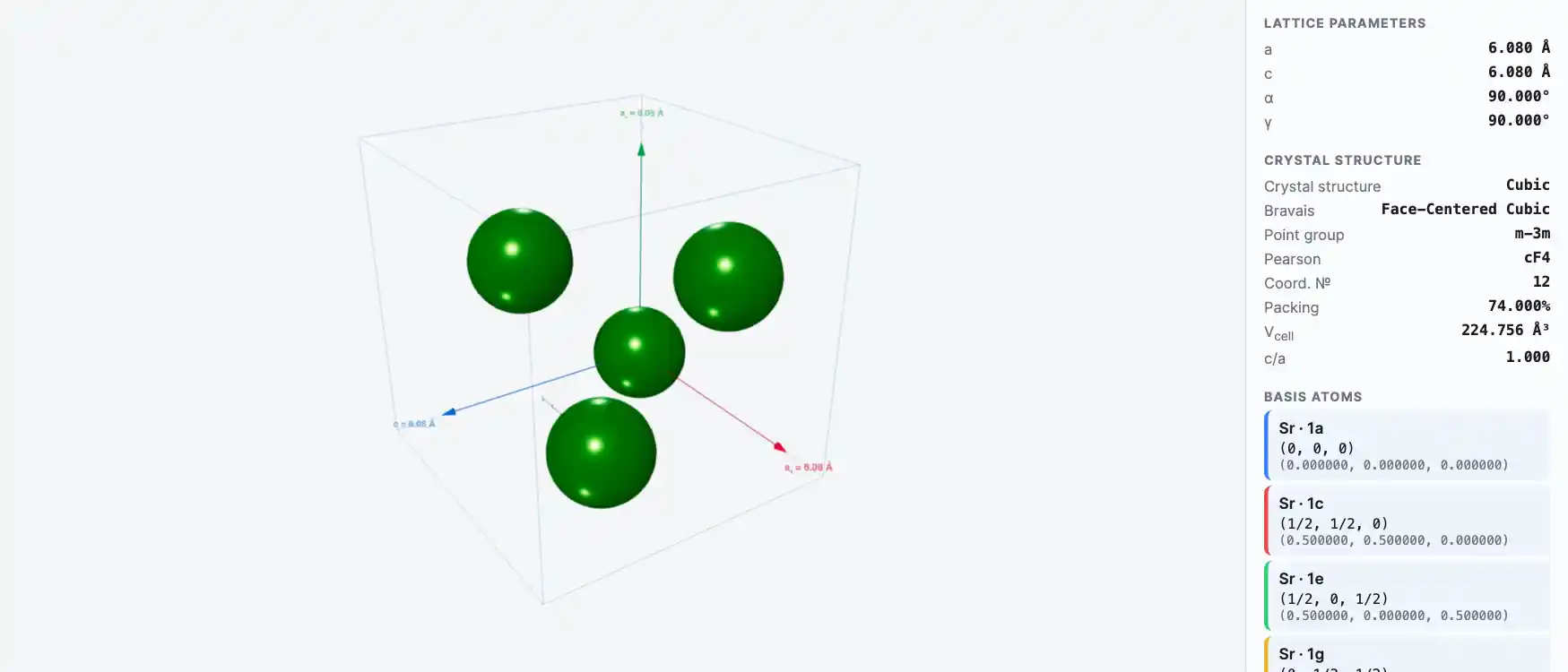
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Sr: 5s²[Kr] 5s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 5s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 84 Стабильный | 83,9134191 ± 0,0000013 | 0.5600% | Стабильный |
| 86 Стабильный | 85,9092606 ± 0,0000012 | 9.8600% | Стабильный |
| 87 Стабильный | 86,9088775 ± 0,0000012 | 7.0000% | Стабильный |
| 88 Стабильный | 87,9056125 ± 0,0000012 | 82.5800% | Стабильный |
Фазовое состояние
Причина: на 751.9 °C ниже точки плавления (776.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 38 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Sr I | 0 | 361 | 86 | 361 |
| Sr II | +1 | 135 | 33 | 135 |
| Sr III | +2 | 613 | 0 | 613 |
| Sr IV | +3 | 1183 | 0 | 1183 |
| Sr V | +4 | 625 | 0 | 625 |
| Sr VI | +5 | 57 | 14 | 57 |
| Sr VII | +6 | 30 | 30 | 30 |
| Sr VIII | +7 | 26 | 24 | 26 |
| Sr IX | +8 | 46 | 28 | 46 |
| Sr X | +9 | 54 | 51 | 54 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Sr I | 0 | 380 |
| Sr II | +1 | 72 |
| Sr III | +2 | 150 |
| Sr IV | +3 | 255 |
| Sr V | +4 | 144 |
| Sr VI | +5 | 22 |
| Sr VII | +6 | 20 |
| Sr VIII | +7 | 21 |
| Sr IX | +8 | 31 |
| Sr X | +9 | 47 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +2 | 6 | N/A | 118 пм |
| +2 | 7 | N/A | 121 пм |
| +2 | 8 | N/A | 126 пм |
| +2 | 9 | N/A | 131 пм |
| +2 | 10 | N/A | 136 пм |
| +2 | 12 | N/A | 144 пм |
Соединения
Изотопы (4)
Sixteen other unstable isotopes are known to exist. Of greatest importance is 90Sr with a half-life of 29 years. It is a product of nuclear fallout and presents a health problem. This isotope is one of the best long-lived high-energy beta emitters known, and is used in SNAP (Systems for Nuclear Auxilliary Power) devices. These devices hold promise for use in space vehicles, remote weather stations, navigational buoys, etc., and where a lightweight, long-lived, nuclear-electric power source is needed.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 84 Стабильный | 83,9134191 ± 0,0000013 | 0.5600% ± 0.0100% | Стабильный | stable | |
| 86 Стабильный | 85,9092606 ± 0,0000012 | 9.8600% ± 0.0100% | Стабильный | stable | |
| 87 Стабильный | 86,9088775 ± 0,0000012 | 7.0000% ± 0.0100% | Стабильный | stable | |
| 88 Стабильный | 87,9056125 ± 0,0000012 | 82.5800% ± 0.0100% | Стабильный | stable |
Спектральные линии
Показано 50 из 500 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 707.0072 нм | 14000 | Sr I | emission | 5s.5p 3P* → 5s.6s 3S | Измерено | NIST | |
| 687.83128 нм | 12000 | Sr I | emission | 5s.5p 3P* → 5s.6s 3S | Измерено | NIST | |
| 679.10198 нм | 7000 | Sr I | emission | 5s.5p 3P* → 5s.6s 3S | Измерено | NIST | |
| 525.68986 нм | 3400 | Sr I | emission | 5s.4d 3D → 4d.5p 3P* | Измерено | NIST | |
| 640.8463 нм | 3100 | Sr I | emission | 5s.4d 3D → 4d.5p 3F* | Измерено | NIST | |
| 483.20425 нм | 2900 | Sr I | emission | 5s.5p 3P* → 5s.5d 3D | Измерено | NIST | |
| 548.08638 нм | 2700 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST | |
| 496.2263 нм | 2500 | Sr I | emission | 5s.5p 3P* → 5s.5d 3D | Измерено | NIST | |
| 481.18799 нм | 2300 | Sr I | emission | 5s.5p 3P* → 5p2 3P | Измерено | NIST | |
| 689.25894 нм | 2300 | Sr I | emission | 5s2 1S → 5s.5p 3P* | Измерено | NIST | |
| 650.3992 нм | 2100 | Sr I | emission | 5s.4d 3D → 4d.5p 3F* | Измерено | NIST | |
| 523.85479 нм | 2000 | Sr I | emission | 5s.4d 3D → 4d.5p 3P* | Измерено | NIST | |
| 550.4181 нм | 2000 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST | |
| 496.5585 нм | 1900 | Sr I | emission | 5s.5p 1P* → 5s.7d 1D | Измерено | NIST | |
| 516.5486 нм | 1800 | Sr I | emission | 5s.5p 1P* → 5s.8s 1S | Измерено | NIST | |
| 478.43198 нм | 1700 | Sr I | emission | 5s.5p 3P* → 5p2 3P | Измерено | NIST | |
| 552.1768 нм | 1700 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST | |
| 730.94166 нм | 1700 | Sr I | emission | 5s.4d 1D → 4d.5p 1D* | Измерено | NIST | |
| 472.22769 нм | 1600 | Sr I | emission | 5s.5p 3P* → 5p2 3P | Измерено | NIST | |
| 474.19221 нм | 1600 | Sr I | emission | 5s.5p 3P* → 5p2 3P | Измерено | NIST | |
| 478.3782 нм | 1500 | Sr I | emission | 5s.5p 1P* → 5s.9s 1S | Измерено | NIST | |
| 487.249 нм | 1500 | Sr I | emission | 5s.5p 3P* → 5s.5d 3D | Измерено | NIST | |
| 489.198 нм | 1500 | Sr I | emission | 5s.4d 3D → 5s.4f 3F* | Измерено | NIST | |
| 581.67702 нм | 1500 | Sr I | emission | 5s.4d 1D → 4d.5p 3P* | Измерено | NIST | |
| 468.8546 нм | 1400 | Sr I | emission | 5s.5p 1P* → 5s.8d 1D | Измерено | NIST | |
| 522.21992 нм | 1400 | Sr I | emission | 5s.4d 3D → 4d.5p 3P* | Измерено | NIST | |
| 522.51079 нм | 1400 | Sr I | emission | 5s.4d 3D → 4d.5p 3P* | Измерено | NIST | |
| 522.92697 нм | 1400 | Sr I | emission | 5s.4d 3D → 4d.5p 3P* | Измерено | NIST | |
| 555.6375 нм | 1400 | Sr I | emission | 5s.5p 1P* → 5s.6d 3D | Измерено | NIST | |
| 634.57265 нм | 1400 | Sr I | emission | 5s.4d 3D → 5s.6p 3P* | Измерено | NIST | |
| 655.0244 нм | 1400 | Sr I | emission | 5s.5p 1P* → 4d2 1D | Измерено | NIST | |
| 495.6274 нм | 1300 | Sr I | emission | 5s.5p 1P* → 5s.7d 3D | Измерено | NIST | |
| 638.64581 нм | 1300 | Sr I | emission | 5s.4d 3D → 5s.6p 3P* | Измерено | NIST | |
| 485.50448 нм | 1200 | Sr I | emission | 5s.4d 3D → 5s.4f 3F* | Измерено | NIST | |
| 486.87005 нм | 1200 | Sr I | emission | 5s.4d 3D → 5s.4f 3F* | Измерено | NIST | |
| 487.60745 нм | 1200 | Sr I | emission | 5s.5p 3P* → 5s.5d 3D | Измерено | NIST | |
| 496.7942 нм | 1200 | Sr I | emission | 5s.5p 3P* → 5s.5d 3D | Измерено | NIST | |
| 559.8159 нм | 1200 | Sr I | emission | 5s.4d 1D → 4d.5p 1F* | Измерено | NIST | |
| 458.29879 нм | 1100 | Sr I | emission | 5s.5p 1P* → 5s.10s 1S | Измерено | NIST | |
| 486.91724 нм | 1100 | Sr I | emission | 5s.4d 3D → 5s.4f 3F* | Измерено | NIST | |
| 489.2642 нм | 1100 | Sr I | emission | 5s.4d 3D → 5s.4f 3F* | Измерено | NIST | |
| 661.72651 нм | 1100 | Sr I | emission | 5s.4d 3D → 4d.5p 3F* | Измерено | NIST | |
| 403.03772 нм | 1000 | Sr I | emission | 5s.5p 3P* → 5s.6d 3D | Измерено | NIST | |
| 443.8043 нм | 1000 | Sr I | emission | 5s.5p 3P* → 5s.7s 3S | Измерено | NIST | |
| 446.32981 нм | 1000 | Sr I | emission | 5s.5p 1P* → 5s.11s 1S | Измерено | NIST | |
| 453.2375 нм | 1000 | Sr I | emission | 5s.5p 1P* → 5s.9d 1D | Измерено | NIST | |
| 471.2151 нм | 1000 | Sr I | emission | 5s.4d 1D → 5s.5f 3F* | Измерено | NIST | |
| 545.08373 нм | 1000 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST | |
| 548.6135 нм | 1000 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST | |
| 553.4799 нм | 1000 | Sr I | emission | 5s.4d 3D → 4d.5p 3D* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1050.15 K |
| Температура кипения | 1650.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (9)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.8089 |
| 2 | p | 3.9696 |
| 2 | s | 10.0982 |
| 3 | d | 15.2738 |
| 3 | p | 15.8324 |
| 3 | s | 15.3362 |
| 4 | p | 26.068 |
| 4 | s | 24.5556 |
| 5 | s | 31.9295 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 2 | VI | 132 | ||
| 2 | VII | 135 | ||
| 2 | VIII | 140 | ||
| 2 | IX | 145 | ||
| 2 | X | 150 | calculated, | |
| 2 | XII | 158 | calculated, |
Режимы распада изотопов (54)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 73 | B+ | 100% |
| 73 | B+p | 63% |
| 74 | B+ | 100% |
| 74 | B+p | — |
| 75 | B+ | 100% |
| 75 | B+p | 5.2% |
| 76 | B+ | 100% |
| 76 | B+p | 3.4% |
| 77 | B+ | 100% |
| 77 | B+p | 0.1% |
Факторы рассеяния X‑лучей (508)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.17126 |
| 10.1617 | — | 0.1749 |
| 10.3261 | — | 0.17861 |
| 10.4931 | — | 0.1824 |
| 10.6628 | — | 0.18627 |
| 10.8353 | — | 0.19061 |
| 11.0106 | — | 0.19514 |
| 11.1886 | — | 0.19977 |
| 11.3696 | — | 0.2045 |
| 11.5535 | — | 0.20936 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
3.70×102 milligrams per kilogram
Источники (1)
- [5] Strontium https://education.jlab.org/itselemental/ele038.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
7.9 milligrams per liter
Источники (1)
- [5] Strontium https://education.jlab.org/itselemental/ele038.html
Isotopes in Forensic Science and Anthropology
Information on the use of this element's isotopes in forensic science and anthropology.
The isotope-amount ratio n(87Sr)/n(86Sr) is highly variable in rocks, minerals, soils, and waters, and it can be transmitted to plants (Fig. IUPAC.38.1), animals, and manufactured materials. Measurements of n(87Sr)/n(86Sr) ratios are used for forensic applications in food authentication (determining where food came from), archaeology, crime-scene investigation, and human migration [298] [298] B. L. Beard, C. M. Johnson. J. Forensic Sci.45, 1049 (2000).[298] B. L. Beard, C. M. Johnson. J. Forensic Sci.45, 1049 (2000)., [299] [299] K. M. Frei, R. Frei. Appl. Geochem.26, 326 (2011).[299] K. M. Frei, R. Frei. Appl. Geochem.26, 326 (2011)..
Источники (4)
- [298] B. L. Beard, C. M. Johnson. J. Forensic Sci.45, 1049 (2000).
- [299] K. M. Frei, R. Frei. Appl. Geochem.26, 326 (2011).
- [300] K. Miller, T. B. Coplen, M. Wieser. “Identification of the geographical origin of exotic wood species using 87Sr/86Sr isotope amount ratios”, in Goldschmidt 22nd Conference, Montreal, Quebec, Canada.
- [4] IUPAC Periodic Table of the Elements and Isotopes (IPTEI) https://doi.org/10.1515/pac-2015-0703
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Strontium.
The element property data was retrieved from publications.