Цинк (Zn)
Переходный металлТвёрдое тело
Стандартный атомный вес
65.38 uЭлектронная конфигурация
[Ar] 4s2 3d10Температура плавления
419.53 °C (692.68 K)Температура кипения
906.85 °C (1180 K)Плотность
7134 kg/m³Степени окисления
−2, 0, +1, +2Электроотрицательность (Полинг)
1.65Энергия ионизации (1-я)
Год открытия
1746Атомный радиус
135 pmДополнительно
Цинк — умеренно реакционноспособный голубовато-белый переходный металл с заполненной 3d-оболочкой, химия которого определяется степенью окисления +2. Он является необходимым микроэлементом для живых организмов и важным промышленным металлом, особенно для защиты стали от коррозии. В минералах он встречается главным образом в виде сульфидных и карбонатных руд, а в технологии ценится за жертвенное гальваническое поведение, образование сплавов и устойчивые, часто бесцветные соединения Zn²⁺.
Цинк — голубовато-белый, блестящий металл. При обычных температурах он хрупок, но при 100–150°C становится ковким. Он является достаточно хорошим проводником электричества и горит на воздухе при высокой краснокалильной температуре с выделением белых облаков оксида.
Он проявляет сверхпластичность. Ни цинк, ни цирконий не являются ферромагнитными; однако ZrZn2 проявляет ферромагнетизм при температурах ниже 35°K. Он обладает необычными электрическими, тепловыми, оптическими и твёрдофазными свойствами, которые ещё не были полностью исследованы.
Название происходит от немецкого zink неизвестного происхождения. Оно впервые использовалось в доисторические времена, когда его соединения применялись для заживления ран и больных глаз, а также для изготовления латуни. Цинк был признан металлом уже в 1374 году.
Хотя соединения цинка использовались по меньшей мере 2500 лет в производстве латуни, цинк был признан отдельным элементом значительно позже. Металлический цинк впервые был получен в Индии где-то в 1400-х годах путем нагревания минерала каламина (ZnCO3) с шерстью. Цинк был заново открыт Андреасом Сигизмундом Маргграфом в 1746 году путем нагревания каламина с древесным углем. Сегодня основную часть цинка получают электролизом водного раствора сульфата цинка (ZnSO4).
От немецкого слова Zink, неясного происхождения. За столетия до того, как цинк был признан отдельным элементом, цинковые руды использовали для изготовления латуни. Сплав, содержащий 87 процентов цинка, был найден в доисторических руинах в Трансильвании.
Металлический цинк был получен в XIII веке н. э. в Индии путем восстановления каламина органическими веществами, такими как шерсть. Металл был заново открыт в Европе Маргграфом в 1746 году. Он показал, что цинк можно получить восстановлением каламина древесным углем.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
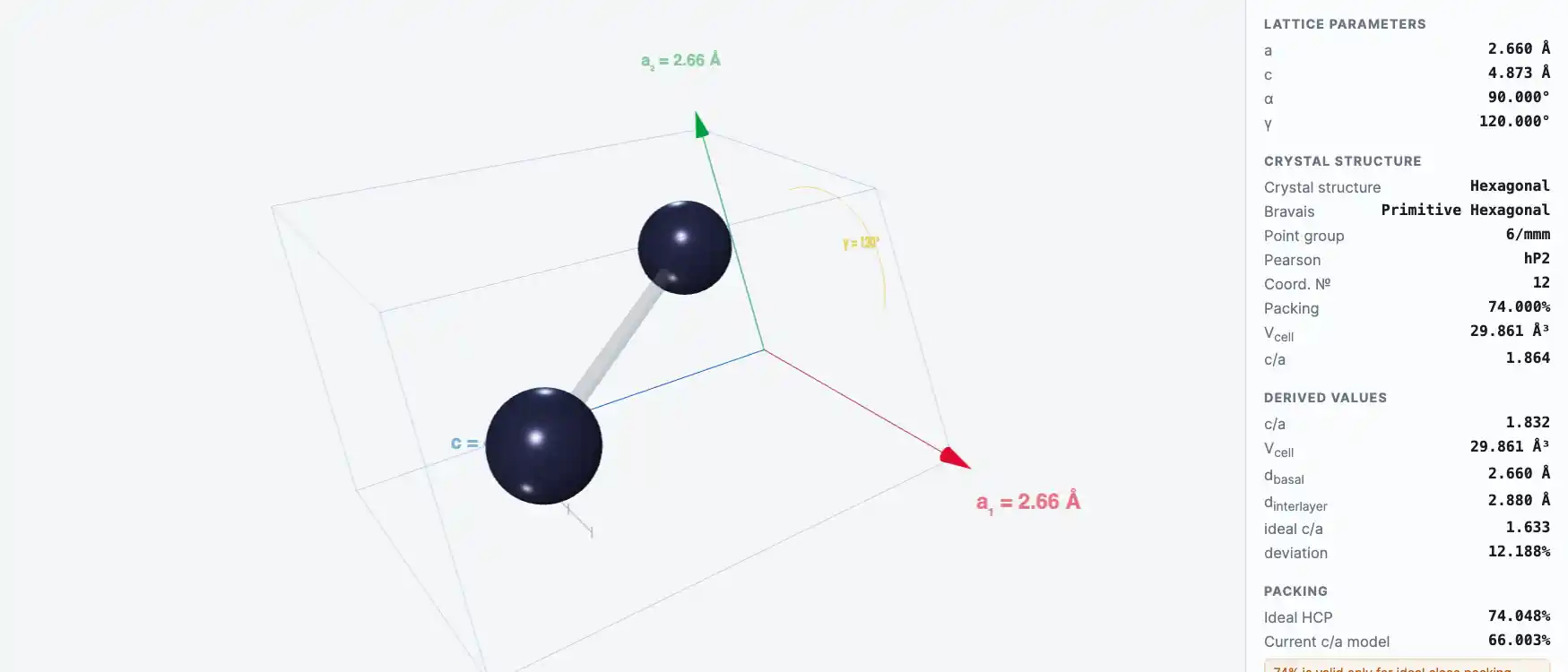
Кристаллическая структура
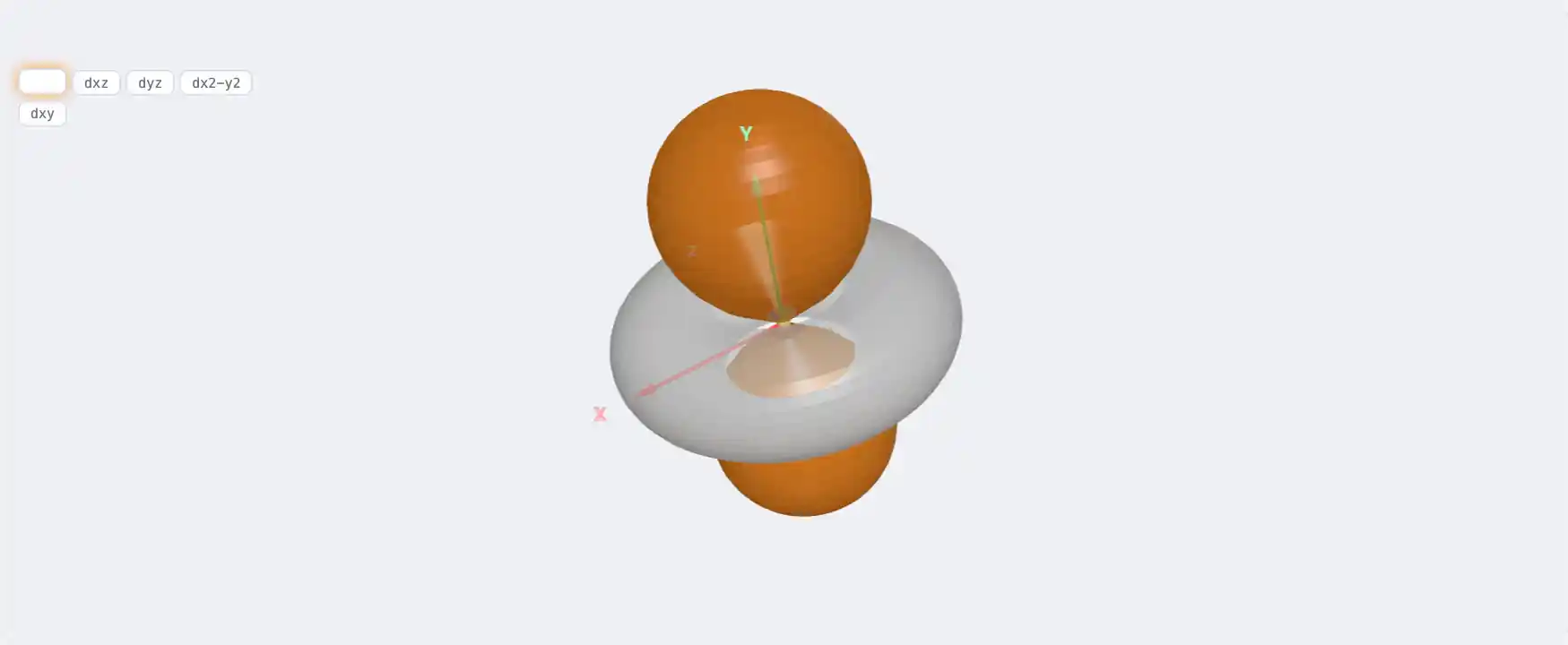
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Zn: 3d¹⁰ 4s²[Ar] 3d¹⁰ 4s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 66 Стабильный | 65,92603381 ± 0,00000094 | 27.7300% | Стабильный |
| 67 Стабильный | 66,92712775 ± 0,00000096 | 4.0400% | Стабильный |
| 68 Стабильный | 67,92484455 ± 0,00000098 | 18.4500% | Стабильный |
Фазовое состояние
Причина: на 394.5 °C ниже точки плавления (419.53 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 30 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Zn I | 0 | 570 | 16 | 564 |
| Zn II | +1 | 96 | 22 | 90 |
| Zn III | +2 | 39 | 0 | 0 |
| Zn IV | +3 | 119 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Zn I | 0 | 380 |
| Zn II | +1 | 94 |
| Zn III | +2 | 316 |
| Zn IV | +3 | 245 |
| Zn V | +4 | 158 |
| Zn VI | +5 | 193 |
| Zn VII | +6 | 134 |
| Zn VIII | +7 | 5 |
| Zn IX | +8 | 2 |
| Zn X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +2 | 4 | N/A | 60 пм |
| +2 | 5 | N/A | 68 пм |
| +2 | 6 | N/A | 74 пм |
| +2 | 8 | N/A | 90 пм |
Соединения
Изотопы (3)
Naturally occurring zinc contains five stable isotopes. Sixteen other unstable isotopes are recognized.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 66 Стабильный | 65,92603381 ± 0,00000094 | 27.7300% ± 0.9800% | Стабильный | stable | |
| 67 Стабильный | 66,92712775 ± 0,00000096 | 4.0400% ± 0.1600% | Стабильный | stable | |
| 68 Стабильный | 67,92484455 ± 0,00000098 | 18.4500% ± 0.6300% | Стабильный | stable |
Спектральные линии
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 387.9141 нм | N/A | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.7d 1D | Измерено | NIST | |
| 396.543 нм | 78000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.8s 1S | Измерено | NIST | |
| 411.31114 нм | 81000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.6d 1D | Измерено | NIST | |
| 429.2883 нм | 32000 | Zn I | emission | 3d10.4s.4p 3P* → 3d10.4s.5s 1S | Измерено | NIST | |
| 429.8325 нм | 49000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.7s 1S | Измерено | NIST | |
| 455.326 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.30p 1P* | Измерено | NIST | |
| 455.548 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.29p 1P* | Измерено | NIST | |
| 455.795 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.28p 1P* | Измерено | NIST | |
| 456.073 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.27p 1P* | Измерено | NIST | |
| 456.388 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.26p 1P* | Измерено | NIST | |
| 456.745 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.25p 1P* | Измерено | NIST | |
| 457.155 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.24p 1P* | Измерено | NIST | |
| 457.623 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.23p 1P* | Измерено | NIST | |
| 458.167 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.22p 1P* | Измерено | NIST | |
| 458.796 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.21p 1P* | Измерено | NIST | |
| 459.541 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.20p 1P* | Измерено | NIST | |
| 460.423 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.19p 1P* | Измерено | NIST | |
| 461.482 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.18p 1P* | Измерено | NIST | |
| 462.768 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.17p 1P* | Измерено | NIST | |
| 462.980809 нм | 390000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.5d 1D | Измерено | NIST | |
| 464.351 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.16p 1P* | Измерено | NIST | |
| 466.559 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.15p 3P* | Измерено | NIST | |
| 468.013589 нм | 540000 | Zn I | emission | 3d10.4s.4p 3P* → 3d10.4s.5s 3S | Измерено | NIST | |
| 469.143 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.14p 3P* | Измерено | NIST | |
| 472.215691 нм | 1000000 | Zn I | emission | 3d10.4s.4p 3P* → 3d10.4s.5s 3S | Измерено | NIST | |
| 472.527 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.13p 3P* | Измерено | NIST | |
| 477.071 нм | N/A | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.12p 3P* | Измерено | NIST | |
| 481.053206 нм | 1100000 | Zn I | emission | 3d10.4s.4p 3P* → 3d10.4s.5s 3S | Измерено | NIST | |
| 506.866 нм | 77000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.9p 3P* | Измерено | NIST | |
| 506.943 нм | 21000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.9p 3P* | Измерено | NIST | |
| 506.998 нм | 3300 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.9p 3P* | Измерено | NIST | |
| 518.19819 нм | 120000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.6s 1S | Измерено | NIST | |
| 530.866 нм | 380000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.8p 3P* | Измерено | NIST | |
| 531.017 нм | 160000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.8p 3P* | Измерено | NIST | |
| 531.101 нм | 56000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.8p 3P* | Измерено | NIST | |
| 577.205 нм | 490000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.7p 3P* | Измерено | NIST | |
| 577.5452 нм | 210000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.7p 3P* | Измерено | NIST | |
| 577.7033 нм | 85000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.7p 3P* | Измерено | NIST | |
| 623.78967 нм | 93000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.4d 3D | Измерено | NIST | |
| 623.9169 нм | 38000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.4d 3D | Измерено | NIST | |
| 636.23458 нм | 240000 | Zn I | emission | 3d10.4s.4p 1P* → 3d10.4s.4d 1D | Измерено | NIST | |
| 647.9184 нм | 55000 | Zn I | emission | 3d10.4s.5s 1S → 3d10.4s.7p 1P* | Измерено | NIST | |
| 692.8295 нм | 40000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.6p 3P* | Измерено | NIST | |
| 693.8449 нм | 20000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.6p 3P* | Измерено | NIST | |
| 694.3184 нм | 7000 | Zn I | emission | 3d10.4s.5s 3S → 3d10.4s.6p 3P* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 692.68 K |
| Температура кипения | 1180.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (7)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.6755 |
| 2 | p | 3.902 |
| 2 | s | 8.172 |
| 3 | d | 16.1217 |
| 3 | p | 14.6307 |
| 3 | s | 13.7808 |
| 4 | s | 24.0348 |
Детализация кристаллических радиусов (4)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 2 | IV | 74 | ||
| 2 | V | 82 | ||
| 2 | VI | 88 | from r^3 vs V plots, | |
| 2 | VIII | 104 | calculated, |
Режимы распада изотопов (49)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 54 | 2p | 87% |
| 55 | B+ | 100% |
| 55 | B+p | 91% |
| 56 | B+ | 100% |
| 56 | B+p | 88% |
| 57 | B+ | 100% |
| 57 | B+p | 87% |
| 58 | B+ | 100% |
| 58 | B+p | 0.7% |
| 59 | B+ | 100% |
Факторы рассеяния X‑лучей (504)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 2.21675 |
| 10.1617 | — | 2.11915 |
| 10.3261 | — | 2.02585 |
| 10.4931 | — | 1.93665 |
| 10.6628 | — | 1.85138 |
| 10.8353 | — | 1.76986 |
| 11.0106 | — | 1.69194 |
| 11.1886 | — | 1.63293 |
| 11.3696 | — | 1.57784 |
| 11.5535 | — | 1.5246 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
7.0×101 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
4.9×10-3 milligrams per liter
Источники (1)
Sources
Sources of this element.
The principal ores of zinc are sphalerite (sulfide), smithsonite (carbonate), calamine (silicate), and franklinite (zinc, manganese, iron oxide). One method of zinc extraction involves roasting its ores to form the oxide and reducing the oxide with coal or carbon, with subsequent distillation of the metal.
Источники (1)
- [6] Zinc https://periodic.lanl.gov/30.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Zinc.
The element property data was retrieved from publications.