Калий (K)
Щелочной металлТвёрдое тело
Стандартный атомный вес
39.0983 uЭлектронная конфигурация
[Ar] 4s1Температура плавления
63.38 °C (336.53 K)Температура кипения
758.85 °C (1032 K)Плотность
890 kg/m³Степени окисления
−1, +1Электроотрицательность (Полинг)
0.82Энергия ионизации (1-я)
Год открытия
1807Атомный радиус
220 pmДополнительно
Калий — щелочной металл и важный породообразующий и биологический элемент. В природе он встречается только в соединениях, главным образом в виде K⁺ в солях, полевых шпатах, слюдах и глинистых минералах. Металл сильно электроотрицателен, бурно реагирует с водой и хранится вдали от воздуха и влаги. В живых клетках калий является основным внутриклеточным катионом и играет центральную роль в осмотическом балансе и электрической сигнализации.
Это один из наиболее реакционноспособных и электроотрицательных металлов. За исключением лития, это самый лёгкий известный металл. Он мягкий, легко режется ножом и имеет серебристый вид сразу после обнажения свежей поверхности. Он быстро окисляется на воздухе и должен храниться в минеральном масле, таком как керосин.
Как и другие металлы щелочной группы, он разлагает воду с выделением водорода. Он самовоспламеняется на воде. Калий и его соли придают пламени фиолетовую окраску.
Название происходит от английского «potash» или «pot ashes», поскольку он содержится в едком поташе (KOH). Символ K происходит от латинского kalium через арабское qali — «щелочь». Впервые был выделен британским химиком Хамфри Дэви в 1807 году путем электролиза поташа (KOH).
Хотя калий является восьмым по распространенности элементом на Земле и составляет около 2,1% земной коры, это очень реакционноспособный элемент и в природе в свободном виде не встречается. Металлический калий впервые был выделен сэром Хамфри Дэви в 1807 году посредством электролиза расплавленного едкого поташа (KOH). Через несколько месяцев после открытия калия Дэви тем же методом выделил натрий. Калий можно получить из минералов сильвина (KCl), карналлита (KCl·MgCl2·6H2O), лангбейнита (K2Mg2(SO4)3) и полигалита (K2Ca2Mg(SO4)4·2H2O). Эти минералы часто встречаются в древних озерных и морских отложениях. Едкий поташ, еще один важный источник калия, в основном добывают в Германии, Нью-Мексико, Калифорнии и Юте. Чистый калий — мягкий, воскообразный металл, который легко режется ножом. Он реагирует с кислородом с образованием супероксида калия (KO2) и с водой с образованием гидроксида калия (KOH), водорода и тепла. Выделяется достаточно тепла, чтобы воспламенить водород. Чтобы предотвратить его реакцию с кислородом и водой в воздухе, образцы металлического калия обычно хранят под слоем минерального масла.
От английского слова potash — pot ashes; латинское kalium, арабское qali — щелочь. Открыт Дэви в 1807 году, который получил его из едкого поташа (KOH); это был первый металл, выделенный электролизом.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
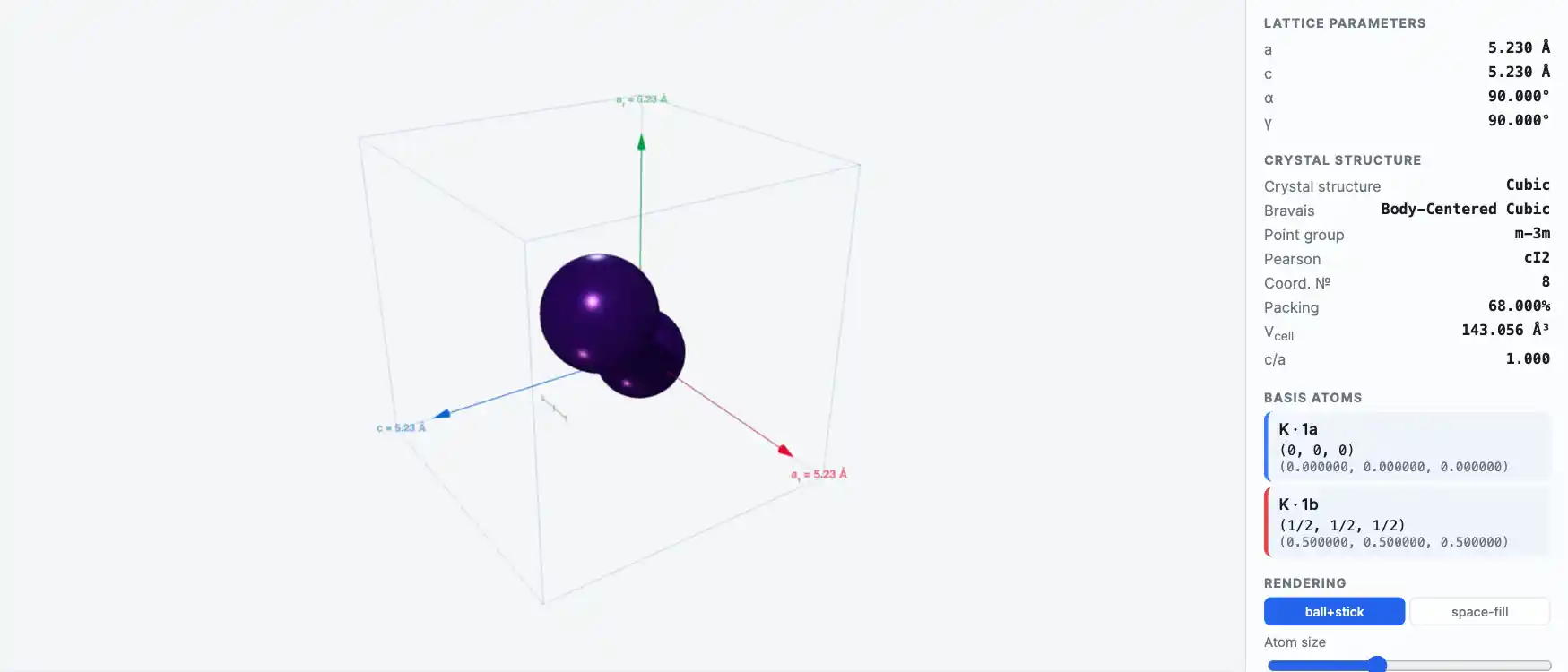
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
K: 4s¹[Ar] 4s¹1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 39 Стабильный | 38,9637064864 ± 0,0000000049 | 93.2581% | Стабильный |
| 41 Стабильный | 40,9618252579 ± 0,0000000041 | 6.7302% | Стабильный |
Фазовое состояние
Причина: на 38.4 °C ниже точки плавления (63.38 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 22 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| 41K I Изотоп | 0 | 8 |
| 40K I Изотоп | 0 | 3 |
| 39K I Изотоп | 0 | 123 |
| K I | 0 | 299 |
| K II | +1 | 97 |
| K III | +2 | 40 |
| K IV | +3 | 38 |
| K V | +4 | 40 |
| K VI | +5 | 28 |
| K VII | +6 | 81 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +1 | 4 | N/A | 137 пм |
| +1 | 6 | N/A | 138 пм |
| +1 | 7 | N/A | 146 пм |
| +1 | 8 | N/A | 151 пм |
| +1 | 9 | N/A | 155 пм |
| +1 | 10 | N/A | 159 пм |
| +1 | 12 | N/A | 164 пм |
Соединения
Изотопы (2)
Seventeen isotopes of potassium are known. Ordinary potassium is composed of three isotopes, one of which is 40°K (0.0118%), a radioactive isotope with a half-life of 1.28 x 109 years.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 39 Стабильный | 38,9637064864 ± 0,0000000049 | 93.2581% ± 0.0044% | Стабильный | stable | |
| 41 Стабильный | 40,9618252579 ± 0,0000000041 | 6.7302% ± 0.0044% | Стабильный | stable |
Спектральные линии
Показано 50 из 141 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 693.8764 нм | 20 | K I | emission | 3p6.4p 2P* → 3p6.6s 2S | Измерено | NIST | |
| 691.10815 нм | 19 | K I | emission | 3p6.4p 2P* → 3p6.6s 2S | Измерено | NIST | |
| 404.41422 нм | 18 | K I | emission | 3p6.4s 2S → 3p6.5p 2P* | Измерено | NIST | |
| 404.72132 нм | 17 | K I | emission | 3p6.4s 2S → 3p6.5p 2P* | Измерено | NIST | |
| 580.17662 нм | 17 | K I | emission | 3p6.4p 2P* → 3p6.7s 2S | Измерено | NIST | |
| 583.18899 нм | 17 | K I | emission | 3p6.4p 2P* → 3p6.5d 2D | Измерено | NIST | |
| 578.23999 нм | 16 | K I | emission | 3p6.4p 2P* → 3p6.7s 2S | Измерено | NIST | |
| 581.21521 нм | 15 | K I | emission | 3p6.4p 2P* → 3p6.5d 2D | Измерено | NIST | |
| 535.95761 нм | 14 | K I | emission | 3p6.4p 2P* → 3p6.6d 2D | Измерено | NIST | |
| 533.96873 нм | 13 | K I | emission | 3p6.4p 2P* → 3p6.8s 2S | Измерено | NIST | |
| 511.225448 нм | 12 | K I | emission | 3p6.4p 2P* → 3p6.7d 2D | Измерено | NIST | |
| 532.32786 нм | 12 | K I | emission | 3p6.4p 2P* → 3p6.8s 2S | Измерено | NIST | |
| 534.29693 нм | 12 | K I | emission | 3p6.4p 2P* → 3p6.6d 2D | Измерено | NIST | |
| 693.62861 нм | 12 | K I | emission | 3p6.4p 2P* → 3p6.4d 2D | Измерено | NIST | |
| 696.46903 нм | 12 | K I | emission | 3p6.4p 2P* → 3p6.4d 2D | Измерено | NIST | |
| 464.23725 нм | 11 | K I | emission | 3p6.4s 2S → 3p6.3d 2D | Измерено | NIST | |
| 509.717137 нм | 11 | K I | emission | 3p6.4p 2P* → 3p6.7d 2D | Измерено | NIST | |
| 509.920005 нм | 11 | K I | emission | 3p6.4p 2P* → 3p6.9s 2S | Измерено | NIST | |
| 464.1875 нм | 10 | K I | emission | 3p6.4s 2S → 3p6.3d 2D | Измерено | NIST | |
| 496.503213 нм | 10 | K I | emission | 3p6.4p 2P* → 3p6.8d 2D | Измерено | NIST | |
| 508.423399 нм | 10 | K I | emission | 3p6.4p 2P* → 3p6.9s 2S | Измерено | NIST | |
| 482.924 нм | 9 | K II | emission | 3p5.4s 3P* → 3p5.4p 3S | Измерено | NIST | |
| 486.975897 нм | 9 | K I | emission | 3p6.4p 2P* → 3p6.9d 2D | Измерено | NIST | |
| 495.081801 нм | 9 | K I | emission | 3p6.4p 2P* → 3p6.8d 2D | Измерено | NIST | |
| 495.614802 нм | 9 | K I | emission | 3p6.4p 2P* → 3p6.10s 2S | Измерено | NIST | |
| 389.7896 нм | 8 | K II | emission | 3p5.4s 3P* → 3p5.4p 1D | Измерено | NIST | |
| 418.6232 нм | 8 | K II | emission | 3p5.4s 3P* → 3p5.4p 3D | Измерено | NIST | |
| 460.849 нм | 8 | K II | emission | 3p5.4s 1P* → 3p5.4p 1D | Измерено | NIST | |
| 480.43395 нм | 8 | K I | emission | 3p6.4p 2P* → 3p6.10d 2D | Измерено | NIST | |
| 485.609209 нм | 8 | K I | emission | 3p6.4p 2P* → 3p6.9d 2D | Измерено | NIST | |
| 486.348075 нм | 8 | K I | emission | 3p6.4p 2P* → 3p6.11s 2S | Измерено | NIST | |
| 500.564 нм | 8 | K II | emission | 3p5.4s 3P* → 3p5.4p 3S | Измерено | NIST | |
| 612.028 нм | 8 | K II | emission | 3p5.3d 3F* → 3p5.4p 3D | Измерено | NIST | |
| 381.7547 нм | 7 | K II | emission | 3p5.4p 3D → 3p5.(2P*<3/2>).5s 2[3/2]* | Измерено | NIST | |
| 400.122 нм | 7 | K II | emission | 3p5.4s 3P* → 3p5.4p 3P | Измерено | NIST | |
| 413.4705 нм | 7 | K II | emission | 3p5.4s 3P* → 3p5.4p 3D | Измерено | NIST | |
| 422.296 нм | 7 | K II | emission | 3p5.4s 1P* → 3p5.4p 3P | Измерено | NIST | |
| 422.566 нм | 7 | K II | emission | 3p5.3d 3P* → 3p5.4p 1D | Измерено | NIST | |
| 426.334 нм | 7 | K II | emission | 3p5.4s 3P* → 3p5.4p 3D | Измерено | NIST | |
| 430.498 нм | 7 | K II | emission | 3p5.3d 3P* → 3p5.4p 1D | Измерено | NIST | |
| 430.911 нм | 7 | K II | emission | 3p5.4s 1P* → 3p5.4p 3P | Измерено | NIST | |
| 438.816 нм | 7 | K II | emission | 3p5.4s 1P* → 3p5.4p 1P | Измерено | NIST | |
| 475.737719 нм | 7 | K I | emission | 3p6.4p 2P* → 3p6.11d 2D | Измерено | NIST | |
| 479.104132 нм | 7 | K I | emission | 3p6.4p 2P* → 3p6.10d 2D | Измерено | NIST | |
| 484.98645 нм | 7 | K I | emission | 3p6.4p 2P* → 3p6.11s 2S | Измерено | NIST | |
| 505.625 нм | 7 | K II | emission | 3p5.3d 3P* → 3p5.4p 3S | Измерено | NIST | |
| 630.728 нм | 7 | K II | emission | 3p5.3d 3F* → 3p5.4p 3D | Измерено | NIST | |
| 696.41712 нм | 7 | K I | emission | 3p6.4p 2P* → 3p6.4d 2D | Измерено | NIST | |
| 380.0162 нм | 6 | K II | emission | 3p5.4p 3D → 3p5.(2P*<3/2>).5s 2[3/2]* | Измерено | NIST | |
| 381.657 нм | 6 | K II | emission | 3p5.4p 3P → 3p5.4d 3P* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 336.65 K |
| Температура кипения | 1032.15 K |
| Критическая точка (температура) | 2223.15 K |
| Критическая точка (давление) | 16 MPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (6)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.5105 |
| 2 | p | 3.9728 |
| 2 | s | 5.9938 |
| 3 | p | 11.2744 |
| 3 | s | 10.3201 |
| 4 | s | 15.5048 |
Детализация кристаллических радиусов (7)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 1 | IV | 151 | ||
| 1 | VI | 152 | ||
| 1 | VII | 160 | ||
| 1 | VIII | 165 | ||
| 1 | IX | 169 | ||
| 1 | X | 173 | ||
| 1 | XII | 178 |
Режимы распада изотопов (53)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 31 | 3p | 100% |
| 32 | p | — |
| 33 | p | — |
| 34 | p | — |
| 35 | B+ | 100% |
| 35 | B+p | 0.4% |
| 36 | B+ | 100% |
| 36 | B+p | 0% |
| 36 | B+A | 0% |
| 37 | B+ | 100% |
Факторы рассеяния X‑лучей (503)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.03426 |
| 10.1617 | — | 0.03529 |
| 10.3261 | — | 0.03635 |
| 10.4931 | — | 0.03744 |
| 10.6628 | — | 0.03856 |
| 10.8353 | — | 0.03972 |
| 11.0106 | — | 0.04091 |
| 11.1886 | — | 0.04214 |
| 11.3696 | — | 0.0434 |
| 11.5535 | — | 0.04471 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.09×104 milligrams per kilogram
Источники (1)
- [5] Potassium https://education.jlab.org/itselemental/ele019.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
3.99×102 milligrams per liter
Источники (1)
- [5] Potassium https://education.jlab.org/itselemental/ele019.html
Sources
Sources of this element.
The metal is the seventh most abundant and makes up about 2.4% by weight of the earth's crust. Most potassium minerals are insoluble and the metal is obtained from them only with great difficulty.
Certain minerals, however, such as sylvite, carnallite, langbeinite, and polyhalite are found in ancient lake and sea beds and form rather extensive deposits from which potassium and its salts can readily be obtained. Potash is mined in Germany, New Mexico, California, Utah, and elsewhere. Large deposits of potash, found at a depth of some 3000 ft in Saskatchewan, promise to be important in coming years.
Potassium is also found in the ocean, but is present only in relatively small amounts, compared to sodium.
Источники (1)
- [6] Potassium https://periodic.lanl.gov/19.shtml
Production
Production of this element (from raw materials or other compounds containing the element).
Potassium is never found free in nature, but is obtained by electrolysis of the hydroxide, much in the same manner as prepared by Davy's first process. Thermal methods also are commonly used to produce potassium (such as by reduction of potassium compounds with CaC2, C, Si, or Na).
Источники (1)
- [6] Potassium https://periodic.lanl.gov/19.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Potassium.
The element property data was retrieved from publications.