Натрий (Na)
Щелочной металлТвёрдое тело
Стандартный атомный вес
22.989769 uЭлектронная конфигурация
[Ne] 3s1Температура плавления
97.8 °C (370.95 K)Температура кипения
882.85 °C (1156 K)Плотность
970 kg/m³Степени окисления
−1, 0, +1Электроотрицательность (Полинг)
0.93Энергия ионизации (1-я)
Год открытия
1807Атомный радиус
180 pmДополнительно
Натрий — мягкий, высокореакционноспособный щелочной металл группы 1. Он имеет один валентный электрон и почти всегда образует Na⁺ в обычных соединениях. Элемент широко распространен в морской воде, эвапоритовых отложениях и силикатных минералах, но в свободном виде в природе не встречается, поскольку легко реагирует с водой, кислородом и многими неметаллами. Его соли имеют центральное значение для физиологии, стекольного производства, моющих средств и крупнотоннажного химического производства.
Натрий, как и любой реакционноспособный элемент, никогда не встречается в природе в свободном виде. Натрий — мягкий, яркий, серебристый металл, плавающий на воде. Разложение в воде приводит к выделению водорода и образованию гидроксида. Он может самовоспламеняться на воде или не самовоспламеняться в зависимости от количества оксида и металла, подвергшихся воздействию воды. Обычно он не воспламеняется на воздухе при температурах ниже 115°C.
Название происходит от английского soda и латинского sodanum — «средство от головной боли». Символ Na происходит от латинского natrium — «натрон» (soda на английском). Натрий был открыт в 1807 году английским химиком Хамфри Дэви в результате электролиза каустической соды (NaOH).
Хотя натрий является шестым по распространенности элементом на Земле и составляет около 2,6% земной коры, он является очень реакционноспособным элементом и никогда не встречается в природе в свободном состоянии. Чистый натрий был впервые выделен сэром Хамфри Дэви в 1807 году посредством электролиза каустической соды (NaOH). Поскольку натрий может воспламеняться при контакте с водой, его необходимо хранить в условиях, исключающих влагу.
От английского слова soda; средневековое латинское sodanum: средство от головной боли. Давно известный в соединениях, натрий был впервые выделен Дэви в 1807 году электролизом каустической соды.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
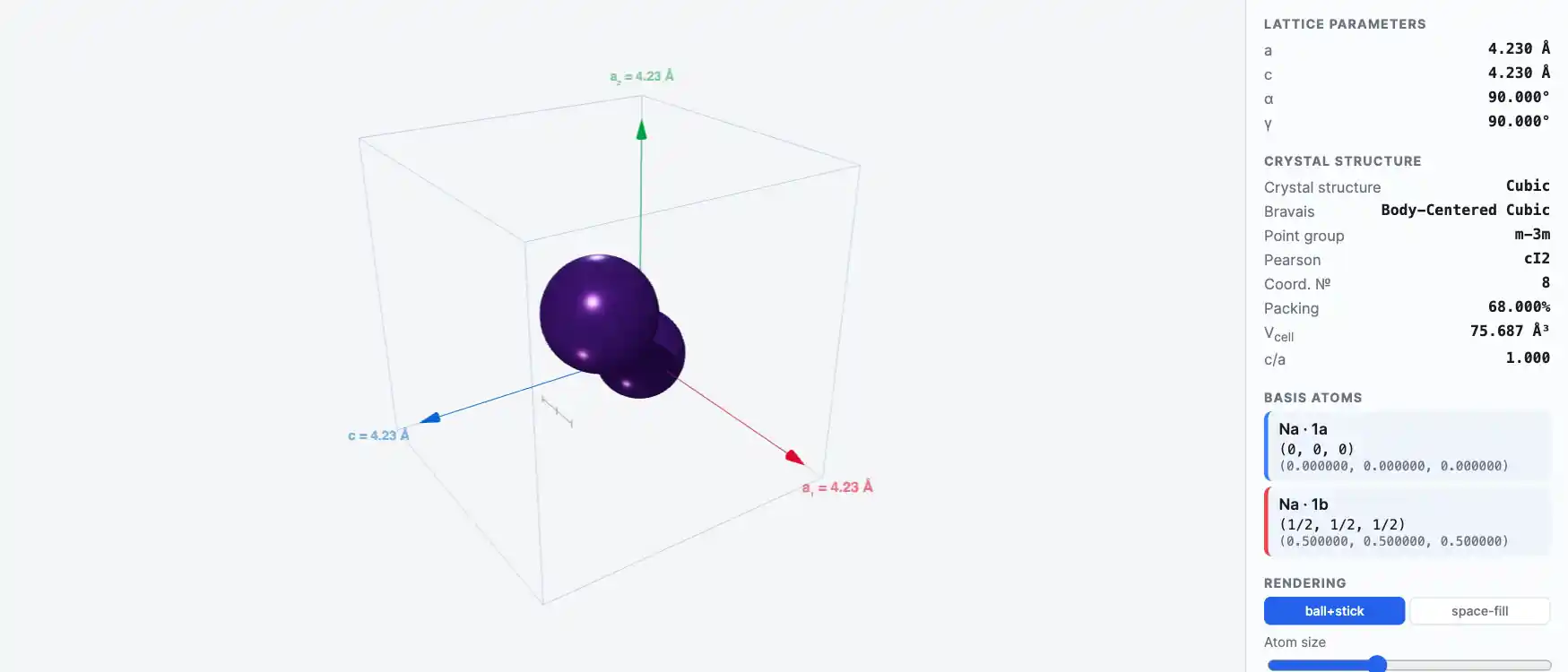
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Na: 3s¹[Ne] 3s¹1s² 2s² 2p⁶ 3s¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 23 Стабильный | 22,989769282 ± 0,0000000019 | 100.0000% | Стабильный |
Фазовое состояние
Причина: на 72.8 °C ниже точки плавления (97.8 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Дополнительно
Атомные спектры
Показано 10 из 11 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Na I | 0 | 869 | 523 | 858 |
| Na II | +1 | 1345 | 176 | 605 |
| Na III | +2 | 560 | 417 | 560 |
| Na IV | +3 | 687 | 671 | 687 |
| Na V | +4 | 529 | 503 | 527 |
| Na VI | +5 | 657 | 594 | 641 |
| Na VII | +6 | 1374 | 1369 | 1374 |
| Na VIII | +7 | 464 | 456 | 464 |
| Na IX | +8 | 172 | 138 | 172 |
| Na X | +9 | 594 | 586 | 594 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Na I | 0 | 430 |
| Na II | +1 | 165 |
| Na III | +2 | 120 |
| Na IV | +3 | 104 |
| Na V | +4 | 102 |
| Na VI | +5 | 116 |
| Na VII | +6 | 142 |
| Na VIII | +7 | 89 |
| Na IX | +8 | 46 |
| Na X | +9 | 111 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +1 | 4 | N/A | 99 пм |
| +1 | 5 | N/A | 100 пм |
| +1 | 6 | N/A | 102 пм |
| +1 | 7 | N/A | 112.00000000000001 пм |
| +1 | 8 | N/A | 118 пм |
| +1 | 9 | N/A | 124 пм |
| +1 | 12 | N/A | 139 пм |
Соединения
Изотопы (1)
Thirteen isotopes of sodium are recognized.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 23 Стабильный | 22,989769282 ± 0,0000000019 | 100.0000% | Стабильный | stable |
Спектральные линии
Показано 50 из 480 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 588.995094 нм | 80000 | Na I | emission | 2p6.3s 2S → 2p6.3p 2P* | Измерено | NIST | |
| 589.592424 нм | 40000 | Na I | emission | 2p6.3s 2S → 2p6.3p 2P* | Измерено | NIST | |
| 388.181 нм | 420 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4D → 2p5.3s.(3P*).3d 4F* | Измерено | NIST | |
| 443.234 нм | 310 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4S → 2p5.3s.(3P*).4s 4P* | Измерено | NIST | |
| 411.3703 нм | 300 | Na II | emission | 2s2.2p5.3p 1S → 2s2.2p5.(2P*<1/2>).3d 2[3/2]* | Измерено | NIST | |
| 507.12 нм | 270 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4D → 2p5.3s.(3P*).4s 4P* | Измерено | NIST | |
| 412.3069 нм | 250 | Na II | emission | 2s2.2p5.3p 1S → 2s2.2p5.(2P*<1/2>).4s 2[1/2]* | Измерено | NIST | |
| 423.335 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[7/2] | Измерено | NIST | |
| 424.09 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[7/2] | Измерено | NIST | |
| 429.249 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[1/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 429.287 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[1/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 430.882 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[1/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 430.904 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[1/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 432.091 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 433.729 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 434.412 нм | 250 | Na II | emission | 2s2.2p5.3p 1S → 2s2.2p5.(2P*<3/2>).4s 2[3/2]* | Измерено | NIST | |
| 439.281 нм | 250 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[9/2] | Измерено | NIST | |
| 408.1372 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[3/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 436.859 нм | 200 | Na II | emission | 2s2.2p5.3p 1S → 2s2.2p5.(2P*<3/2>).3d 2[3/2]* | Измерено | NIST | |
| 437.522 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 438.748 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 440.512 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[9/2] | Измерено | NIST | |
| 444.669 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 444.741 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[7/2] | Измерено | NIST | |
| 445.473 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 445.523 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<1/2>).4f 2[7/2] | Измерено | NIST | |
| 445.72 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).4s 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 447.463 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).4s 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 447.88 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[3/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 448.167 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 449.015 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 449.088 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 449.961 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 450.697 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 451.92 нм | 200 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[3/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST | |
| 452.497 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 453.331 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).4s 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 455.152 нм | 200 | Na II | emission | 2s2.2p5.(2P*<3/2>).4s 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[3/2] | Измерено | NIST | |
| 391.803 нм | 160 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4D → 2p5.3s.(3P*).3d 4F* | Измерено | NIST | |
| 438.42 нм | 160 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 439.63 нм | 160 | Na II | emission | 2s2.2p5.(2P*<3/2>).3d 2[7/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 459.094 нм | 160 | Na II | emission | 2s2.2p5.3p 1S → 2s2.2p5.(2P*<3/2>).3d 2[1/2]* | Измерено | NIST | |
| 472.23 нм | 160 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 473.113 нм | 160 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[7/2] | Измерено | NIST | |
| 474.163 нм | 160 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[5/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 476.892 нм | 160 | Na II | emission | 2s2.2p5.(2P*<1/2>).3d 2[3/2]* → 2s2.2p5.(2P*<3/2>).4f 2[5/2] | Измерено | NIST | |
| 418.546 нм | 150 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4P → 2p5.3s.(3P*).3d 4D* | Измерено | NIST | |
| 386.543 нм | 130 | Na I | emission | 2p5.(2P*).3s.3p.(3P*) 4D → 2p5.3s.(3P*).3d 4F* | Измерено | NIST | |
| 408.7593 нм | 130 | Na II | emission | 2s2.2p5.3s 1P* → 2s2.2p5.3p 3S | Измерено | NIST | |
| 420.2759 нм | 130 | Na II | emission | 2s2.2p5.(2P*<3/2>).4s 2[3/2]* → 2s2.2p5.(2P*<1/2>).4f 2[5/2] | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 370.94 K |
| Температура кипения | 1156.09 K |
| Критическая точка (температура) | 2573.15 K |
| Критическая точка (давление) | 35 MPa |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (4)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.3741 |
| 2 | p | 4.1982 |
| 2 | s | 4.4286 |
| 3 | s | 8.4926 |
Детализация кристаллических радиусов (7)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 1 | IV | 113 | ||
| 1 | V | 114 | ||
| 1 | VI | 116 | ||
| 1 | VII | 126 | ||
| 1 | VIII | 132 | ||
| 1 | IX | 138 | calculated, | |
| 1 | XII | 153 |
Режимы распада изотопов (47)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 17 | p | 100% |
| 18 | p | — |
| 19 | p | 100% |
| 20 | B+ | 100% |
| 20 | B+A | 25% |
| 21 | B+ | 100% |
| 22 | B+ | 100% |
| 22 | e+ | 90.6% |
| 22 | EC | 9.4% |
| 24 | B- | 100% |
Факторы рассеяния X‑лучей (504)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 0.01475 |
| 10.1617 | — | 0.01517 |
| 10.3261 | — | 0.01559 |
| 10.4931 | — | 0.01603 |
| 10.6628 | — | 0.01648 |
| 10.8353 | — | 0.01695 |
| 11.0106 | — | 0.01743 |
| 11.1886 | — | 0.01792 |
| 11.3696 | — | 0.01842 |
| 11.5535 | — | 0.01894 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
2.36×104 milligrams per kilogram
Источники (1)
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.08×104 milligrams per liter
Источники (1)
Sources
Sources of this element.
Sodium is present in fair abundance in the sun and stars. The D lines of sodium are among the most prominent in the solar spectrum. Sodium is the fourth most abundant element on earth, comprising about 2.6% of the earth's crust; it is the most abundant of the alkali group of metals.
It is now obtained commercially by the electrolysis of absolutely dry fused sodium chloride. This method is much cheaper than that of electrolyzing sodium hydroxide, as was used several years ago.
Источники (1)
- [6] Sodium https://periodic.lanl.gov/11.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Sodium.
The element property data was retrieved from publications.