Таллий (Tl)
Постпереходный металлТвёрдое тело
Стандартный атомный вес
204.38 u [204,382, 204,385]Электронная конфигурация
[Xe] 6s2 4f14 5d10 6p1Температура плавления
303.85 °C (577 K)Температура кипения
1472.85 °C (1746 K)Плотность
1.180000e+4 kg/m³Степени окисления
−5, −2, −1, +1, +2, +3Электроотрицательность (Полинг)
1.62Энергия ионизации (1-я)
Год открытия
1861Атомный радиус
190 pmДополнительно
Таллий — это мягкий постпереходный металл группы 13. Химически он примечателен устойчивостью степени окисления +1, что отражает эффект инертной пары и делает многие соли таллия(I) по размеру и растворимости похожими на соли щелочных металлов. Элемент редко встречается в рудах и обычно извлекается как побочный продукт переработки сульфидных минералов. Его высокая токсичность резко сократила прежнее потребительское и сельскохозяйственное применение.
При свежем доступе к воздуху таллий обладает металлическим блеском, но вскоре приобретает синевато-серый оттенок, по внешнему виду напоминая свинец. Если таллий оставить на воздухе, на нём образуется плотный оксидный слой, а в присутствии воды образуется гидрид. Металл очень мягок и ковок. Его можно резать ножом. Известны двадцать пять изотопных форм таллия с атомными массами от 184 до 210. Природный таллий представляет собой смесь двух изотопов. Сообщается, что ртутно-таллиевый сплав, образующий эвтектику при 8,5% таллия, замерзает при -60C, то есть примерно на 20 градусов ниже точки замерзания ртути.
Название происходит от греческого thallos, означающего «зелёный побег» или «веточка», из-за ярко-зелёной линии в его спектре. Таллий был открыт английским физиком и химиком Уильямом Круксом в 1861 году. Металлический таллий впервые был выделен французским химиком Клодом-Огюстом Лами в 1862 году.
Таллий был открыт спектроскопически сэром Уильямом Круксом, английским химиком, в 1861 году. Крукс получил осадок, оставшийся после производства серной кислоты (H2SO4), от своего друга. После удаления всего селена из этого осадка он исследовал его с помощью прибора, известного как спектроскоп, чтобы найти признаки теллура. Вместо жёлтых спектральных линий, характерных для теллура, он наблюдал ярко-зелёную линию, которой прежде никто никогда не видел. Он назвал новый элемент, дававший зелёную линию, таллием, по греческому слову, означающему «зелёная веточка», thallos. Образцы таллия он выделил в следующем году. Таллий встречается в минералах кроксите (CuThSe), лорандите (TlAsS2) и хатчинсоните ((Pb, Tl)2As5S9), но обычно его получают как побочный продукт производства серной кислоты или как побочный продукт переработки цинка либо свинца.
От греческого thallos, означающего зелёный побег или веточку. Таллий был открыт спектроскопически в 1861 году Круксом. Элемент был назван по красивой зелёной спектральной линии, по которой он был идентифицирован. Металл был выделен как Круксом, так и Лами в 1862 году примерно одновременно.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
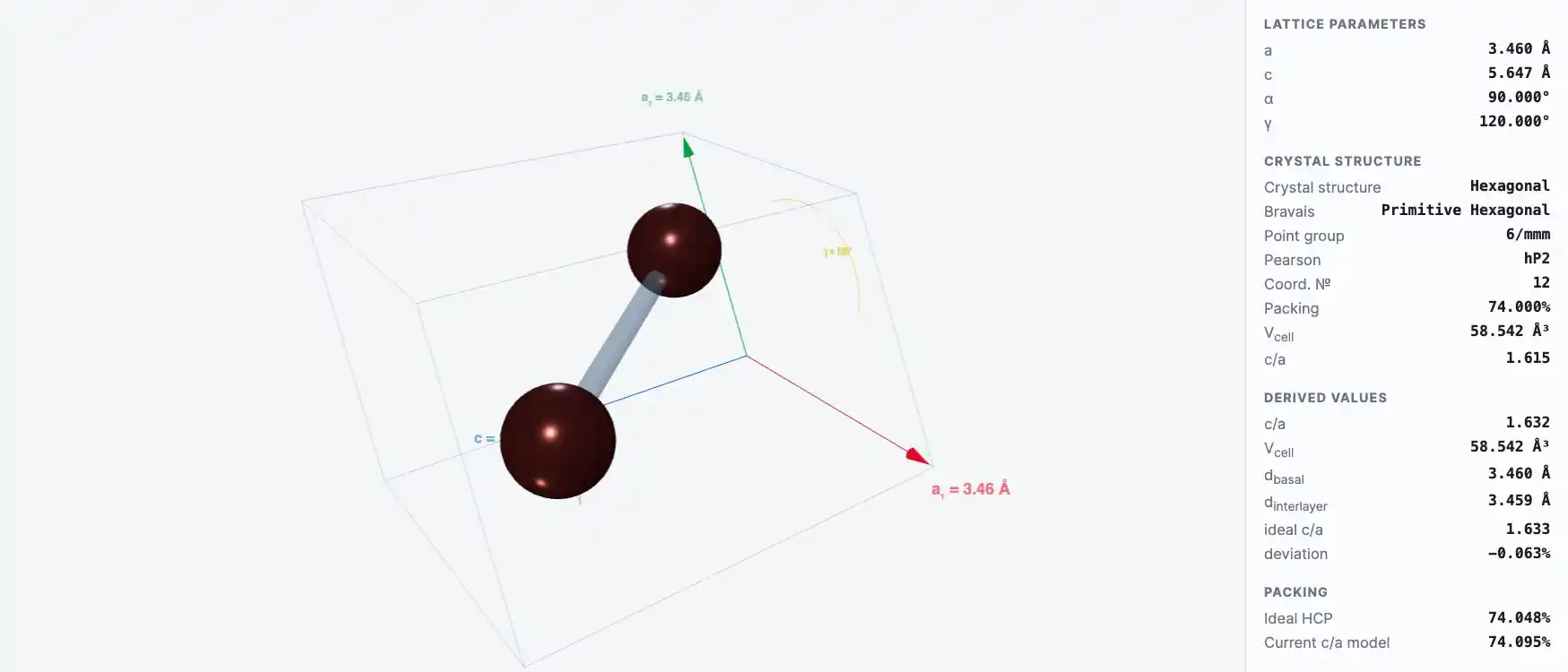
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Tl: 4f¹⁴ 5d¹⁰ 6s² 6p¹[Xe] 4f¹⁴ 5d¹⁰ 6s² 6p¹1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹⁰ 4s² 4p⁶ 4d¹⁰ 5s² 5p⁶ 4f¹⁴ 5d¹⁰ 6s² 6p¹Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 203 Стабильный | 202,9723446 ± 0,0000014 | 29.5200% | Стабильный |
| 205 Стабильный | 204,9744278 ± 0,0000014 | 70.4800% | Стабильный |
Фазовое состояние
Причина: на 278.9 °C ниже точки плавления (303.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 81 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Tl I | 0 | 65 | 25 | 11 |
| Tl II | +1 | 82 | 3 | 7 |
| Tl III | +2 | 22 | 0 | 0 |
| Tl IV | +3 | 35 | 0 | 0 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Tl I | 0 | 70 |
| Tl II | +1 | 82 |
| Tl III | +2 | 109 |
| Tl IV | +3 | 44 |
| Tl V | +4 | 2 |
| Tl VI | +5 | 2 |
| Tl VII | +6 | 2 |
| Tl VIII | +7 | 2 |
| Tl IX | +8 | 2 |
| Tl X | +9 | 2 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +1 | 6 | N/A | 150 пм |
| +1 | 8 | N/A | 159 пм |
| +1 | 12 | N/A | 170 пм |
| +3 | 4 | N/A | 75 пм |
| +3 | 6 | N/A | 88.5 пм |
| +3 | 8 | N/A | 98 пм |
Соединения
Изотопы (2)
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 203 Стабильный | 202,9723446 ± 0,0000014 | 29.5200% ± 0.0100% | Стабильный | stable | |
| 205 Стабильный | 204,9744278 ± 0,0000014 | 70.4800% ± 0.0100% | Стабильный | stable |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Параметры Мидемы
Фазовые переходы и аллотропы
| Температура плавления | 577.15 K |
| Температура кипения | 1746.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (15)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 1.5591 |
| 2 | p | 4.5138 |
| 2 | s | 21.3158 |
| 3 | d | 13.4658 |
| 3 | p | 22.6335 |
| 3 | s | 23.5809 |
| 4 | d | 37.6112 |
| 4 | f | 38.1324 |
| 4 | p | 35.7832 |
| 4 | s | 34.9212 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 1 | VI | 164 | from r^3 vs V plots, | |
| 1 | VIII | 173 | from r^3 vs V plots, | |
| 1 | XII | 184 | from r^3 vs V plots, estimated, | |
| 3 | IV | 89 | ||
| 3 | VI | 102.5 | from r^3 vs V plots, | |
| 3 | VIII | 112 | calculated, |
Режимы распада изотопов (69)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 176 | p | 100% |
| 176 | A | — |
| 176 | B+ | — |
| 177 | A | 73% |
| 177 | p | — |
| 178 | A | 62% |
| 178 | B+ | 38% |
| 178 | B+SF | 0.1% |
| 179 | A | 60% |
| 179 | B+ | — |
Факторы рассеяния X‑лучей (516)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.80392 |
| 10.1617 | — | 1.75555 |
| 10.3261 | — | 1.69589 |
| 10.4931 | — | 1.59546 |
| 10.6628 | — | 1.46625 |
| 10.8353 | — | 1.39341 |
| 11.0106 | — | 1.31349 |
| 11.1886 | — | 1.20783 |
| 11.3696 | — | 1.13261 |
| 11.5535 | — | 1.07387 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
8.5×10-1 milligrams per kilogram
Источники (1)
- [5] Thallium https://education.jlab.org/itselemental/ele081.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1.9×10-5 milligrams per liter
Источники (1)
- [5] Thallium https://education.jlab.org/itselemental/ele081.html
Sources
Sources of this element.
Thallium occurs in crooksite, lorandite, and hutchinsonite. It is also present in pyrites and is recovered from the roasting of this ore in connection with the production of sulfuric acid. It is also obtained from the smelting of lead and zinc ores. Extraction is somewhat complex and depends on the source of the thallium. Manganese nodules, found on the ocean floor, contain thallium.
Источники (1)
- [6] Thallium https://periodic.lanl.gov/81.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Thallium.
The element property data was retrieved from publications.