Титан (Ti)
Переходный металлТвёрдое тело
Стандартный атомный вес
47.867 uЭлектронная конфигурация
[Ar] 4s2 3d2Температура плавления
1667.85 °C (1941 K)Температура кипения
3286.85 °C (3560 K)Плотность
4500 kg/m³Степени окисления
−2, −1, 0, +1, +2, +3, +4Электроотрицательность (Полинг)
1.54Энергия ионизации (1-я)
Год открытия
1791Атомный радиус
140 pmДополнительно
Титан — лёгкий прочный переходный металл с высокой температурой плавления и исключительной устойчивостью к коррозии во многих природных и промышленных средах. Его химия определяется степенью окисления +4, хотя в специализированных соединениях встречаются +3 и более низкие степени. Металл распространён в земной коре, но редко встречается в концентрированной металлической форме, поскольку прочно связывается с кислородом и азотом. Сочетание низкой плотности, прочности и пассивации делает его важным для аэрокосмической отрасли, химического оборудования, пигментов и медицинских материалов.
Титан в чистом виде — блестящий белый металл. Он имеет низкую плотность, хорошую прочность, легко поддаётся обработке и обладает отличной коррозионной стойкостью. Он пластичен только тогда, когда свободен от кислорода. Металл, который горит на воздухе, — единственный элемент, который горит в азоте.
Титан устойчив к разбавленной серной и соляной кислотам, большинству органических кислот, большинству хлора и растворам хлоридов.
Сообщается, что природный титан становится очень радиоактивным после бомбардировки дейтронами. Испускаемое излучение в основном состоит из позитронов и жёстких гамма-лучей. Металл диморфен. Гексагональная альфа-форма очень медленно переходит в кубическую бета-форму примерно при 880°C. Металл соединяется с кислородом при красном калении и с хлором при 550°C.
Металлический титан считается физиологически инертным. В чистом виде диоксид титана относительно прозрачен и имеет чрезвычайно высокий показатель преломления с оптической дисперсией выше, чем у алмаза.
Название происходит от латинского titans, которые были мифологическими «первыми сыновьями земли». Впервые он был открыт английским священником Уильямом Грегором в минерале ильмените (FeTiO3) в 1791 году. Он назвал этот минерал менаханитом, а элемент — менахином, по приходу Менакан, где он был найден. Он был заново открыт в 1795 году немецким химиком Мартином Генрихом Клапротом, который назвал его титаном, поскольку он не обладал характерными свойствами, которые можно было бы использовать в качестве названия. Металлический титан впервые был выделен шведскими химиками Свеном Отто Петтерссоном и Ларсом Фредриком Нильсоном.
Титан был открыт в 1791 году преподобным Уильямом Грегором, английским пастором. Чистый титан впервые был получен Мэтью А. Хантером, американским металлургом, в 1910 году. Титан — девятый по распространенности элемент земной коры и в основном встречается в минералах рутиле (TiO2), ильмените (FeTiO3) и сфене (CaTiSiO5). Титан составляет около 0,57% земной коры.
От латинского titans, первых сынов Земли, в греческой мифологии.
Открыт Грегором в 1791 году; назван Клапротом в 1795 году. Нечистый титан был получен Нильсоном и Петтерссоном в 1887 году; однако чистый металл (99,9%) был получен только в 1910 году, когда Хантер нагрел TiCl4 с натрием в стальном бомбе.
Изображения
Свойства
Физические
Химические
Термодинамические
Ядерные
Распространённость
Реакционная способность
N/A
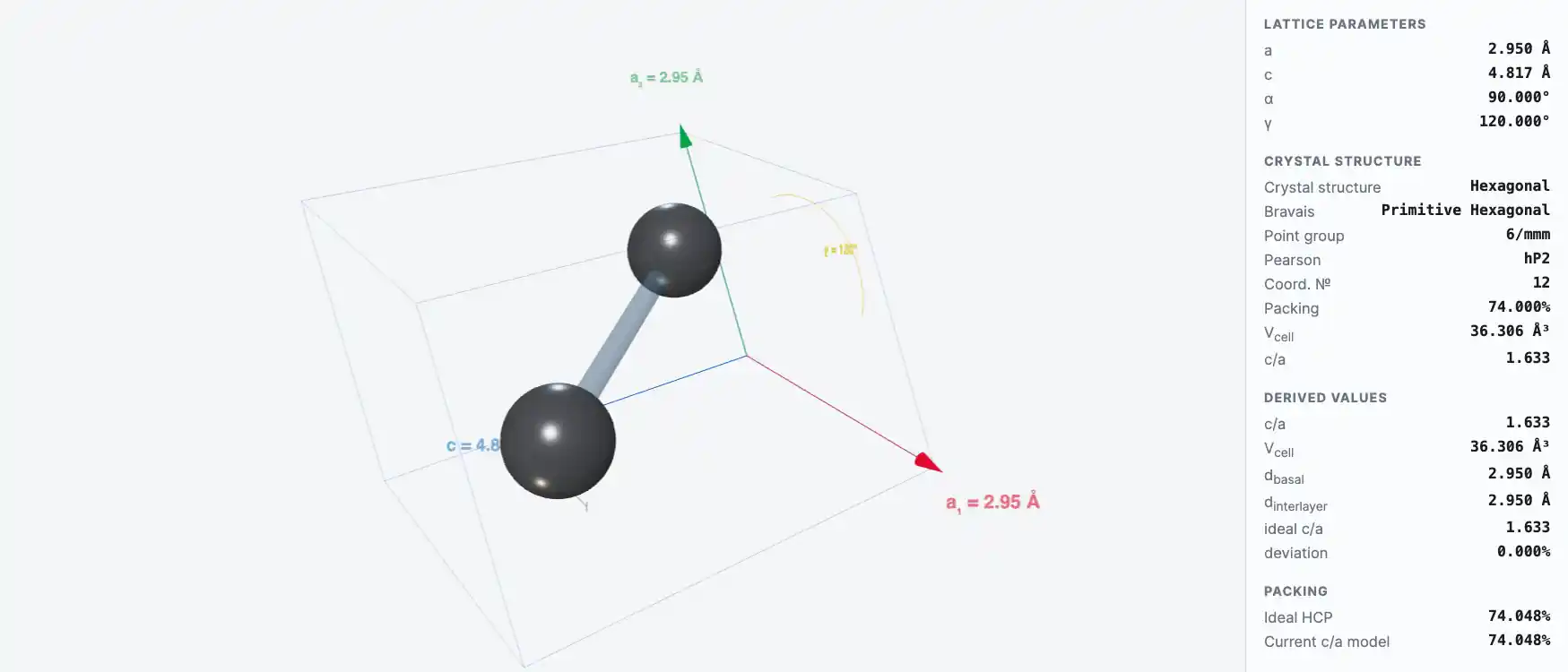
Кристаллическая структура
Электронная структура
Идентификаторы
Электронная конфигурация Measured
Ti: 3d² 4s²[Ar] 3d² 4s²1s² 2s² 2p⁶ 3s² 3p⁶ 3d² 4s²Модель атома
Изотопы меняют число нейтронов, массу и стабильность — но не электронную конфигурацию нейтрального атома.
Схематическая модель атома, не в масштабе.
Атомный отпечаток
Спектр испускания / поглощения
Распределение изотопов
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада |
|---|---|---|---|
| 46 Стабильный | 45,95262772 ± 0,00000035 | 8.2500% | Стабильный |
| 47 Стабильный | 46,95175879 ± 0,00000038 | 7.4400% | Стабильный |
| 48 Стабильный | 47,94794198 ± 0,00000038 | 73.7200% | Стабильный |
| 49 Стабильный | 48,94786568 ± 0,00000039 | 5.4100% | Стабильный |
| 50 Стабильный | 49,94478689 ± 0,00000039 | 5.1800% | Стабильный |
Фазовое состояние
Причина: на 1642.8 °C ниже точки плавления (1667.85 °C)
Схематично, не в масштабе
Точки фазовых переходов
Энергии переходов
Энергия для плавления 1 моля при tплав
Энергия для испарения 1 моля при tкип
Энергия для возгонки 1 моля при tвозг
Плотность
При нормальных условиях
При нормальных условиях
Атомные спектры
Показано 10 из 22 Атомные спектры. Сортировка по заряду иона (по возрастанию).
Состав спектральных линий ?
| Ion | Заряд | Total lines | Transition probabilities | Level designations |
|---|---|---|---|---|
| Ti I | 0 | 4029 | 496 | 4029 |
| Ti II | +1 | 1872 | 470 | 1872 |
| Ti III | +2 | 819 | 297 | 819 |
| Ti IV | +3 | 86 | 39 | 86 |
| Ti V | +4 | 252 | 4 | 252 |
| Ti VI | +5 | 71 | 14 | 71 |
| Ti VII | +6 | 92 | 13 | 92 |
| Ti VIII | +7 | 85 | 37 | 85 |
| Ti IX | +8 | 85 | 50 | 85 |
| Ti X | +9 | 162 | 78 | 162 |
Состав энергетических уровней ?
| Ion | Заряд | Levels |
|---|---|---|
| Ti I | 0 | 559 |
| Ti II | +1 | 253 |
| Ti III | +2 | 200 |
| Ti IV | +3 | 40 |
| Ti V | +4 | 66 |
| Ti VI | +5 | 59 |
| Ti VII | +6 | 62 |
| Ti VIII | +7 | 44 |
| Ti IX | +8 | 32 |
| Ti X | +9 | 83 |
Ионные радиусы
| Заряд | Координация | Спин | Радиус |
|---|---|---|---|
| +2 | 6 | N/A | 86 пм |
| +3 | 6 | N/A | 67 пм |
| +4 | 4 | N/A | 42 пм |
| +4 | 5 | N/A | 51 пм |
| +4 | 6 | N/A | 60.5 пм |
| +4 | 8 | N/A | 74 пм |
Соединения
Изотопы (5)
Natural titanium consists of five isotopes with atomic masses from 46 to 50. All are stable. Eight other unstable isotopes are known.
| Массовое число | Атомная масса (а.е.м.) | Природная распространённость | Период полураспада | Режим распада | |
|---|---|---|---|---|---|
| 46 Стабильный | 45,95262772 ± 0,00000035 | 8.2500% ± 0.0300% | Стабильный | stable | |
| 47 Стабильный | 46,95175879 ± 0,00000038 | 7.4400% ± 0.0200% | Стабильный | stable | |
| 48 Стабильный | 47,94794198 ± 0,00000038 | 73.7200% ± 0.0300% | Стабильный | stable | |
| 49 Стабильный | 48,94786568 ± 0,00000039 | 5.4100% ± 0.0200% | Стабильный | stable | |
| 50 Стабильный | 49,94478689 ± 0,00000039 | 5.1800% ± 0.0200% | Стабильный | stable |
Спектральные линии
Показано 50 из 1717 Спектральные линии. По умолчанию показаны только спектральные линии с измеренной интенсивностью.
| Длина волны (нм) | Интенсивность | Стадия ионизации | Тип | Переход | Точность | Источник | |
|---|---|---|---|---|---|---|---|
| 521.03843 нм | 21000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3F* | Измерено | NIST | |
| 506.46526 нм | 17000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3D* | Измерено | NIST | |
| 519.29686 нм | 17000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3F* | Измерено | NIST | |
| 517.37431 нм | 15000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3F* | Измерено | NIST | |
| 498.17305 нм | 14000 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 503.99574 нм | 14000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3D* | Измерено | NIST | |
| 468.19089 нм | 13000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3G* | Измерено | NIST | |
| 499.1066 нм | 13000 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 499.9503 нм | 12000 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 501.41861 нм | 11000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3D* | Измерено | NIST | |
| 399.86363 нм | 10000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(1P*) y 3F* | Измерено | NIST | |
| 466.75845 нм | 10000 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3G* | Измерено | NIST | |
| 500.72093 нм | 10000 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 453.32394 нм | 9200 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 398.17616 нм | 8800 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(1P*) y 3F* | Измерено | NIST | |
| 398.97582 нм | 8800 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(1P*) y 3F* | Измерено | NIST | |
| 501.42762 нм | 8700 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 395.82055 нм | 8600 | Ti I | emission | 3d2.4s2 a 3F → 3d3.(4F).4p y 3D* | Измерено | NIST | |
| 465.64693 нм | 8400 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(3P*) z 3G* | Измерено | NIST | |
| 395.63338 нм | 8000 | Ti I | emission | 3d2.4s2 a 3F → 3d3.(4F).4p y 3D* | Измерено | NIST | |
| 453.47761 нм | 7900 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 394.86705 нм | 7000 | Ti I | emission | 3d2.4s2 a 3F → 3d3.(4F).4p y 3D* | Измерено | NIST | |
| 484.08737 нм | 6600 | Ti I | emission | 3d2.4s2 a 1D → 3d2.(1D).4s.4p.(1P*) y 1D* | Измерено | NIST | |
| 430.59074 нм | 6400 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p x 5D* | Измерено | NIST | |
| 453.55686 нм | 6100 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 394.77683 нм | 5700 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(1D).4s.4p.(3P*) 3P* | Измерено | NIST | |
| 502.00263 нм | 5100 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 430.10787 нм | 4900 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p x 5D* | Измерено | NIST | |
| 503.5903 нм | 4900 | Ti I | emission | 3d3.(4F).4s b 3F → 3d3.(4F).4p w 3G* | Измерено | NIST | |
| 502.28679 нм | 4800 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 453.59176 нм | 4700 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 430.05538 нм | 4400 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p x 5D* | Измерено | NIST | |
| 453.60403 нм | 4000 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 503.64639 нм | 4000 | Ti I | emission | 3d3.(4F).4s b 3F → 3d3.(4F).4p w 3G* | Измерено | NIST | |
| 501.61609 нм | 3800 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 451.8022 нм | 3700 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 488.50794 нм | 3700 | Ti I | emission | 3d3.(2G).4s a 3G → 3d3.(2G).4p y 3H* | Измерено | NIST | |
| 392.45264 нм | 3600 | Ti I | emission | 3d2.4s2 a 3F → 3d3.(4F).4p y 3D* | Измерено | NIST | |
| 402.45711 нм | 3600 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(1P*) y 3F* | Измерено | NIST | |
| 390.47826 нм | 3500 | Ti I | emission | 3d2.4s2 a 1D → 3d2.(1D).4s.4p.(1P*) y 1F* | Измерено | NIST | |
| 452.2797 нм | 3500 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 502.48444 нм | 3500 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5G* | Измерено | NIST | |
| 398.24811 нм | 3400 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3P).4s.4p.(3P*) z 5S* | Измерено | NIST | |
| 454.87635 нм | 3400 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 455.24533 нм | 3400 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p y 5F* | Измерено | NIST | |
| 400.89274 нм | 3300 | Ti I | emission | 3d2.4s2 a 3F → 3d2.(3F).4s.4p.(1P*) y 3F* | Измерено | NIST | |
| 503.83979 нм | 3300 | Ti I | emission | 3d3.(4F).4s b 3F → 3d3.(4F).4p w 3G* | Измерено | NIST | |
| 392.98737 нм | 3200 | Ti I | emission | 3d2.4s2 a 3F → 3d3.(4F).4p y 3D* | Измерено | NIST | |
| 429.86657 нм | 3200 | Ti I | emission | 3d3.(4F).4s a 5F → 3d3.(4F).4p x 5D* | Измерено | NIST | |
| 489.99088 нм | 3200 | Ti I | emission | 3d3.(2G).4s a 3G → 3d3.(2G).4p y 3H* | Измерено | NIST |
Расширенные свойства
Ковалентные радиусы (расш.)
Радиусы Ван-дер-Ваальса
Атомные и металлические радиусы
Шкалы нумерации
Шкалы электроотрицательности
Поляризуемость и дисперсия
Химическое сродство
Параметры Мидемы
Риск поставок и экономика
Фазовые переходы и аллотропы
| Температура плавления | 1943.15 K |
| Температура кипения | 3560.15 K |
Категории степеней окисления
Расширенные справочные данные
Константы экранирования (7)
| n | Орбиталь | σ |
|---|---|---|
| 1 | s | 0.5591 |
| 2 | p | 3.9352 |
| 2 | s | 6.6234 |
| 3 | d | 13.8586 |
| 3 | p | 11.8963 |
| 3 | s | 10.9669 |
| 4 | s | 17.1832 |
Детализация кристаллических радиусов (6)
| Заряд | CN | Спин | rcrystal (pm) | Источник |
|---|---|---|---|---|
| 2 | VI | 100 | estimated, | |
| 3 | VI | 81 | from r^3 vs V plots, | |
| 4 | IV | 56 | calculated, | |
| 4 | V | 65 | calculated, | |
| 4 | VI | 74.5 | from r^3 vs V plots, | |
| 4 | VIII | 88 | calculated, |
Режимы распада изотопов (47)
| Изотоп | Режим | Интенсивность |
|---|---|---|
| 37 | p | — |
| 38 | 2p | — |
| 39 | B+ | 100% |
| 39 | B+p | 93.7% |
| 39 | 2p | — |
| 40 | B+ | 100% |
| 40 | B+p | 95.8% |
| 41 | B+ | 100% |
| 41 | B+p | 91.1% |
| 42 | B+ | 100% |
Факторы рассеяния X‑лучей (530)
| Энергия (eV) | f₁ | f₂ |
|---|---|---|
| 10 | — | 1.51668 |
| 10.1428 | — | 1.54246 |
| 10.3068 | — | 1.57217 |
| 10.4735 | — | 1.60245 |
| 10.6429 | — | 1.63331 |
| 10.8151 | — | 1.66477 |
| 10.99 | — | 1.70636 |
| 11.1677 | — | 1.75257 |
| 11.3484 | — | 1.80003 |
| 11.5319 | — | 1.84878 |
Дополнительные данные
Estimated Crustal Abundance
The estimated element abundance in the earth's crust.
5.65×103 milligrams per kilogram
Источники (1)
- [5] Titanium https://education.jlab.org/itselemental/ele022.html
Estimated Oceanic Abundance
The estimated element abundance in the earth's oceans.
1×10-3 milligrams per liter
Источники (1)
- [5] Titanium https://education.jlab.org/itselemental/ele022.html
Sources
Sources of this element.
Titanium is present in meteorites and the sun. Rocks obtained during the Apollo 17 lunar mission showed presence of 12.1% TiO2; rocks obtained during earlier Apollo missions show lower percentages.
Titanium oxide bands are prominent in the spectra of M-type stars. The element is the ninth most abundant in the crust of the earth. Titanium is almost always present in igneous rocks and in the sediments derived from them.
It occurs in the minerals rutile, ilmenite, and sphene, and is present in titanates and in many iron ores. Titanium is present in ash of coal, in plants, and in human body.
The metal was a laboratory curiosity until Kroll, in 1946, showed that titanium could be produced commercially by reducing titanium tetrachloride with magnesium. This method is still largely used for producing the metal. The metal can be purified by decomposing the iodide.
Источники (1)
- [6] Titanium https://periodic.lanl.gov/22.shtml
Источники
(9)
Data deposited in or computed by PubChem
The half-life and atomic mass data was provided by the Atomic Mass Data Center at the International Atomic Energy Agency.
Element data are cited from the Atomic weights of the elements (an IUPAC Technical Report). The IUPAC periodic table of elements can be found at https://iupac.org/what-we-do/periodic-table-of-elements/. Additional information can be found within IUPAC publication doi:10.1515/pac-2015-0703 Copyright © 2020 International Union of Pure and Applied Chemistry.
The information are cited from Pure Appl. Chem. 2018; 90(12): 1833-2092, https://doi.org/10.1515/pac-2015-0703.
Thomas Jefferson National Accelerator Facility (Jefferson Lab) is one of 17 national laboratories funded by the U.S. Department of Energy. The lab's primary mission is to conduct basic research of the atom's nucleus using the lab's unique particle accelerator, known as the Continuous Electron Beam Accelerator Facility (CEBAF). For more information visit https://www.jlab.org/
The periodic table at the LANL (Los Alamos National Laboratory) contains basic element information together with the history, source, properties, use, handling and more. The provenance data may be found from the link under the source name.
The periodic table contains NIST's critically-evaluated data on atomic properties of the elements. The provenance data that include data for atomic spectroscopy, X-ray and gamma ray, radiation dosimetry, nuclear physics, and condensed matter physics may be found from the link under the source name. Ref: https://www.nist.gov/pml/atomic-spectra-database
This section provides all form of data related to element Titanium.
The element property data was retrieved from publications.